Clear Sky Science · ja
シスプラチン耐性メラノーマにおけるサリノマイシン誘導細胞死でのオートファジーとp38 MAPKの相互作用
この研究が重要な理由
メラノーマは皮膚がんの中でも致死率が高い病型の一つで、腫瘍がしばしばシスプラチンのような標準化学療法薬に耐性を持つようになることが一因です。本研究は、抗生物質の一種であるサリノマイシンがその耐性を打ち破れるかを検討するとともに、薬剤の作用メカニズムを細胞内のリサイクル(オートファジー)やストレス応答系の観点から掘り下げています。治療後に一部のがんが再発する理由、そしてそれをいかに回避できるかに関心がある人々にとって、この研究は腫瘍細胞内で起きている生死の判断過程をのぞく手がかりを提供します。
がん細胞が治療に“聞かなく”なるとき
シスプラチンは多くの固形腫瘍に対して用いられる主要な薬剤ですが、メラノーマ細胞はしばしば適応して殺しにくくなります。研究者らはシスプラチン耐性を獲得させたマウス由来のメラノーマ細胞株を作製し、これにサリノマイシンを投与して評価しました。培養皿内では、サリノマイシンの濃度上昇に伴って生存細胞数が急速に減少し、プログラム化された細胞死の典型的な指標が出現し、短時間の曝露でも新しいコロニー形成能が失われました。シスプラチン耐性メラノーマ腫瘍を移植したマウスでは、サリノマイシンの注射により腫瘍増殖が著しく抑制され、腫瘍体積と重量が縮小しましたが、明らかな毒性は観察されませんでした。これらの結果は、サリノマイシンが従来の化学療法に反応しなくなったメラノーマ細胞にも効果を示し得ることを示唆しています。 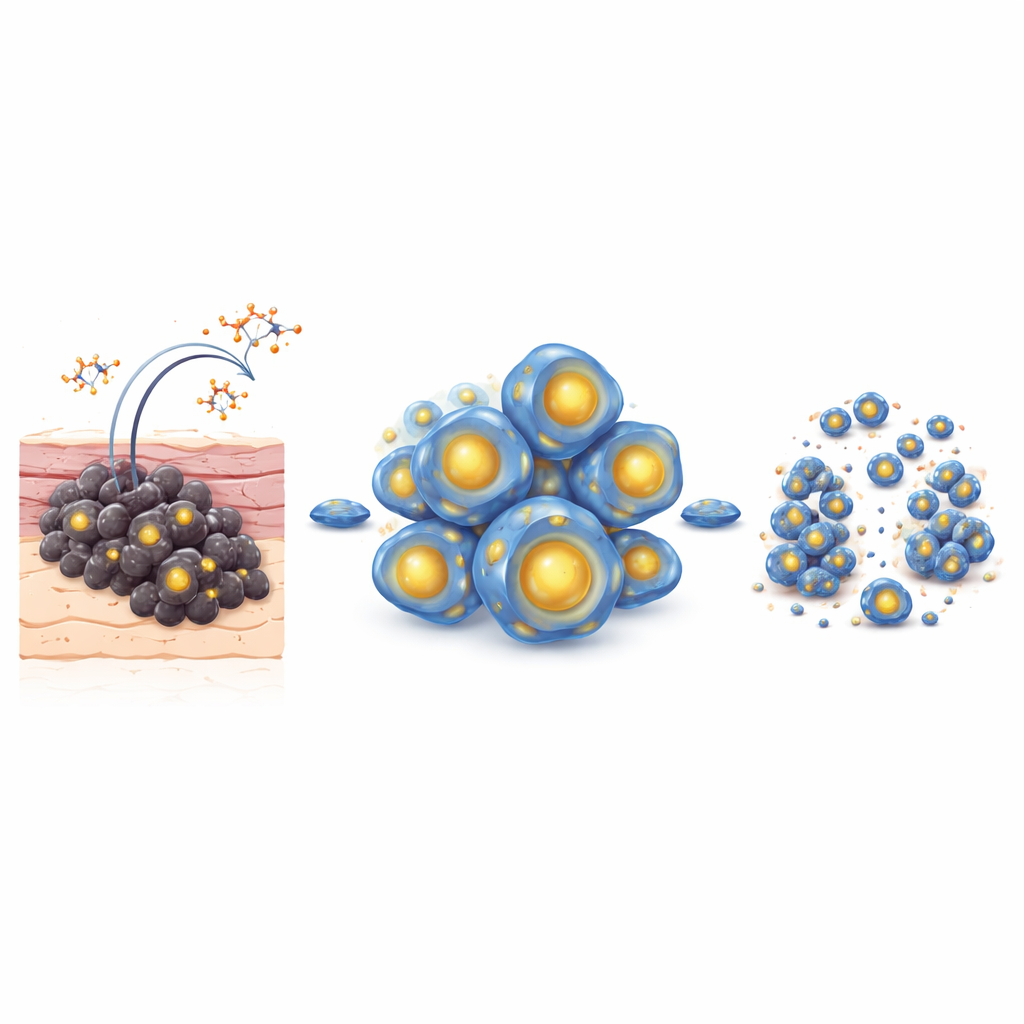
細胞ストレス、カルシウムの波、そして負荷のかかったリサイクル系
サリノマイシンが細胞内で何を引き起こすかを調べるため、研究チームはタンパク質の折りたたみや加工を担う小胞体(ER)に注目しました。サリノマイシンはイオンシャトルのように振る舞い、膜を介した電荷粒子の流れを攪乱するため、このオルガネラの機能不全を招きます。研究者らは、タンパク質折りたたみ装置が逼迫した際に現れるタンパク質マーカーの強い活性化を確認しました。同時に、小胞体から細胞質へ、さらにミトコンドリアへとカルシウムが大量に漏出する現象を検出しました。ミトコンドリアによるカルシウムの取り込みを阻害すると細胞死がさらに促進されたことから、通常ミトコンドリアはバッファーとして働き、サリノマイシンによるストレス下で死を遅らせていることが示唆されます。
自己清掃が致命的な渋滞に変わる
細胞は逆境に対処するために「自食(オートファジー)」と呼ばれる過程を利用し、損傷した物質を小胞に包んで酸性の分解区画に送って分解・再利用します。サリノマイシンはこの経路の初期段階を強く促進し、小胞形成を駆動するタンパク質を増加させました。しかし重要なのは、最終的な掃除段階が阻害されていた点です。本来分解されるべきマーカーが蓄積し、顕微鏡観察ではリソソーム(細胞の消化ユニット)と適切に融合しない大型の液胞様構造が観察されました。さらなる検査により、リソソーム膜の透過性が高まり、消化酵素が不適切な場所で活性化していることが示されました。その結果、再利用用の小胞が次々と形成される一方で効率的に処理されず、通常は保護的なプロセスが細胞死の引き金となる、いわば細胞内の交通渋滞が生じます。
腫瘍に対して反転させうるストレスシグナルのスイッチ
もう一つの重要な要素は、MAPキナーゼと総称されるストレス感知酵素群です。サリノマイシンはこの系の三つの枝を活性化しましたが、とりわけp38と呼ばれる枝が際立っていました。研究者らがp38を阻害すると、サリノマイシンはさらに多くのメラノーマ細胞を死に至らしめ、細胞質内の液胞の数とサイズが著しく増加しました。カルパインというカルシウム依存性酵素を阻害しても同様の効果が見られ、液胞の蓄積と長期生存への影響が示されました。対照的に、オートファジーをより効率的に進める薬(ラパマイシン)は再利用小胞の有害な蓄積を減らし、サリノマイシンから細胞を保護しました。これらの実験は、サリノマイシンによるストレス下でp38とカルパインがメラノーマ細胞にとって遅く不完全なリサイクル応答を生存戦術として利用させており、このバックアップを無効化すると薬剤の致死性が高まることを示唆します。 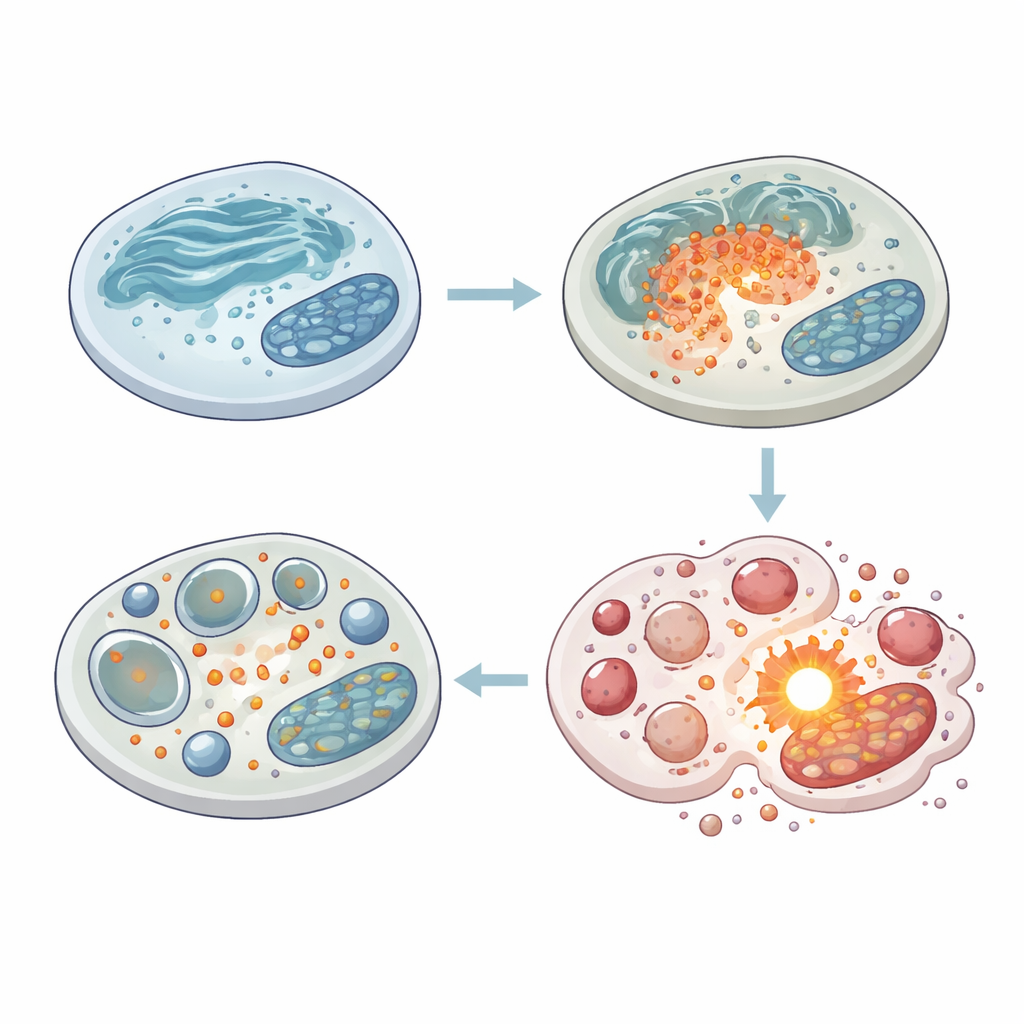
将来のがん治療にとっての意味
総じて本研究は、サリノマイシンがシスプラチン耐性メラノーマ細胞に重篤な内部ストレスを与え、カルシウムを過剰に流入させ、廃棄物処理システムを詰まらせ、最終的にプログラム細胞死へと導くという二面性を描き出しています。同時に、細胞はp38主導のリサイクル応答などを用いて自己防衛を試みます。臨床的な含意としては、サリノマイシンまたはその改良型をp38阻害剤やオートファジー阻害剤など生存経路を遮断する薬剤と組み合わせることで、各薬剤の用量を下げつつしぶといメラノーマ細胞を選択的に倒せる可能性があるという点です。臨床応用に至るまでにはなお多くの検討が必要ですが、本研究は併用療法が狙える脆弱性の詳細なロードマップを提供しています。
引用: Tyagi, M., Patro, B.S. Interplay between autophagy and p38 MAPK during salinomycin-induced cell death in cisplatin-resistant melanoma. Sci Rep 16, 9640 (2026). https://doi.org/10.1038/s41598-025-34796-5
キーワード: メラノーマ, 薬剤耐性, サリノマイシン, オートファジー, 併用療法