Clear Sky Science · ja
肺がんに対するワクチン候補設計のための腫瘍ピロトーシス関連抗原の同定と評価
なぜこの研究が肺がん患者にとって重要か
肺がんは依然として世界で最も致死率の高いがんであり、外科、化学療法、放射線療法、免疫療法といった現在の治療法でも長期的な選択肢を得られない患者が多く残っています。本研究はまったく別の発想を探ります:感染予防ではなく、免疫系を訓練して肺腫瘍をよりよく認識し攻撃させることを目的とした治療ワクチンです。高度な計算モデリングを用いて、著者らは完全にインシリコで、タンパク質ベースのワクチンを構築・試験し、ピロトーシスと呼ばれる炎症性の細胞死に結びつく分子を標的とすることで、より精密で持続的な肺がん治療への新たな道を切り開いています。
細胞死のスイッチをがんの標的に変える
研究者らは古典的ながんマーカーに焦点を当てる代わりに、ピロトーシスに関与するCARD8、NAIP、NLRP1、NLRP3という4つのタンパク質を選びました。ピロトーシスは爆発的なプログラム細胞死であり、免疫系に警告を発することがあります。これらのタンパク質は免疫調節に関与し、肺腺がんで生存率の向上と関連していることが示されているため、魅力的な標的です。著者らは、免疫系をこれらのタンパク質の小さな断片(エピトープ)を腫瘍細胞上で正確に認識するように訓練できれば、がん細胞を直接破壊するだけでなく、腫瘍に対するより広範な免疫応答を増幅できると考えました。
ワクチンを一つずつ組み上げる
免疫情報学ツールを使って、著者らは4つのタンパク質をスキャンし、T細胞およびB細胞に認識されると予測される短い配列(エピトープ)を同定しました。数百の候補の中から、免疫細胞に認識されやすく、かつ非毒性・非アレルゲンであると予測された15のエピトープを選び出しました。これらの断片は慎重に選んだ分子「スペーサー」でつなぎ合わせて一つの長いタンパク質にまとめられ、各エピトープがアクセス可能な状態に保たれるようにしました。免疫応答を高めるために、既知の細菌由来免疫賦活成分を3つアジュバントとして加えました。その結果できたコンストラクトは678アミノ酸からなり、安定性、可溶性、強い抗原性が予測されており、実用的なワクチンにとって重要な性質を兼ね備えています。
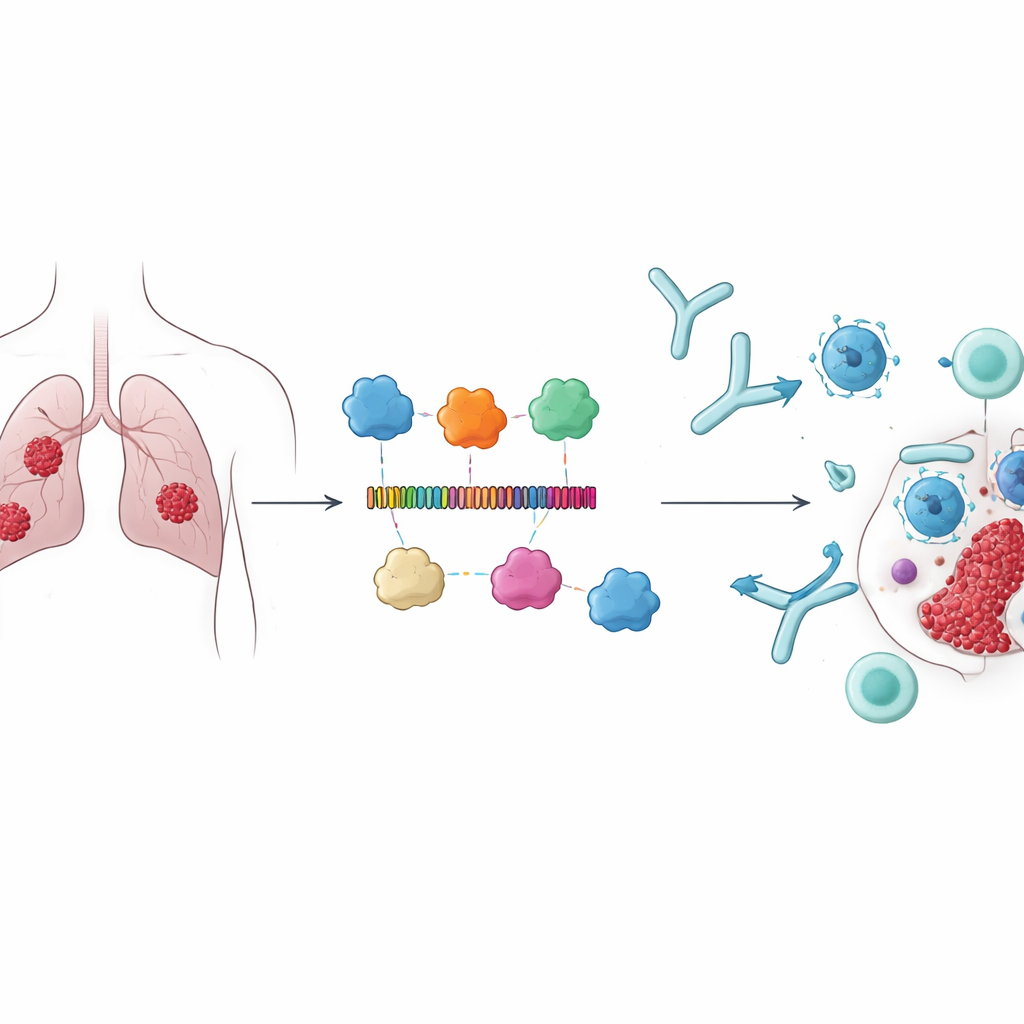
設計の形状と強度をコンピュータ上で試す
ワクチンの有効性は立体構造に大きく依存するため、研究チームは最先端の構造予測プログラムを用いて新しいタンパク質の3次元モデルを構築しました。これらのモデルを繰り返し精緻化し、標準的な構造評価指標で品質を検査した結果、現実的なタンパク質幾何学と安定性に関する厳しい基準を満たす最終版を採用しました。また、抗体が結合しやすい表面領域をマッピングし、タンパク質をさらに剛直化・安定化すると予測されるジスルフィド結合という内部の“橋”を設計しました。ワクチンが体内の水性環境でどのように振る舞うかを模倣するために、10回の独立した試行で合計100ナノ秒(100億分の1秒)の詳細な分子動力学シミュレーションを行いました。これらのシミュレーションを通じて、モデルタンパク質はコンパクトで構造的に安定なままであり、実際の条件下でも意図した形状を保持することが示唆されました。
免疫系がどのように反応するかをシミュレーション
次に研究者らは、ワクチンが免疫細胞上または細胞内に存在する主要な“警報”センサーであるトール様受容体(TLR)と相互作用できるかどうかを調べました。コンピュータ上のドッキング実験により、ワクチンとヒトの6種類のTLRとの間に強く安定した相互作用が示され、とりわけ強力な免疫カスケードを引き起こすことが知られるTLR5とTLR8との結合が顕著でした。さらに免疫系モデリングソフトを用いて一連のワクチン接種スケジュールをシミュレートしました。これらの仮想実験では、ワクチンを3回投与すると模擬抗原の迅速な除去、強い抗体波(特にIgMとIgG1)の発生、長期記憶B細胞およびヘルパーT細胞の増加が見られました。インターフェロン-γや各種インターロイキンなどの重要なシグナル分子も高まっており、自然免疫と獲得免疫の両方が活性化されていることを示しています。これは抗腫瘍防御に望まれるバランスの取れた応答です。
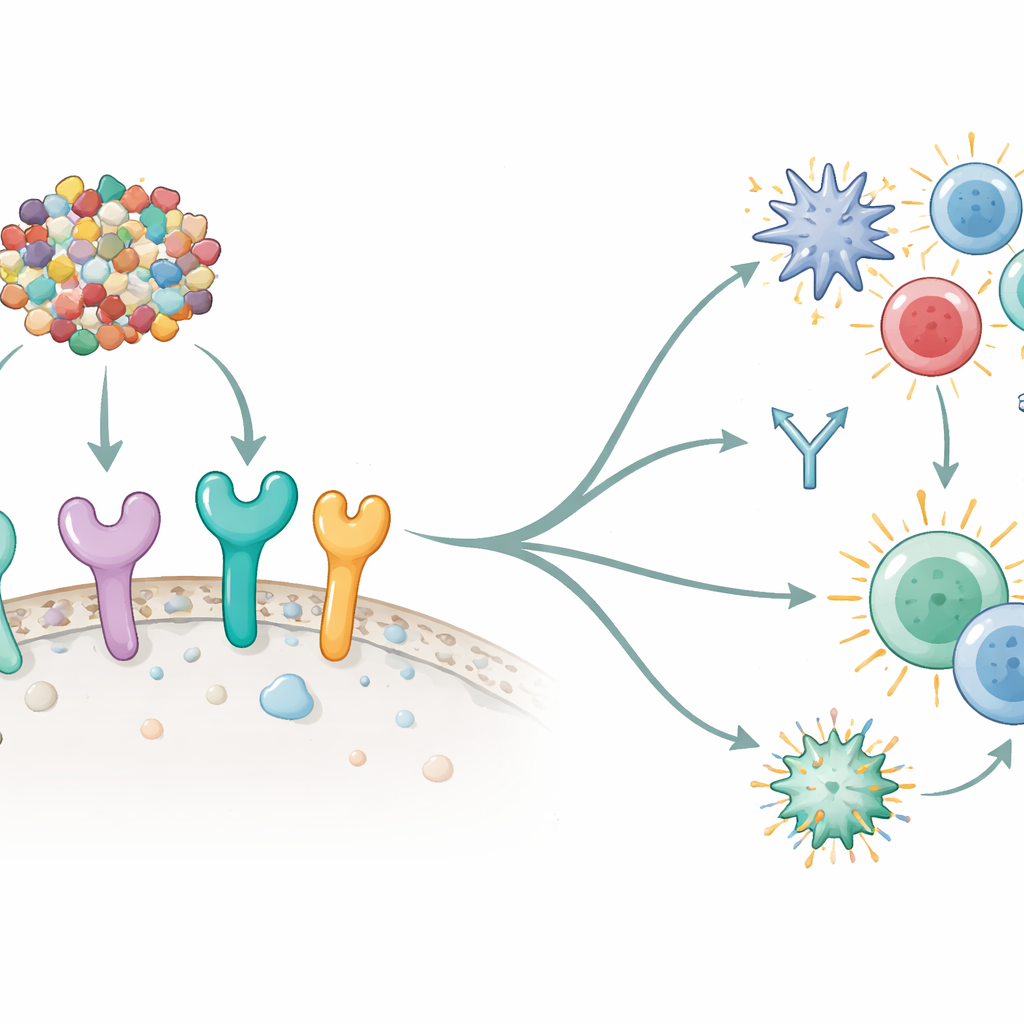
実製造に向けた準備
概念から実験室での試験へ移すために、チームはこのワクチンが一般的な細菌の実験用宿主である大腸菌で効率的に生産できるかを確認しました。ワクチンのタンパク質配列を変えずに遺伝コードを最適化することで、細菌によるタンパク質生産に好適な配列パターンとバランスの取れたDNAの化学的特性を達成しました。続いて最適化された遺伝子をタンパク質発現に用いられる標準的な実験用プラスミドに挿入する仮想クローニングを行いました。これらの手順は、実験室に持ち込まれた場合にワクチンがスケールで製造可能であることを示唆しています。
将来のがん治療にとっての意味
簡潔に言えば、本研究は炎症性の細胞死に結びつくタンパク質を標的とする肺がんワクチンの、徹底的にコンピュータ検証された設計図を提示しています。この設計は安全で安定し、シミュレーション上では免疫防御を強く活性化できると予測され、ヒト集団に広く適用可能であることが示唆されています。ただしこれはデジタル上のプロトタイプにすぎず、細胞・動物・最終的には人での検証が必要です。とはいえ本研究は、現代の計算ツールが試行錯誤に要する年月を一つの統合設計へと圧縮できることを示しています。今後の実験でこれらの予測が裏付けられれば、この種のワクチンは既存の治療法を補完し、患者自身の免疫系が肺腫瘍をより確実に認識して攻撃するのを助ける可能性があります。
引用: Nguyen, T.L., Kim, H. Identification and evaluation of tumor pyroptosis-associated antigens for design a vaccine candidate against lung cancer. Sci Rep 16, 9559 (2026). https://doi.org/10.1038/s41598-024-84792-4
キーワード: 肺がんワクチン, ピロトーシス, マルチエピトープ免疫療法, 計算機によるワクチン設計, 腫瘍免疫応答