Clear Sky Science · ja
ビタミンB2の代謝はFSP1の安定性を促進しフェロトーシスを防ぐ
一般的なビタミンが細胞の生死の判断を助ける仕組み
私たちの細胞は常に生存と自己破壊の綱渡りをしています。フェロトーシスと呼ばれる劇的な細胞死は、他の治療に抵抗するがん細胞を選択的に死に至らせうるため注目を集めています。本研究は、日常的な栄養素—ビタミンB2(リボフラビン)が、重要な保護タンパク質を安定化させることでひそかにその均衡を傾けていることを明らかにします。食事、細胞代謝、がん細胞死の間にあるこの隠れた結びつきを理解することは、研究者がより賢い治療法を設計し将来の栄養指針を見直す手がかりになるかもしれません。
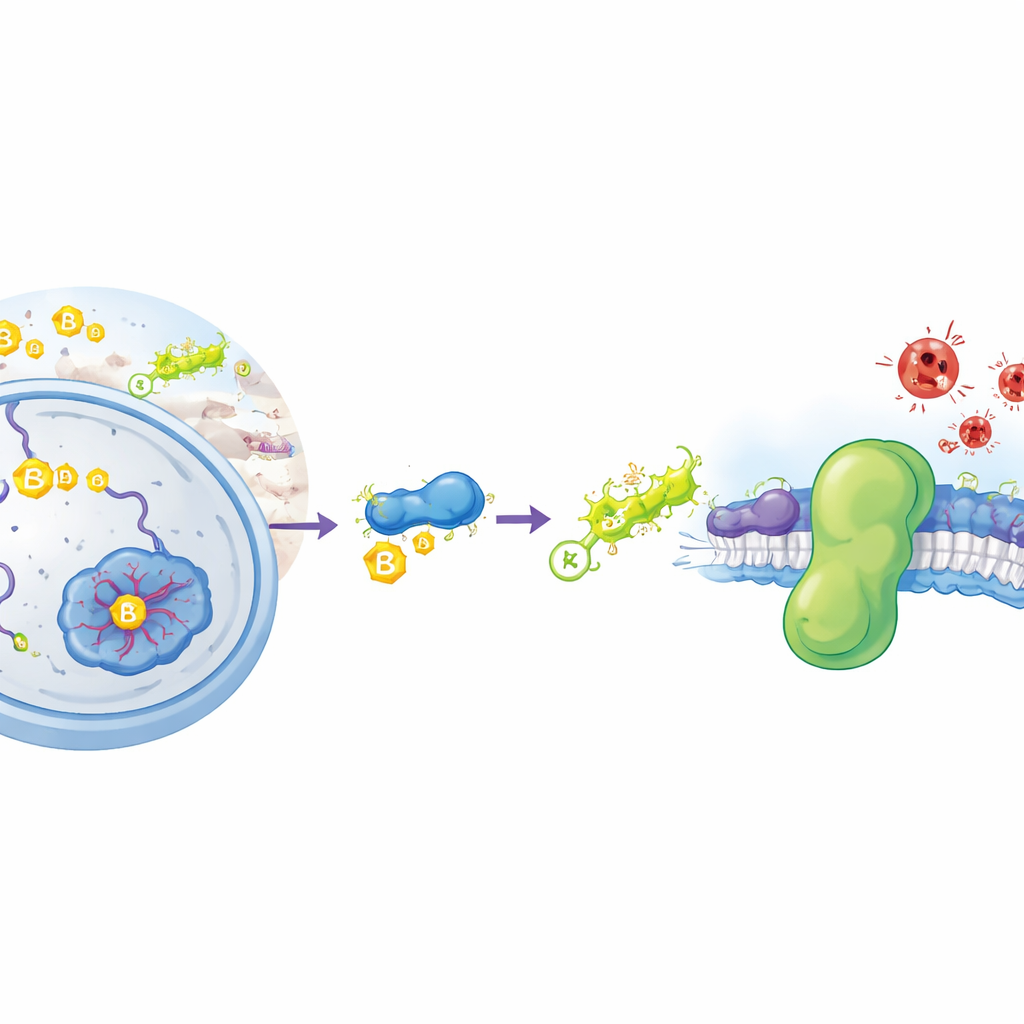
細胞内に起きる特別な“さび”
フェロトーシスは、金属のさびに似た化学的プロセス、すなわち細胞膜中の脂質の制御されない酸化によって引き起こされる細胞死の一種です。これらの脂質が壊れると膜の一体性が失われ細胞は破裂します。細胞は通常、これを防ぐためにいくつかの防御手段を展開します。主要な防御の一つはGPX4という酵素で、グルタチオンという小分子を用いて有害な脂質過酸化物を無毒化します。もう一つ平行する防御がFSP1というタンパク質で、細胞膜に位置し脂質様の小分子を使って拡散する前に破壊的なラジカルを捕らえます。がん細胞はしばしばフェロトーシスを回避するためにFSP1を増強しており、このタンパク質は新たな抗がん薬の重要な標的になっています。しかしこれまで、細胞がどのようにしてFSP1の産生量や寿命を制御しているのかは明らかではありませんでした。
死を阻む因子のための細胞内「燃料計」を作る
FSP1の隠れた管理役を明らかにするために、研究者たちはまずヒト骨肉腫細胞を蛍光レポーターを持つように設計しました。自然のFSP1タンパク質に緑色の光信号をタグ付けし、同時にFSP1のメッセージ量(mRNA量)を報告する青色の信号を結びつけました。この巧妙な設計により、遺伝子活性(青)とタンパク質安定性(緑)の変化を区別することができました。この二色システムを構築した上で、彼らはCRISPR–Cas9を用いてほぼ全ゲノムの遺伝子を系統的に破壊し、FSP1レベルが高い細胞と低い細胞を選別しました。各グループでどのガイドRNAが濃縮されているかを比較することで、遺伝子制御あるいはタンパク質の回転に作用してFSP1を増強または減少させる数百の遺伝子をマップしました。
ビタミンB2の隠れた役割:安定化用の“把手”を作ること
最も注目すべきヒットの中には、リボフラビンをFADという補酵素に変換するリボフラビンキナーゼ(RFK)とFADシンターゼ(FLAD1)という二つの酵素がありました。FSP1は通常FADをしっかりと結合して化学反応を行うフラボタンパク質です。RFKやFLAD1を除去したり、ビタミンB2欠乏の培地で細胞を培養すると、FSP1の遺伝子活性がほぼ同じであってもFSP1タンパク質の量が急激に低下しました。チームは、この喪失がGPX4を阻害した際に細胞をフェロトーシスに対してはるかに脆弱にしたことを示しました。重要なのは、ビタミンB2自体が古典的な抗酸化物質として機能したわけではないことです:感度の高い試験管内アッセイでは、ビタミンEとは異なり脂質の酸化を阻止できませんでした。代わりに、欠乏した細胞にFAD(および部分的にはその前駆体FMN)を添加するとFSP1のレベルとフェロトーシス耐性が回復しましたが、加工酵素が欠けている場合には追加のビタミンB2だけでは効果がありませんでした。
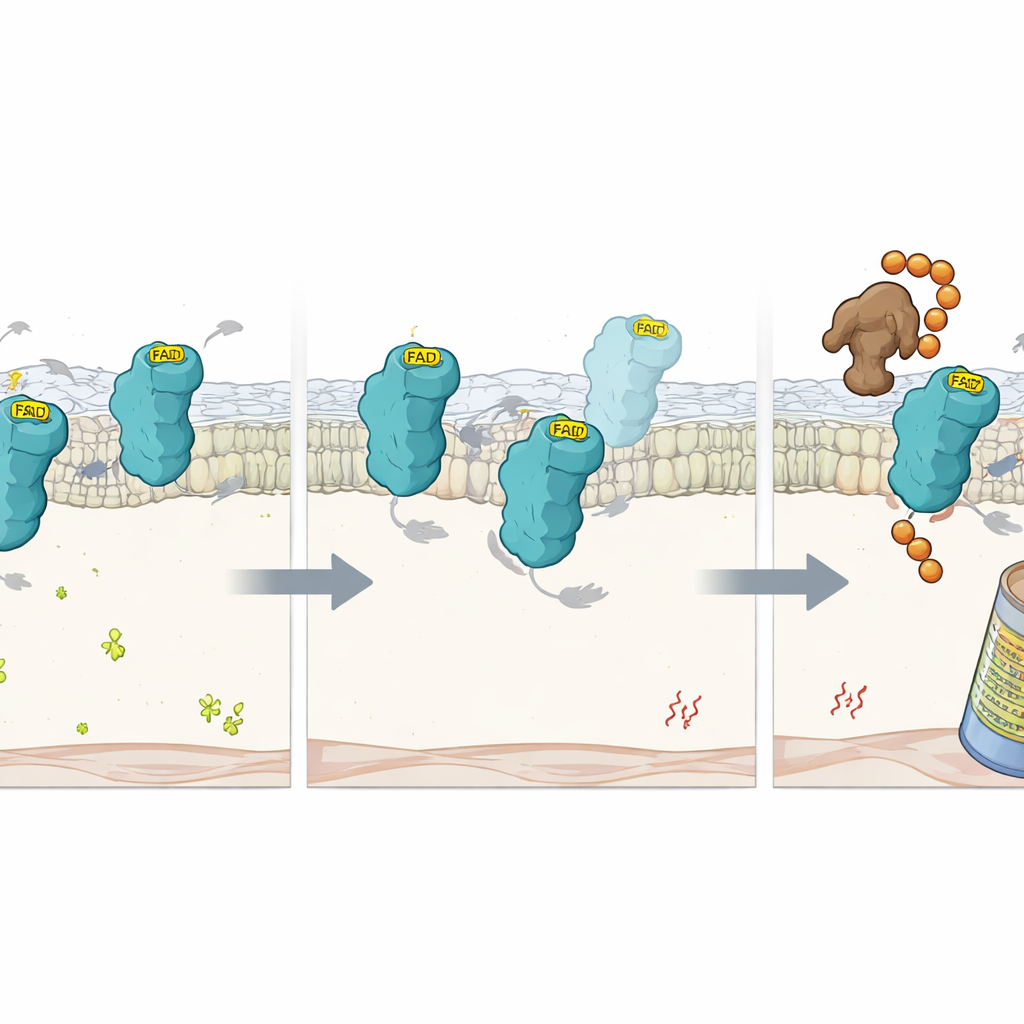
補因子が欠けると何が起きるか
さらに詳細を調べるため、科学者たちはFADを保持する能力を損なうFSP1の正確な変異体を研究しました。これらの変異タンパク質は概ね正常な折りたたみを示しましたがFADと触媒活性を失っていました。細胞内では、プロテアソーム(タンパク質を分解する機構)がブロックされない限り、これらは正常なFSP1よりもはるかに速く分解されました。これはFAD結合自体がFSP1を欠陥品としてタグ付けされるのから守る安定化用の把手のように働くことを示唆します。低FAD条件下での別の焦点を絞ったCRISPRスクリーニングにより、RNF8というE3リガーゼがFADを欠くFSP1を認識する重要な因子として同定されました。RFKが欠失するとRNF8は空のFSP1にユビキチン鎖を付加し、それをプロテアソームでの破壊へと導きました。RNF8を除去するとFAD不足の細胞でFSP1の回転が遅くなりましたが、補因子なしでは失われた保護機能を回復することはできませんでした。
分子回路からがん治療の着想へ
これらの断片を総合して、著者らは単純だが強力なモデルを提案します。ビタミンB2はRFKとFLAD1によってFADに変換され、これがFSP1に結合してその生化学的活性と寿命の両方に不可欠です。ビタミンB2の供給やその加工が滞ると、新しく作られたFSP1はFADを確保できずRNF8によりタグ付けされプロテアソームで速やかに分解され、結果として細胞はフェロトーシス損傷に対して脆弱になります。がんデータはRFK発現の高い腫瘍がフェロトーシス誘導薬に対してより耐性があることを示唆しており、この経路の実世界での関連性を裏付けています。専門外の読者への重要なメッセージは、身近なビタミンが単なる抗酸化物質以上の役割を果たしているということです:それは強力な抗死因子が守る側に立つか、取り払われるかを左右します。ビタミンB2代謝やFSP1の安定性を調整することで、将来的には健康な組織を守りながらがん細胞を選択的に消去するためにフェロトーシスをよりうまく利用する治療法が開発される可能性があります。
引用: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
キーワード: フェロトーシス, ビタミンB2, FSP1, がん細胞の死, 細胞代謝