Clear Sky Science · ja
転移因子要素(TE)–遺伝子キメラの地図作成、起源とトランスクリプトーム可塑性を高める役割
DNAに潜む隠れた同乗者
私たちのDNAの多くは、かつてゲノム内を寄生的に飛び回った古いウイルスの残骸である転移因子要素(transposable elements)でできています。本研究は、これらの古いウイルス断片が単なる沈黙する“ジャンク”ではないことを示します:それらは自分たちの遺伝子にスプライスしてハイブリッドなメッセージを作り、細胞が環境変化に適応するのを助け、時には疾患を促進することさえあります。発生、老化、がんにわたってこれらのキメラをマップすることで、ウイルス由来DNAが今日のヒト生物学を形作り続けている意外な道筋が明らかになりました。
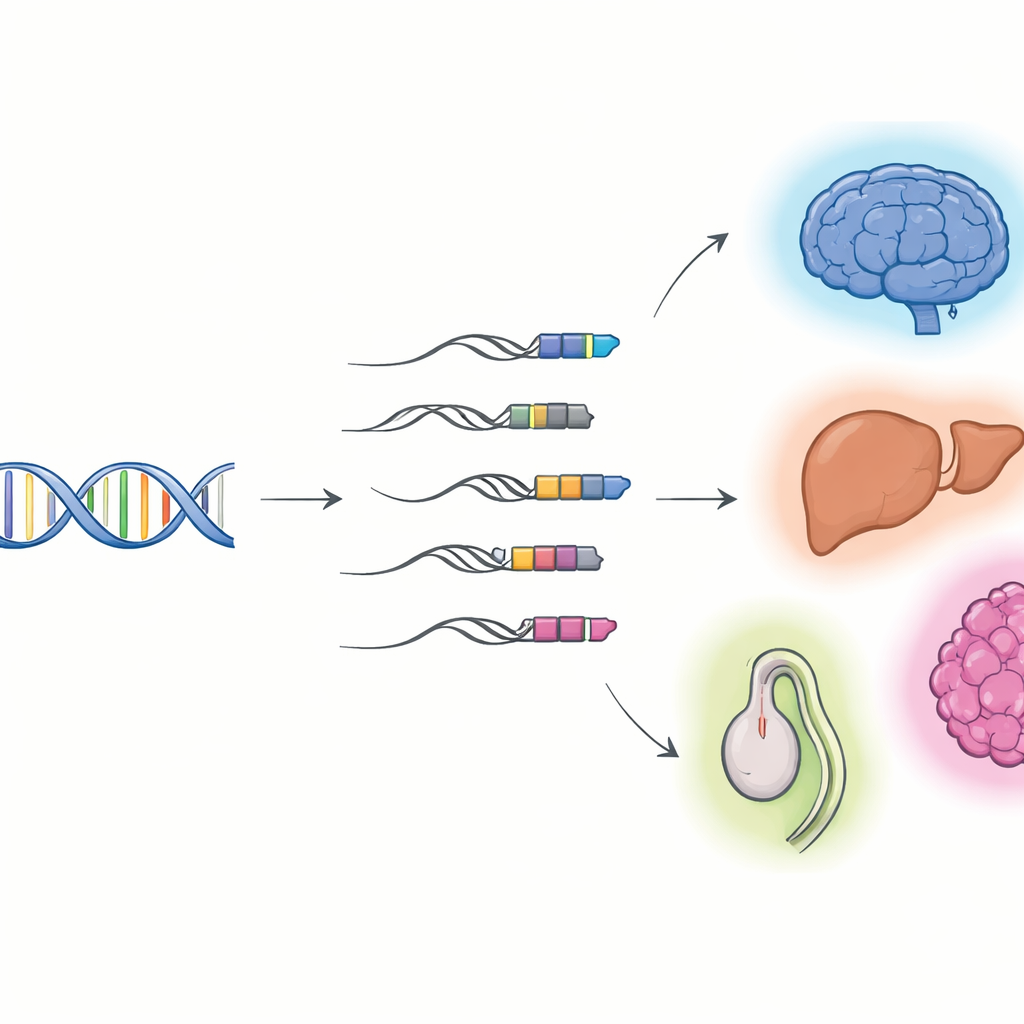
ウイルスDNAが私たちの遺伝子の一部になるとき
研究者たちは「TE–遺伝子キメラ」に注目しました:転移因子要素で始まりその後宿主遺伝子へと続くRNA分子です。全長を捉えられるロングリードシーケンシングと標準的なショートリードシーケンシングを組み合わせて、マウスとヒトの細胞や臓器におけるこれらのハイブリッドの詳細なカタログを作成しました。彼らはこれまで知られていなかった何千ものキメラ転写産物を発見し、その多くはタンパク質の設計図ではなくノンコーディングRNAでした。多くはロングターミナルリピート(LTR)と呼ばれるウイルス残骸の一群で始まり、これらは遺伝子の前方に位置して代替的なオン・オフスイッチのように振る舞うことがあります。組織や臓器ごとに使われるキメラの集合は異なり、特に脳、肝臓、精巣で活発で、胎児期から成人期へと組織が発達するにつれて利用が変化します。
老化とがんにおけるキメラ
これらのウイルス–宿主ハイブリッドが実際の集団でどのように振る舞うかを調べるために、研究チームは多数の臓器を含む何百人もの人からの大規模ヒトデータセットや腫瘍サンプルを解析しました。彼らは複数の個体に再現的に見られる数百の高信頼度キメラを同定しました。それらの発現は臓器間で異なるだけでなく年齢とも関連します:血液や脳のような組織では一部のLTR駆動キメラが高齢者で減少する一方、特定の末梢組織では増加することがあります。多くの種類のがんでは、これらのLTR基盤のハイブリッドは周辺の正常組織と比べて腫瘍で広く上昇しており、腫瘍でこれらを多く発現する患者は転帰が悪い傾向にあります。化学療法や免疫療法に抵抗性を示す患者のデータでは、新しく生じたLTR駆動のエクソンが影響する遺伝子群がこれらの薬剤の作用経路に関連していることが多く、TEキメラが治療圧に応じて腫瘍が再配線するのを助ける可能性を示唆しています。
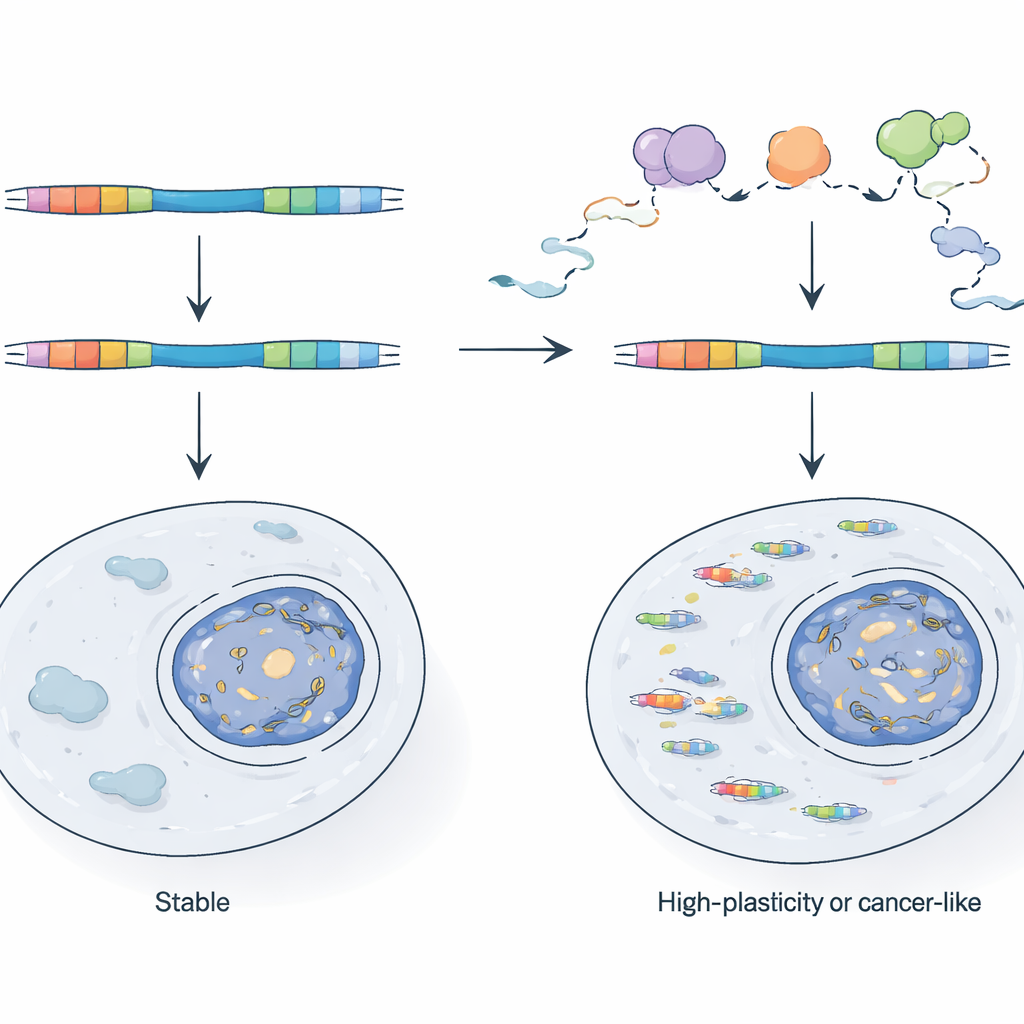
細胞はどのようにウイルス由来キメラを抑えているか
それらが強力であるにもかかわらず、なぜTEキメラが正常な細胞を圧倒しないのでしょうか?著者らは、細胞が核内エキソソーム複合体を中心としたRNA品質管理システムに依存して、多くのこれらの転写産物を生成過程で監視・破壊していることを示します。マウス幹細胞で重要なエキソソーム成分を遺伝学的に損なうと、LTR駆動プロモーターの活性が格段に高まりキメラRNAが急増します。新しく作られたRNAと安定なRNAを比較することで、いくつかのLTRはその転写産物が急速に分解されるため通常は抑えられている一方で、他は転写開始頻度のレベルで制御されていると示されました。これらの活性なLTRは、すでにアクセス可能で頻繁に転写されているゲノム領域に位置する傾向があり、活性な遺伝子やアンチセンス転写の近くにあること自体がウイルス断片を従来のエピジェネティックなサイレンシングから逃がす助けになることを示唆します。
スプライシング、幹細胞の可塑性、そしてウイルスの「マスタースイッチ」
細胞のスプライシング機構が撹乱されると、物語はさらに複雑になります。著者らは複数の主要スプライシング因子をノックダウンするかスプライスソームを化学的に阻害すると、エキソソーム喪失と共通する結果を観察しました:LTR駆動キメラと短くイントロンに乏しい遺伝子の強い増加です。勝ち組の一つに、非常に初期のマウス胚で活性な内在性レトロウイルスMERVLが含まれます。MERVLの内部配列とその下流の転写因子がアップレギュレートされると、幹細胞はより「全能様」状態、すなわち全ての組織を形成できる早期胚細胞に似た状態へとシフトします。逆に、アンチセンスオリゴヌクレオチドでMERVL RNAを分解するとこのシフトとLTRプロモーター活性が抑えられ、MERVLがより広いTEキメラと細胞状態可塑性のネットワークを引き起こすマスタースイッチとして機能することを示しています。
進化を通じたウイルス性イノベーション
多くの哺乳類ゲノムを横断して見ると、チームはどのTEファミリーがいつ宿主遺伝子にエクソンを供給し始めたかをたどります。ヒトとマウスの両方で、比較的若いLTRファミリーは宿主転写物の一部として読み取られる「センス」方向のキメラを形成しやすい傾向が特に強いことが示されました。このパターンは、新しいTE挿入の波が進化の過程で繰り返し遺伝子制御ネットワークに原材料を供給してきたことを示唆します。これらの挿入は純粋に有害というよりも、細胞の転写と分解の機構によって試験され、大部分はサイレンシングされるか分解されますが、少数が適切な位置と文脈に入ることで有用な制御要素や新しい遺伝子開始点として取り込まれるのです。
なぜこれらのウイルス残存物が重要なのか
専門外の読み手に向けて言えば、本研究はかつては無視されていたゲノムの大きな領域が、遺伝子の読み方、細胞のアイデンティティ変化、疾患の進行に積極的に影響を与えていることを示しています。古代のウイルス配列は代替的な遺伝子の「正面玄関」として利用されうるキメラRNAを生み出し、通常は細胞の掃除システムによって監視されています。その監視や正常なスプライシングが乱れると、これらのハイブリッドは急増して幹細胞をより可塑的な状態に押しやり、あるいは腫瘍が適応して治療に抵抗するのを助けることがあります。何百万年にもわたる進化はこれらのウイルス断片を繰り返しいじり、ゲノム寄生体から多くを規制複雑性の構成要素へと変えてきました。その結果、私たちのトランスクリプトームは単なる遺伝子の一覧よりもはるかに可塑的で動的なものになっているのです。
引用: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
キーワード: 転移因子要素, キメラ転写産物, RNA監視機構, 幹細胞の可塑性, がんの進化