Clear Sky Science · ja
酵母のアミノ酸感知SEAC–EGOCスーパーコンプレックスの構造と機能
細胞はいつ成長するかをどう決めるか
すべての細胞は成長する余裕があるか、資源を節約すべきかを常に判断しなければなりません。その判断はタンパク質の構成要素であり重要な窒素源でもあるアミノ酸に大きく依存します。本論文は、酵母細胞がどのように巨大な分子集合体を通じてアミノ酸の利用可能性を感知し、その情報を用いて主要な成長制御因子であるTORC1をオン・オフするかを、顕著な構造的詳細で解き明かします。同じ回路がヒト細胞にも保存され、がんや代謝に関連するため、酵母からの知見は我々自身の細胞が成長に適した条件をどのように判断するかを理解する手がかりを提供します。
細胞のリサイクルセンター上の精密なハブ
酵母では、SEACと呼ばれる中心的な意思決定複合体が液胞の膜上に位置します。液胞は細胞のリサイクルセンターとして機能します。そこでSEACはアミノ酸レベルに関する情報を伝える別の複合体EGOCと会合します。両者は協調して主要な成長スイッチであるTORC1に信号を伝えます。SEACは機能的に二つの半分から成り、TORC1をシャットダウンできるSEACITと、長くSEACITを抑制していると考えられていたSEACATです。著者らは高分解能のクライオ電子顕微鏡を用いて、EGOCに結合した完全なSEACを可視化し、シグナル伝達が実際に起こる液胞表面にあるこの分子ハブのスナップショットを捉えました。 
分子アーキテクチャを間近で見る
構造は、SEACがSEACATサブユニットで構成される大きなコアであり、そこから二つの柔軟なSEACITの“ウィング”が伸びていることを明らかにします。各ウィングは一つのEGOC複合体を結合できるため、単一のSEACが同時に二つのシグナル入力を扱えます。注目すべきは、EGOCがコアではなくウィングにのみ付着し、EGOCの有無でSEACの全体形状がほとんど変化しないことです。これはSEACATがSEACITの活性部位を物理的に塞ぐわけでも、EGOCの結合を妨げるわけでもないことを示します。液胞膜上での複合体の配向は、SEACコアが細胞質側を向いて追加の調節因子と相互作用できる一方で、ウィングは膜近傍に位置し、EGOCや他の膜結合パートナーと接触するのに理想的になっていることも示します。
SEACはどの信号を選ぶか
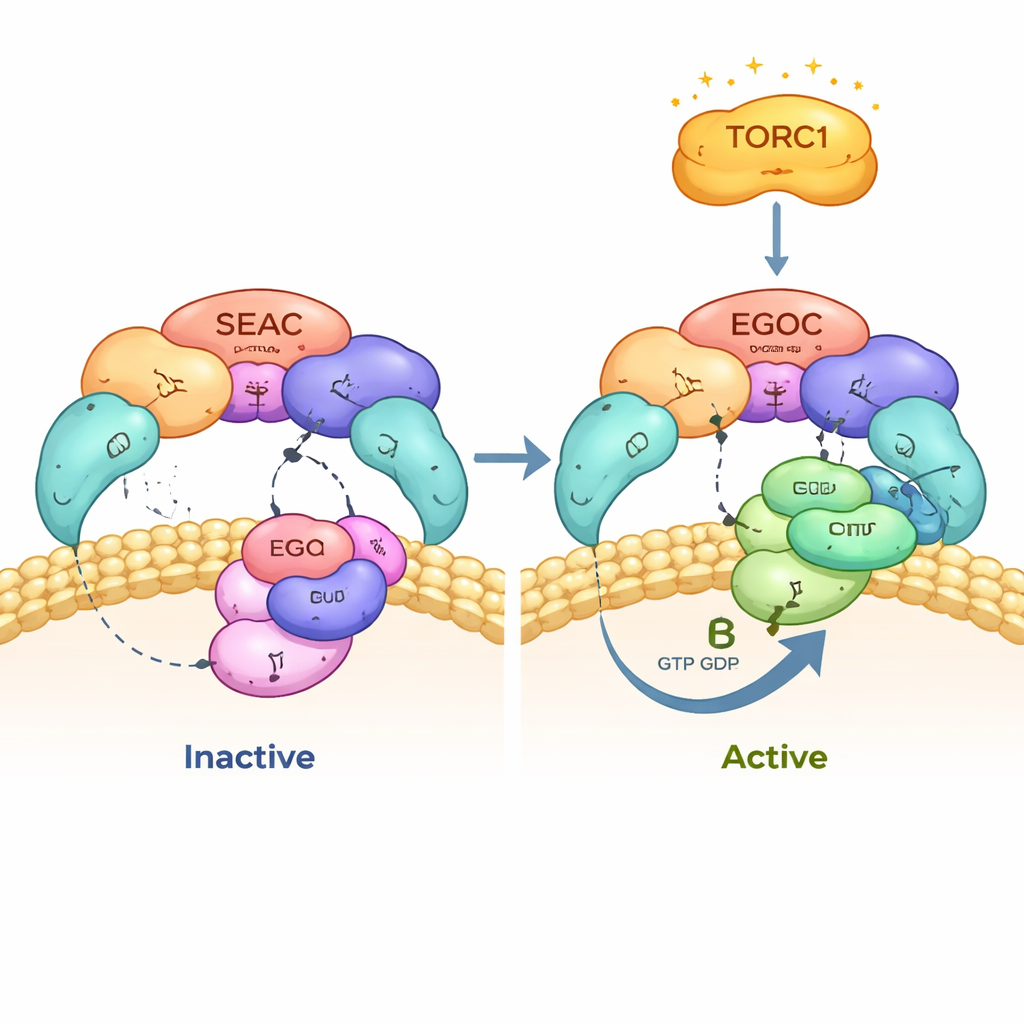
著者らはSEACとEGOCの接触部位を拡大して解析し、SEACがEGOCの“活性”型のみを認識することを見出しました。活性型では小さなGTPaseであるGtr1がGTP様ヌクレオチドを保持し、相方のGtr2はGDPを保持しています。SEACITは触媒的な“指”を提供し、それがGtr1のヌクレオチドポケットに届いてGTPの加水分解を促進し、EGOCを活性から不活性へと反転させます。詳細なクライオEMマップと変異実験は、この触媒指と隣接する補助残基が相互作用およびヌクレオチド状態の正確な読み取りに必須であることを示します。これらの重要な残基を変えたとき、SEACは液胞に正しく局在せず、EGOCは生産的に結合できなくなりました。
成長スイッチの迅速制御と遅延制御
生きた細胞における意味を理解するために、研究者らはアミノ酸を除去し再導入した際のTORC1活性を時間経過で追跡しました。正常な細胞では、窒素飢餓から数分でTORC1は迅速にオフになり、アミノ酸が戻るとすぐに再びオンになります。SEACITの触媒指を無効化するか、SEACITサブユニットを欠失させると、この初期時間窓でTORC1はほとんど反応しませんでした。同様のことはGtr1とGtr2の両方を除去した場合にも見られ、SEAC–EGOCペアがTORC1に対するアミノ酸制御の支配的で高速な経路であることを示します。しかし、後の時間—約30分前後—では、これらの変異体でもTORC1活性がゆっくりと調整され、GTPase系とは独立した別の遅い経路が細胞内で働いていることが示唆されます。
遠く離れたサブユニットの意外な役割
特に興味深い発見は、コアから突き出した柔軟な“プロペラ”領域を持つSEACATの構成要素Sea2に関するものです。Sea2またはそのプロペラを取り除くと、SEACの触媒活性が失われたときとほとんど同一のシグナル欠損が生じ、TORC1はアミノ酸除去と再導入の両方に対して鈍い応答を示しました。とはいえ、Sea2は触媒部位から遠く離れておりSEACITウィングに直接触れるわけではないため、単純なブロッキング機構は考えにくいです。Sea2欠失と触媒不活性SEAC変異体を組み合わせた遺伝学的実験は、GAP活性が完全にオンかオフかのいずれかに固定されると迅速応答が阻害され、中間的な調節が必要であることを示しました。著者らは、Sea2のプロペラがSEACITの活性を抑える未知の因子のドッキングプラットフォームとして機能し、TORC1を単に恒久的にオフにするのではなく微調整できるようにしていると提案します。
細胞の成長判断にとっての意義
総じて、本研究はSEACを対立する二つの集合体としてではなく、触媒ウィング(SEACIT)と構造コア(SEACAT)が協働してアミノ酸を感知し成長スイッチTORC1を迅速に調節する一つの統合された機械として再定義します。SEACITのEGOCに対する酵素的作用が迅速で正確な制御を提供し、Sea2のプロペラはこの活性を調節する因子を募集している可能性があります。同時に、より遅い平行経路が存在することで、主要なセンサーが乱されても最終的にはTORC1が栄養状態を反映するようになっています。密接に関連した複合体がヒト細胞でも同じ役割を担っているため、酵母からのこれらの洞察は栄養供給と成長のバランスを我々の細胞がどのように取っているかを照らし、TORC1シグナル伝達が誤動作する病態の理解にも示唆を与えます。
引用: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
キーワード: アミノ酸感知, TORC1シグナル伝達, SEAC GATOR複合体, 細胞成長制御, クライオ電子顕微鏡法