Clear Sky Science · ja
新規の小さなRNAをクライオ電子顕微鏡で構造決定するための四量体対称性を最適化した足場(スキャフォールド)
最小クラスのRNAの形を可視化する
すべての細胞内で、短い一本鎖RNAは遺伝子のオン・オフ切替、細胞損傷の感知、あるいは顕微鏡下での発光といった働きを担う小さな三次元構造に折りたたまれます。これらのRNAの多くは非常に小さいため、現在のイメージング法では正確な立体構造を明らかにするのが難しいことがあります。本稿は、こうしたとらえどころのない分子を可視化する巧妙な方法を紹介します。それは、自己組織化して大きな構造をつくるRNAの“枠”に目的のRNAを取り付けることで、凍結した生体分子を撮像する強力な手法であるクライオ電子顕微鏡(cryo-EM)で鮮明に観察できるようにするものです。
役立つRNAフレームの構築
研究者らはまず、ウイルス由来のRNA断片を出発点としました。この断片は本来、二量体を形成しやすい性質を持っています。彼らはこの配列を再設計し、従来ではごく一部しか対を作らなかったものが、溶液中でほぼ常に規則正しい二量体または四量体の形に組み上がるようにしました。こうした繰り返し構造が、事実上のRNAフレーム(スキャフォールド)を生み出し、元来の対称性を備えます。対称性はcryo-EMにおいて重要で、同一の繰り返しユニットを平均化することで最終画像の解像度を高められるからです。
既知のRNAを試験ゲストとして取り付ける
彼らはスキャフォールドがほかのRNAを視認可能にできるかを確かめるため、既によく研究されている分子をフレームの一領域に接ぎ木しました。1つは細菌由来のトランスファーRNA(tRNA)で、タンパク質合成でアミノ酸を運ぶ典型的なL字形分子です。もう1つはMango-IIIという小さな設計RNAで、色素と結合して発光するため蛍光タグとして広く使われています。どちらの場合も、結合体は設計どおりに折りたたまれ対を作り、cryo-EMは全体形状の詳細なマップを与えました。tRNAでは、ここで用いた修飾のない形と、以前に化学修飾で解析された形との微妙な違いまで検出できるほど鮮明でした。Mango-IIIでは、色素が結合するとアプタマーが著しく剛直化することがマップから示され、これが結合によって蛍光がオンになる仕組みを説明しています。 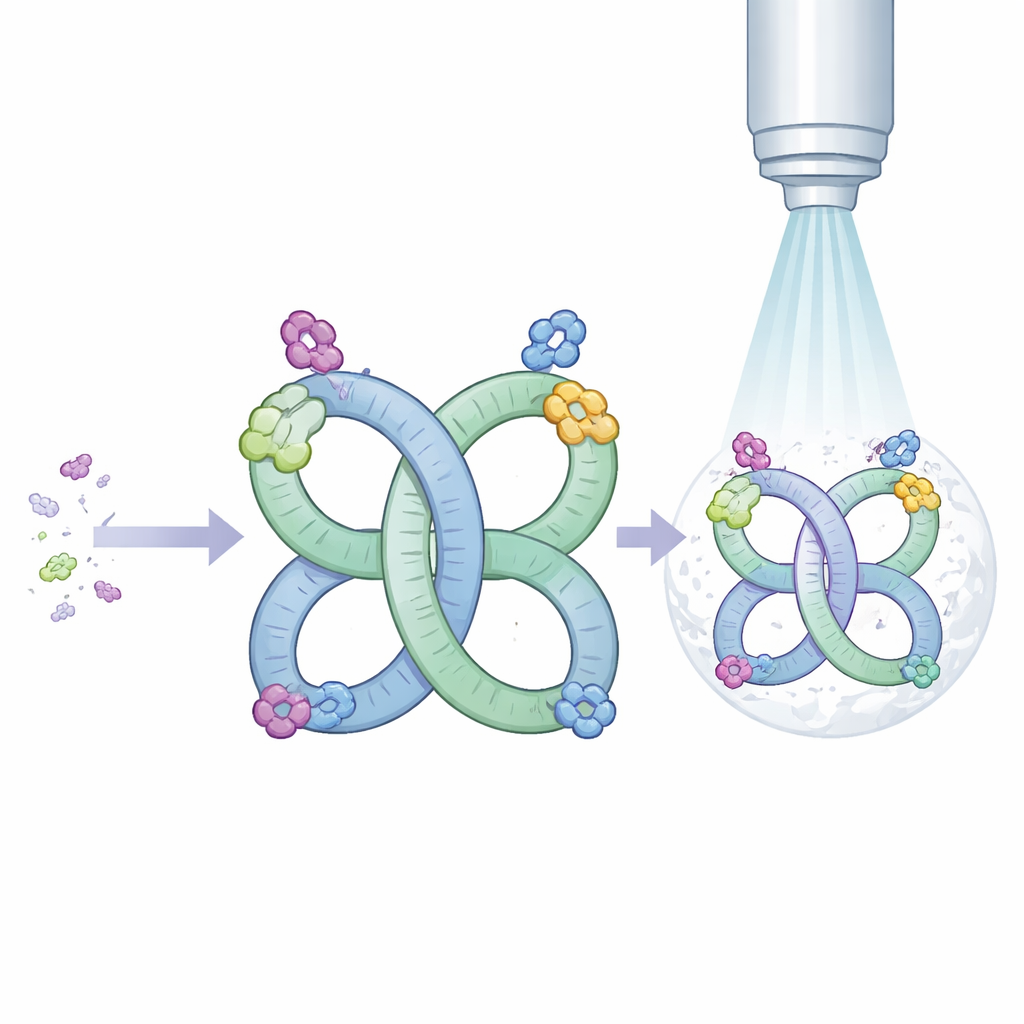
デザイナーRNAが小分子をどうつかむかを明らかにする
次に研究チームは、まだ全体構造が明らかでなかったRNAに取り組みました。彼らは二つの小さなアプタマー(試験管内で特定の小分子に結合するよう選択された短いRNA)をスキャフォールドに取り付けました。1つは医薬品キニーネを認識し、もう1つは8-オキソグアニン(酸化ストレス下で生じる塩基の損傷型)を感知します。スキャフォールドのおかげでcryo-EMは極めて高品質なマップを提供し、各RNA鎖を端から端まで追跡し、金属イオンや水分子の位置まで見分けられるほどでした。キニーネアプタマーでは、結合ポケットは主に積み重なり(スタッキング)と形の相補性で薬剤を包み込み、意外と少ない直接的な水素結合で安定化しています。一方、8-オキソグアニンアプタマーは配位相互作用に富んだ複雑な水素結合の網でリガンドを包み込み、損傷塩基のほとんどすべての化学的に異なる位置と接触しており、8-オキソグアニンと通常のグアニンを鋭く区別する理由を説明しています。
より鮮明な像のための柔軟な対称性
興味深いことに、同じRNAスキャフォールドは条件や取り付けたゲストによって、二量体または四量体のどちらにも組み上がることができます。四量体が形成されると、繰り返される幾何学がさらに画像品質を向上させます。ある例では、配列自体は二量体バージョンと同一であるにもかかわらず四量体の形をとり、塩基対のわずかなずれが全体のアセンブリを再編成することを示しました。著者らはまた、粒子がグリッド上で取りやすい偏った配向を克服するためのステージ傾斜の使い方や、画像処理時に対称性を課すことが構造を控えめながら一貫して鋭くする実務上の側面についても検討しています。
極小RNA機械を覗く新たな窓
総じて、この研究はコンパクトで対称性を持つRNAフレームが、通常は見えない小さなRNAを優れたcryo-EMの標的に変えうることを示しています。好条件では原子レベルを超える詳細も得られます。未知のRNAを単純なヘリックス状の接続でスキャフォールドに取り付けるだけで、その三次元折りたたみを決定し、小分子パートナーをどう掴むかを正確に観察し、その振る舞いを調節する秩序だった金属イオンや水分子を見つけられるようになります。一般向けの要点は、自然界やバイオテクノロジーで働く最小で最も多才なRNA機械のいくつかを実用的に詳しく観察できる手段が得られたことであり、新たなRNAベースのセンサー、医薬品、分子デバイスの合理的設計への道を開くということです。 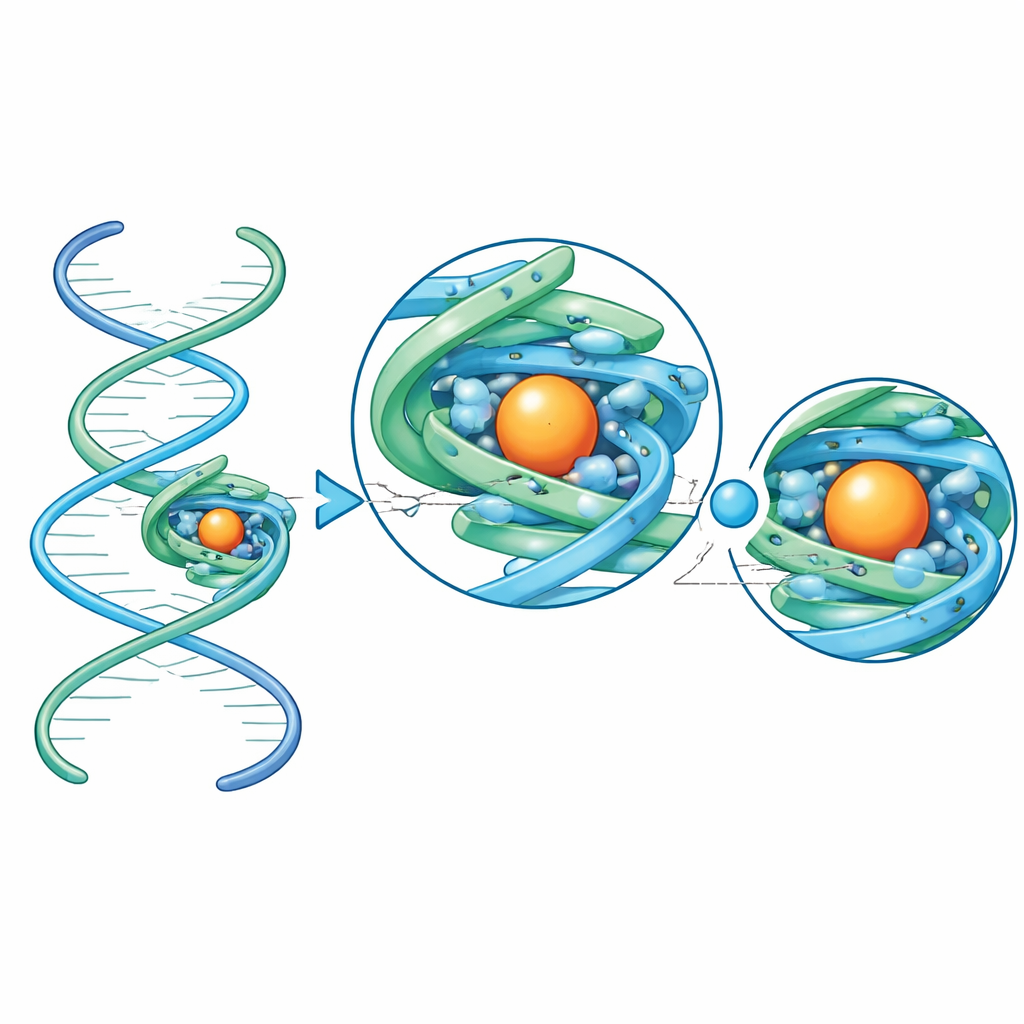
引用: Jones, C.P., Ferré-D’Amaré, A.R. Scaffolds with optimized quaternary symmetry for de novo cryoEM structure determination of small RNAs. Nat Methods 23, 609–616 (2026). https://doi.org/10.1038/s41592-026-03016-x
キーワード: RNA構造, クライオ電子顕微鏡, アプタマー, リボスイッチ, 分子スキャフォールド