Clear Sky Science · ja
AF2BIND: AlphaFold2のペア表現を用いた低分子結合部位の予測
蛋白質の海から薬の標的を見つける
現代の医薬品は、しばしば細胞内のタンパク質表面にある小さな凹みや隙間に結合することで作用します。それでも、今日の膨大なタンパク質構造カタログがあっても、小分子(潜在的な薬)が実際にどこに付着するかを事前に見極めるのは驚くほど難しいです。本研究はAF2BINDという、シンプルでありながら強力な計算ツールを紹介します。これは、画期的なタンパク質構造予測器であるAlphaFold2の内部表現を解析して、何千ものヒトタンパク質にわたって薬物結合の可能性が高い部位を浮かび上がらせることを目指します。その目的は、新薬探索の候補を絞り込み、従来の手法が見落としがちな機能的ホットスポットを明らかにすることです。
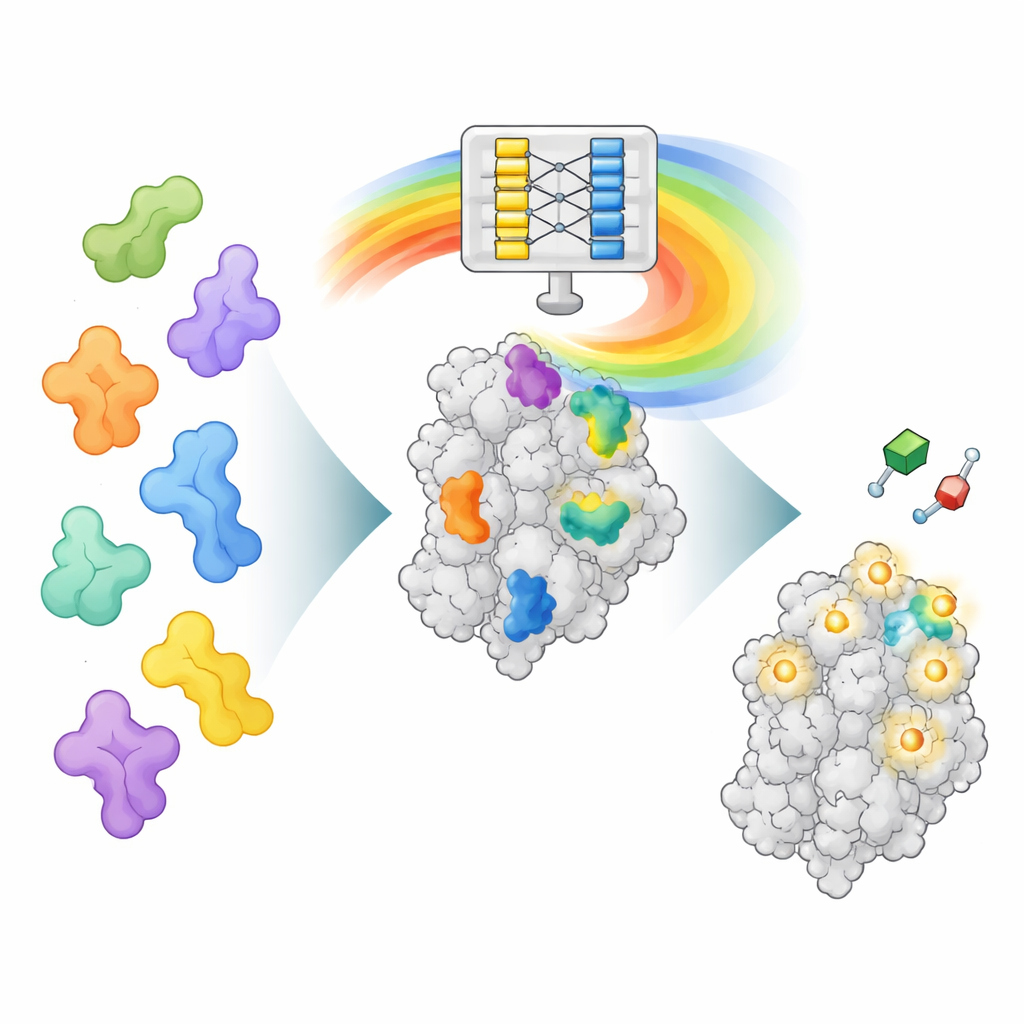
AlphaFoldの“頭脳”を読む新しい方法
AlphaFold2はアミノ酸配列がどのように三次元のタンパク質に折りたたまれるかを予測するように訓練されており、薬物がどこに結合するかを直接探すためのものではありません。しかし、タンパク質の折りたたみを学ぶ過程で、タンパク質の異なる部位がどのように相互作用するかについての豊富なパターンも獲得しています。AF2BINDはこれら内部データ層の一つであるペア表現にアクセスします。ペア表現はアミノ酸位置のペアごとに空間的な関係を符号化します。著者らはタンパク質配列とそのバックボーン構造をAlphaFold2に与え、さらに各種アミノ酸を1つずつそれぞれ別の「餌」鎖として20残基追加します。AlphaFold2はその後、タンパク質が各餌残基とどのように相互作用するかを計算します。これらの相互作用パターンが非常に単純なロジスティック回帰モデルへの入力となり、タンパク質内の各位置が低分子結合部位に属する確率を推定します。
隠れた信号を実用的な予測に変える
AF2BINDの訓練には、約1,900件の小分子が高品質な実験証拠で結合しているタンパク質–リガンド構造を注意深く選別したデータセットが必要でした。研究者らは類似性による「不正」を避けるためにかなりの工夫を行い、テスト用タンパク質が訓練に用いたものと全体的な折りたたみ、配列、さらには結合ポケット形状さえ共有しないようにデータを分割しました。この厳格なベンチマーク上で、AF2のペア表現は配列のみや構造条件付きの配列設計に基づく埋め込みを含むいくつかの代替ニューラルネットワーク埋め込みを上回りました。ペア特徴のみを用いて、AF2BINDは上位予測で既知の結合残基の約3分の2を回復し、標準的な分類指標でも高い性能を示しました。しかも、タンパク質の形状や側鎖向きの適度な変化に対して頑健でした。
餌残基から化学的手がかりを読む
AF2BINDは単純な線形モデルであるため、その判断は現代のAIシステムとしては比較的透明です。20種類の各餌アミノ酸は、特定のタンパク質位置における最終的な結合スコアに測定可能な寄与をします。約2,000のタンパク質–リガンド複合体にわたってこれらの寄与を調べたところ、ある餌の組み合わせは炭素に富む疎水性リガンドに対して強く働き、別の組み合わせはより極性で水を好む分子に反応することが分かりました。言い換えれば、餌の活性化パターンは、あるポケットがどの種類の小分子を好むかを示す粗い化学的フィンガープリントのように機能します。将来的には、AF2BINDに類するアプローチが、薬がどこに結合するかを示すだけでなく、どのような化学が最も適合するかの手がかりを与える可能性が示唆されます。
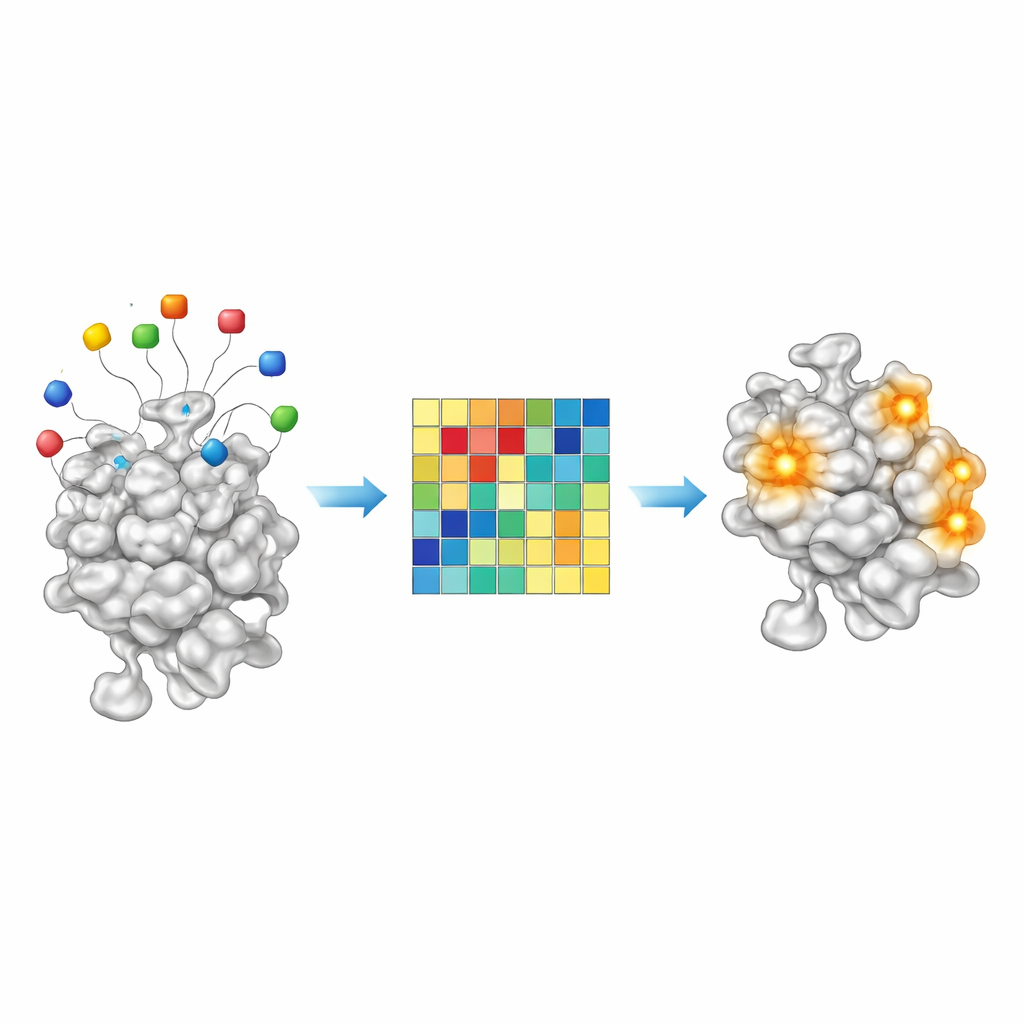
ヒトプロテオームの新しいポケットをスキャンする
訓練済みモデルを手に入れたチームは、AF2BINDをヒトプロテオーム全体のAlphaFold予測構造に適用しました。低信頼領域を切り落とし、非常に大きなタンパク質は扱いやすい構造チャンクに分割した後、近接する高スコア残基をクラスター化して候補結合部位を構築しました。AF2BINDは13,000以上のタンパク質で20,000を超えるこうした部位を予測しました。注目すべきは、これらの大部分が関連する結晶構造からリガンドをコピーするAlphaFillのような相同性ベース手法や、広く使われるポケット検出器P2Rankで推定されたポケットとは重ならない点でした。AF2BINDのみで検出された多くの部位は、古典的な埋没ポケットより浅かったり拡散的だったりし、しばしばペプチド、RNA、DNA、あるいは他のタンパク質と結合する領域—それでも小分子で狙える可能性のあるインターフェース—と一致していました。
創薬と疾患への含意
これら新たに示唆された部位が創薬にどれほど有望かを評価するため、著者らはポケットの大きさ、包囲性、化学環境に基づいて「薬剤適合性」をスコアリングする独立したツールを用いました。平均すると、AF2BINDの部位は一般的な閾値を上回り、遺伝性疾患に関連するタンパク質で見つかった部位も含め、魅力的な薬物標的と見なされました。細胞内の反応性システインに標識を付けるケモプロテオミクス実験と照合すると、AF2BINDとP2Rankは合わせて観察されたリガンド結合可能領域のおよそ半分を説明し、各手法が互いに見逃したケースを補い合っていました。本研究は、構造予測ネットワークが学習した内部表現を特定のリガンド情報なしに大規模に薬物結合部位の地図化に再利用できることを示しています。非専門家向けに言えば、タンパク質形状を予測するという同じAIの進歩が、薬がどこでどのようにその形状をしっかりつかむかを明らかにし始めており、新しい治療法探索を加速し、これまで隠れていたタンパク質内の制御点を照らし出す可能性がある、ということが主要なメッセージです。
引用: Gazizov, A., Lian, A., Goverde, C. et al. AF2BIND: predicting small-molecule binding sites using the pair representation of AlphaFold2. Nat Methods 23, 626–635 (2026). https://doi.org/10.1038/s41592-026-03011-2
キーワード: タンパク質結合部位, ドラッグディスカバリー, AlphaFold2, 計算生物学, 構造生物情報学