Clear Sky Science · ja
多発性骨髄腫におけるGPRC5D標的T細胞エンゲージャーへの多様な抗原逃避
標的免疫療法にがんが先回りするとき
強力な新しい免疫を基盤とする薬剤は、多発性骨髄腫という多くの患者で未だ治癒に至らない血液がんの治療を変えつつあります。これらの治療は、体内のT細胞をがん細胞表面に示された特定の「旗」に向けて誘導し、標的化された細胞を排除するよう働きます。有望な標的の一つがGPRC5Dという分子です。しかし多くの標的療法と同様に、腫瘍は進化して治療をすり抜けることがあります。本研究は、骨髄腫細胞がどのようにGPRC5Dの旗を変化させたり隠したりして、高効力のT細胞エンゲージャー薬から逃れるのかを詳細に解き明かしています。
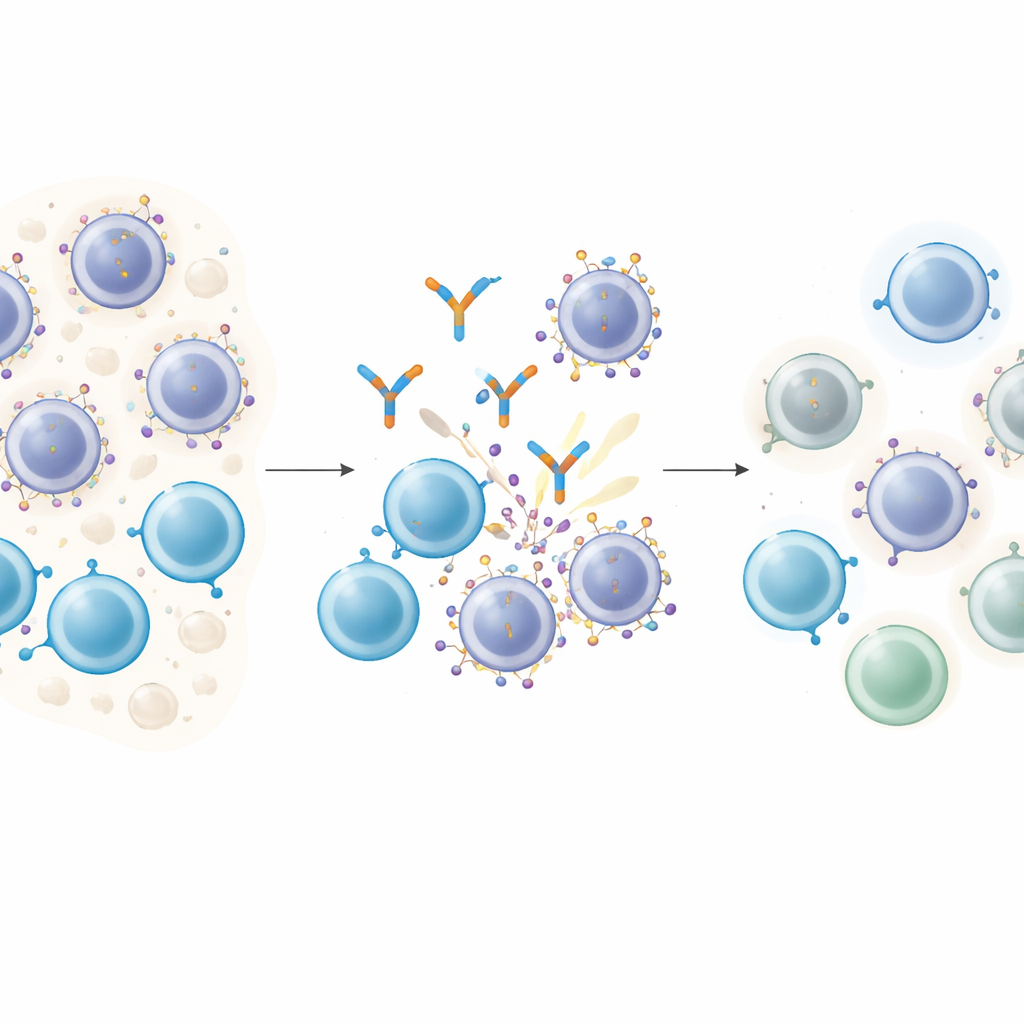
薬はどうやってがん細胞に「鍵」をかけるのか
T細胞エンゲージャー抗体は分子の仲介役のように働きます:一端がT細胞をつかみ、もう一端ががん細胞上の標的分子に結合して両者を直接接触させ、T細胞が標的を殺せるようにします。多発性骨髄腫では、GPRC5Dは悪性形質細胞に多く発現し、正常組織には乏しいため魅力的な標的です。GPRC5Dを標的とするtalquetamabという薬で治療された患者はしばしば深い寛解を得ます。しかし、ほとんどの患者がやがて再発するため重要な疑問が生じます:がん細胞は、これらの薬が依存する標的そのものを変えてしまっているのか?
腫瘍の進化をリアルタイムで追う
研究者らは、talquetamabを受けた治療困難な骨髄腫患者21人を追跡しました。治療前の骨髄サンプルを一部の患者から採取し、再発時にも再度採取して、DNA、RNA、クロマチン解析の多層的手法で腫瘍細胞を詳しく調べました。この超詳細な解析により、再発患者のおよそ3分の2で、がんはtalquetamabの効果を弱めたり阻害したりするようにGPRC5Dを変化させていることが明らかになりました。注目すべきは、異なる抵抗性サブクローン(遺伝的に異なる腫瘍の枝)が同一人物内で共存することが多く、逃避に向かう進化が同時に複数の経路を辿ることがある点です。
腫瘍が標的を隠す三つの主要な道筋
チームは、骨髄腫細胞が認識を免れる再現性のある三つのパターンを見つけました。一部の患者では、GPRC5D遺伝子を含む染色体の領域が両対立遺伝子で欠失し、細胞表面から旗が完全に消失していました。別の患者群では、塩基一つの置換や小さな挿入・欠失といった小規模な変化がGPRC5Dタンパク質の重要領域を歪めていました。これらの多くは、タンパク質が細胞内から外膜へ正しく輸送されるのに必要な部分を損ない、GPRC5Dが細胞外に表示されず内部コンパートメントに留まる原因となっていました。第三の経路はエピジェネティックなサイレンシングで、GPRC5Dを取り巻くDNAが密にパッケージされ化学的修飾を受けることで、その配列自体は比較的保たれていても遺伝子の読み取りが著しく抑えられ、ほとんどまたは全くGPRC5Dを産生しないというものでした。
旗が存在しても鍵が合わなくなる場合
すべての逃避経路がGPRC5Dを細胞表面から取り除くわけではありませんでした。あるケースでは、標準的な検査ではタンパク質が正常に見えても、薬が鍵として合わなくなっていました。研究チームは特定患者由来の変異を培養細胞に再現し、異なるGPRC5D標的抗体がこれらの細胞にどれほど結合し殺傷できるかを検証しました。ある変異はtalquetamabが受容体をとらえる正確な部位を微妙に変え、受容体が通常の染色で見えるにもかかわらず薬の結合や細胞死誘導能を著しく低下させました。興味深いことに、受容体の2か所に同時に結合する別のGPRC5D標的薬は、いくつかの変異体に対して依然として有効であり、マルチバレントや複数エピトープ結合といった薬剤設計が抵抗性クローンの生存に影響を与え得ることを示しています。
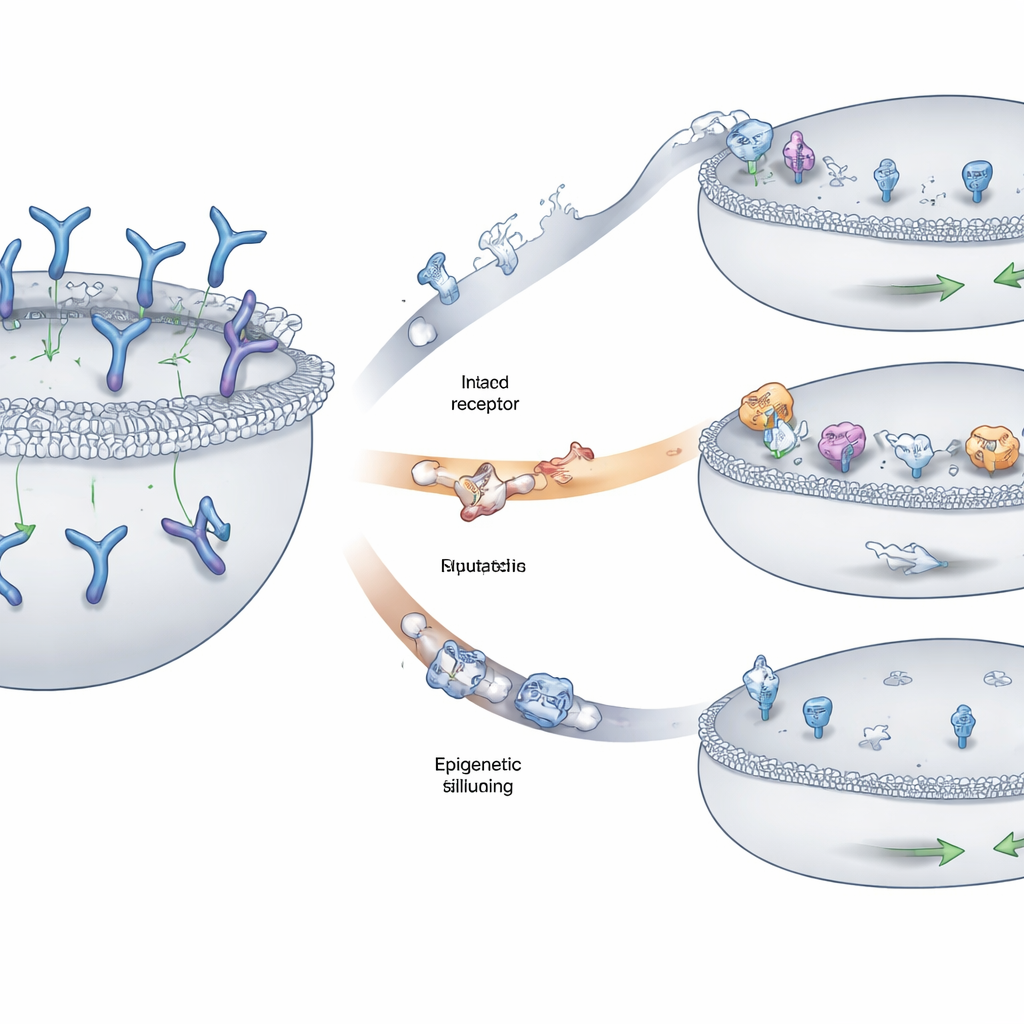
標的以外:免疫攻撃のほかの限界
ほとんどの再発例では何らかの形でGPRC5Dの喪失や変化が見られましたが、少数の患者では標的自体に明白な変化がないまま再発していました。これらのケースでは問題はT細胞側にあり、実験室試験でのがん細胞殺傷能力が低下していて、長期にわたるエンゲージャー療法への持続的曝露が免疫系を疲弊させる可能性が示唆されました。研究はまた、特定の遺伝学的サブタイプ(t(11;14)という染色体転座を伴うもの)が元々GPRC5D遺伝子をより「閉じた」クロマチン状態に保ち、基礎発現が低めであることも明らかにしました。これは、腫瘍が初めから標的のレベルが低いことで反応不良になりやすい患者がいる可能性を示唆します。
患者と今後の治療への含意
患者や臨床医にとって、この研究はなぜ非常に強力なGPRC5D標的療法であってもまだ根治にならないのかを説明します:骨髄腫細胞は、まさにこれらの薬が頼る旗を欠失、再構成、誤輸送、あるいはオフにすることができ、しかもしばしば複数の方法を同時に用います。所見は、単にタンパク質レベルを測るだけでなく腫瘍DNAをモニターすることが、標準検査では見落とされがちな出現する逃避変異を検出する上で重要であることを示唆します。また、複数箇所に強く結合する薬、同時に複数の標的を攻める併用、あるいはサイレンシングされた遺伝子を再活性化する薬剤といった次世代戦略が、腫瘍進化に先んじるために有望であることを示しています。本質的にこの研究は、骨髄腫が用いる逃避経路を地図化し、将来の治療がそれらを封じるよう設計され、T細胞を基盤とする治療の有効期間を延ばせるようにするための手掛かりを提供します。
引用: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
キーワード: 多発性骨髄腫, T細胞エンゲージャー, GPRC5D, 抗原逃避, がん免疫療法