Clear Sky Science · ja
免疫チェックポイント阻害に耐性を示す進行固形腫瘍におけるリナボンキバートとペムブロリズマブ:第1相試験
なぜ手強いがんが私たち全員に関係するのか
免疫系の“ブレーキ”を外す免疫療法薬は多くのがん治療を変えましたが、大半の患者は最初から効果が出ないか、いずれ腫瘍が再び増大します。本研究は、腫瘍が免疫攻撃から隠れるために使う強力な防御機構を無力化するよう設計された新しい抗体薬リナボンキバートを試験し、既存の免疫療法であるペムブロリズマブと組み合わせて評価します。その結果は、チェックポイント阻害薬に既に抵抗を示していた患者でも、免疫制御を回復させつつ副作用を抑えられる可能性があることを初期的に示唆します。
腫瘍を取り巻く隠れた盾
多くの現代的免疫療法薬は、通常T細胞を抑制するPD‑1のような「チェックポイント」分子を遮断して働きます。これらのブレーキが外れると、免疫細胞はがんをより活発に攻撃できます。しかし腫瘍はしばしば、キラーT細胞が近づけない、あるいは到着しても弱められてしまうような敵対的な微小環境を作り出して適応します。この保護バブルの重要な設計者の一つがTGFβ1と呼ばれるシグナル伝達タンパク質で、がん細胞や周囲の支持細胞の両方が産生します。TGFβファミリー全体を阻害する以前の試みは有望でしたが、他のファミリー分子が正常組織に重要であるため心血管や出血性の重大な問題が生じました。リナボンキバートは、この難題を回避するよう設計され、活性化される前の潜在的で不活性なTGFβ1だけを選択的に中和し、体に必要な近縁分子は残すよう作られています。
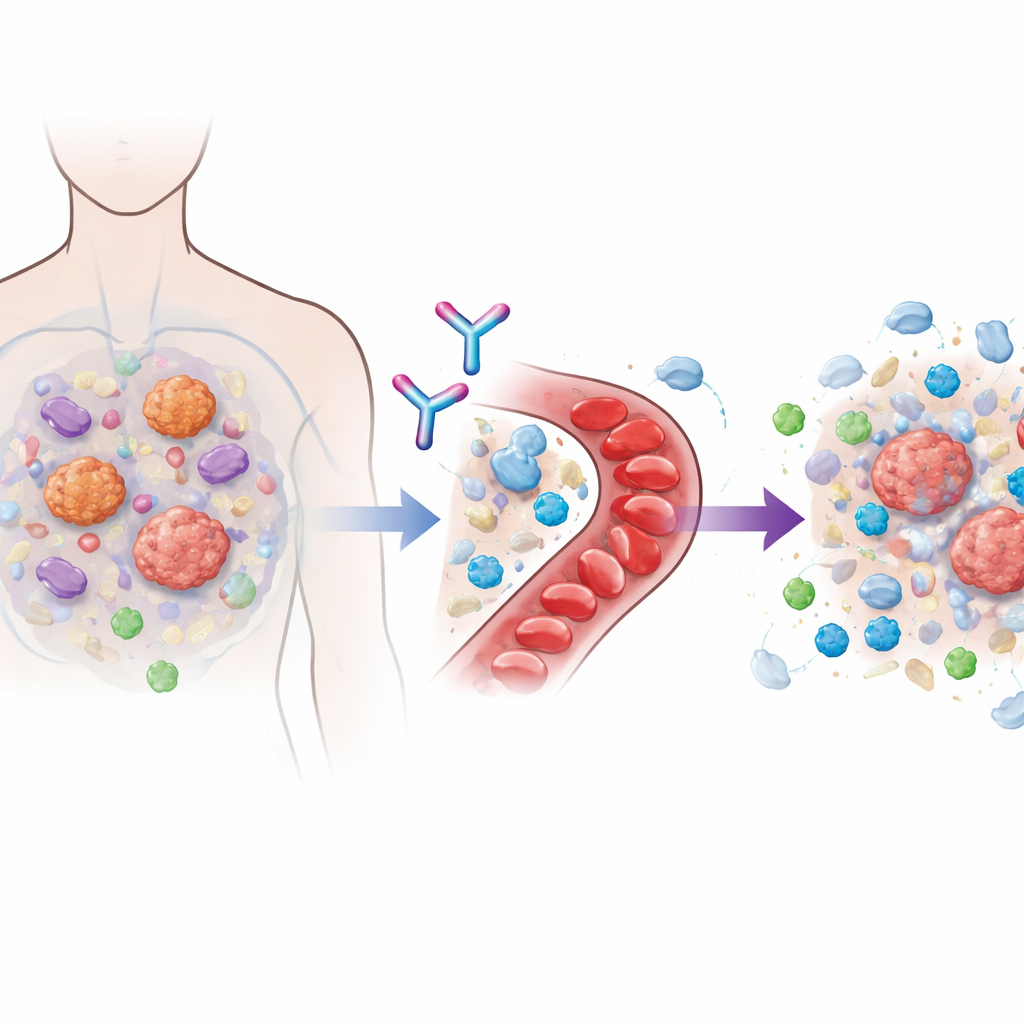
慎重に設計された初のヒト試験
DRAGON試験は米国と韓国の22病院で実施された多施設第1相試験です。治療選択肢が限られた進行固形腫瘍の成人112人が登録されました。研究の第1部では、リナボンキバートを少人数の患者群に単独で漸増投与するか、既往のPD‑1ベース治療と併用して投与しました。この段階的アプローチにより、安全性、薬物の血中動態および持続性を評価し、より広範な試験のための投与量を選定しました。第2部では、少なくとも1コースのPD‑1免疫療法に既に抵抗を示していた78人が、一定投与量のリナボンキバートとペムブロリズマブの併用を受けました。これらの患者は治療困難ながん(透明細胞腎がん、メラノーマ、頭頸部がん、尿路(膀胱)がん、肺がんなど)を抱え、ほとんどが複数の前治療を受けていました。
まず安全性:患者に何が起きたか
この早期試験の主目的は安全性であり、リナボンキバートはその点で期待が持てる結果を示しました。すべての用量レベルで最大許容用量には達せず、薬剤に関連する用量制限性あるいは致命的な有害事象は認められませんでした。第2相用量でリナボンキバートをペムブロリズマブと併用した場合、約4分の3の患者が治療関連の副作用を経験し、これは単独の免疫療法でしばしば観察されるものと同様の頻度でした。発疹やかゆみが最も多い追加的な問題であり、ごく少数の患者により重篤な皮膚や肺の炎症が生じました。重要な点として、一部の抗体療法で見られる危険な免疫過反応であるサイトカイン放出症候群は観察されず、全体としての安全性プロファイルは主にペムブロリズマブ単独のそれに類似していました。
免疫系を再び目覚めさせる兆候
これは大規模な決定的効果判定試験ではありませんでしたが、TGFβ1を遮断することでPD‑1阻害への反応を再燃させ得ることを示す複数の兆候がありました。拡大試験では、リナボンキバートとペムブロリズマブの併用療法は、以前にPD‑1薬の利益を失っていた患者群の目に見える腫瘍を有意な割合で縮小させました。確定的反応率は透明細胞腎がんで20%、メラノーマで18.2%、頭頸部および尿路がんでそれぞれ9%強で、腎がん患者の1例は可視病変が完全に消失しました。これらの反応の多くは数か月にわたり持続し、反応した患者は一般に以前のPD‑1療法よりも併用療法を長期間継続しました。治療前後の生検は生物学的な説明を示しました:腫瘍にはCD8“キラー”T細胞の浸潤が増加し、活性化T細胞が多く、抑制的な制御性T細胞や骨髄系細胞が減少し、全体としてより炎症性で攻撃準備が整った微小環境へと変化していました。
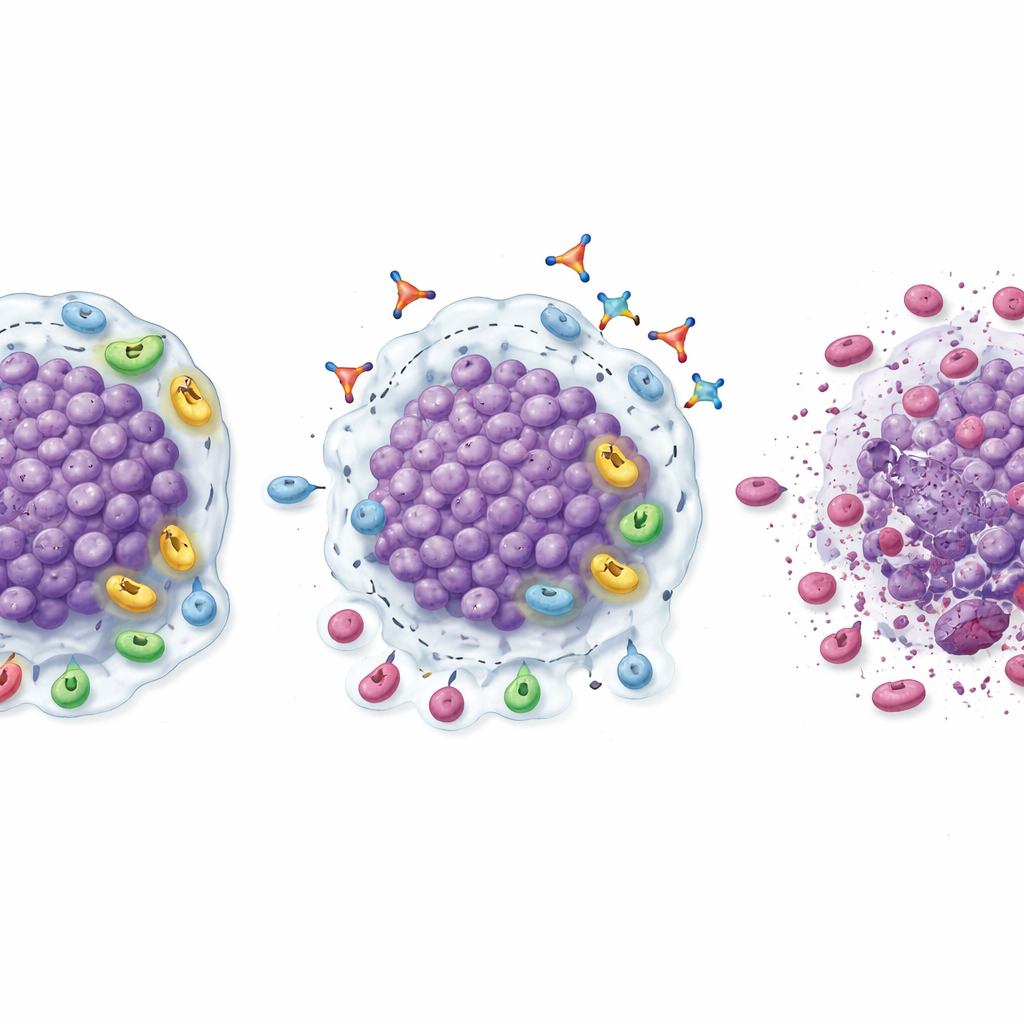
誰が最も恩恵を受けるかを探る
研究者らはどの患者が特に反応しやすいかも探りました。透明細胞腎がんでは、ベースラインで多くのCD8 T細胞を含んでいるものの、同時に制御性T細胞が豊富でTGFβ1発現が高い腫瘍は、併用療法で縮小しやすい傾向がありました。これらの患者では反応率と無増悪生存期間が腎がん全体群よりもかなり高かったのです。このパターンは「甘いスポット」を示唆します:免疫の兵士が多数存在するもののTGFβ1駆動の抑制で抑えられている腫瘍は、リナボンキバートとPD‑1阻害の組み合わせに最適な候補になり得ます。これがより大規模な研究で検証されれば、これらのマーカーを簡便な組織検査で検出することで、恩恵を受けやすい患者を選択できる可能性があります。
今後この成果が意味すること
免疫療法に既に抵抗を示した進行がんと向き合う人々にとって、自身の免疫系を激化させながら重篤な毒性を増やさないという展望は非常に魅力的です。この初のヒト試験は、リナボンキバートでTGFβ1の盾を選択的に無効化することが安全に行え、PD‑1阻害剤と組み合わせることで特に一部の腎がんにおいて有意な腫瘍制御を回復させ得る初期証拠を提供します。試験は小規模で無作為化ではありませんが、安全性の記録、生物学的所見、持続する反応はともにより大規模な第2相試験を支持する強い根拠を築いています。将来の研究でこれらの所見が確認されれば、このアプローチは免疫療法の恩恵を受けられる患者の範囲を広げ、現在は手強いとされる一部のがんを再び自己の免疫によって制御可能にするかもしれません。
引用: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
キーワード: がん免疫療法, TGFβ1阻害, 免疫チェックポイント抵抗性, 透明細胞腎細胞がん, 腫瘍微小環境