Clear Sky Science · ja
循環免疫細胞の解釈可能な炎症ランドスケープ
なぜ血中の炎症があなたにとって重要なのか
炎症は関節炎や喘息からCOVID-19やがんに至るまで多くの病気の核心にあります。それでも医師は、体の炎症シグナルを読み取り、何がうまくいっていないのか、どの治療が最適かを明確に説明するのに苦労しています。本研究は、血流中を循環する免疫細胞の巨大な「地図」を構築し、これらの細胞が広範な炎症性疾患を分類するための、簡便に採取できる生体バイオマーカーとして機能し得ることを示しています。
免疫細胞の巨大地図を作る
このランドスケープを描くため、研究者らは1,047人から採取した650万を超える免疫細胞を解析しました。参加者は、ループスやリウマチなどの自己免疫疾患、喘息やCOPDなどの慢性肺疾患、COVID-19やHIVなどの感染症、いくつかのがん、そして健常ドナーを含む19の状態に及びます。単一細胞RNAシーケンシングを用いて各細胞でどの遺伝子がオンになっているかを測定し、研究間の技術的差異を補正する高度な統計手法で解析した上で、細胞を64の異なる免疫細胞状態に分類しました。この「炎症アトラス」は、T細胞、B細胞、単球などの既知の主要メンバーに加え、疾患に応じて移動するより専門化したサブタイプも捉えています。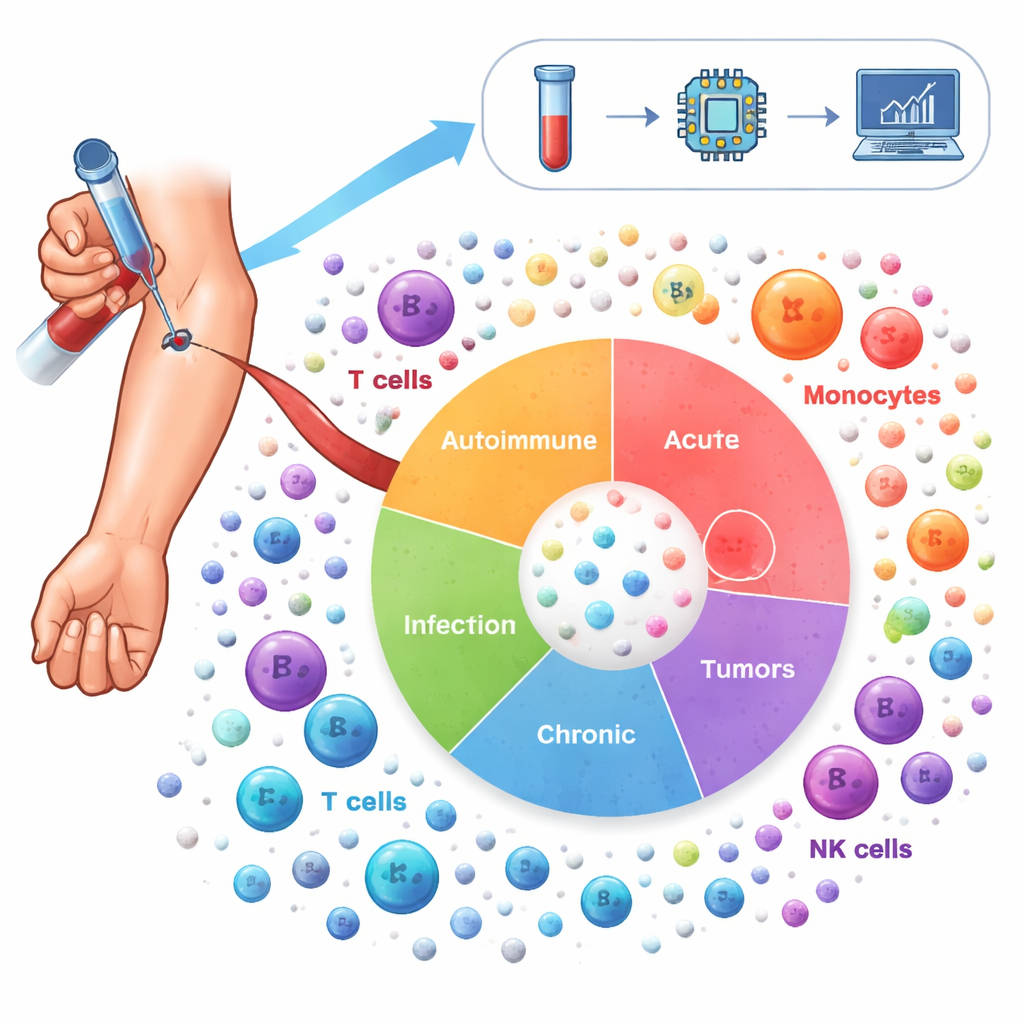
体の炎症シグネチャを読む
次にチームは、免疫細胞がどのように活性化され、体内を移動し、抗原を提示し、インターフェロンや腫瘍壊死因子のようなシグナル分子に応答するかを制御する遺伝子に注目しました。これらの遺伝子を21の生物学的「シグネチャ」にまとめ、主要な細胞型ごとに洗練しました。患者と健常ドナーを比較することで、異なる疾患でどのシグネチャが上方あるいは下方に調節されているかを可視化できました。例えば、多くの免疫介在性炎症性疾患では接着分子や抗原提示機構の活性が強まる一方、インターフェロン応答は多くの細胞型で抑制されていましたが、特定のCD8 T細胞では亢進していました。インフルエンザやCOVID-19のようなウイルス感染はインターフェロン誘導プログラムを強化し、HIVやB型肝炎のような慢性感染はそれを弱めました。
重要な遺伝子と制御スイッチにズームイン
広範なシグネチャでは重要な詳細が隠れてしまうため、研究者らは個々の遺伝子とその調節因子まで掘り下げました。非ナイーブCD8 T細胞では、FGFBP2とGZMBの2遺伝子が特定のエフェクターメモリーサブタイプで特に活性化しており、潰瘍性大腸炎で顕著でした。これらの遺伝子は上皮面での損傷と関連しており、血中で強いシグナルが観察されることは、これらの攻撃的な細胞が組織に入る前から既に活性化されている可能性を示唆します。遺伝子制御ネットワークの別解析では、STAT1とSP1という二つの転写因子がインターフェロン誘導プログラムの中心的制御因子として浮かび上がりました。これらの活性パターンは疾患や細胞型で異なり、例えばループスでは単球とCD8 T細胞で逆の挙動を示したり、フレア期と非フレア期で変化したりしており、同じ経路がある文脈では保護的で別の文脈では有害になり得ることを示唆しています。
血中細胞から病気を見分ける機械を訓練する
このアトラスを実用的なツールにするため、チームは解釈可能な機械学習を適用しました。各主要細胞型ごとに勾配ブースティング決定木モデルを個別に訓練し、細胞の遺伝子発現から各細胞に正しい疾患ラベルを付与するようにアルゴリズムに学習させました。これらのモデルは、技術的差異を補正した後に特に、ホールドアウトサンプルで高い精度を示しました。SHAPという、どの遺伝子が各決定を駆動しているかを説明する手法を用いることで、候補となるバイオマーカーを同定できました。例えば単球におけるCYBAは、乾癬などの皮膚疾患をクローン病や潰瘍性大腸炎などの腸の炎症から区別するのに役立ちました。また、特定のT細胞や自然リンパ系細胞におけるIFITM1は、喘息とCOPDを分け、慢性的な抗ウイルス防御の異なるパターンを示唆しました。
血液ベースの診断コンパスに向けて
最後に著者らは、個々の細胞だけでなく患者全体を循環免疫プロファイルから分類できるかを検討しました。各細胞のデータを圧縮された「埋め込み」空間に投影し、患者ごとに細胞型ごとの埋め込みを平均化して、疾患を予測する分類器を訓練しました。新しい患者が訓練データの患者と類似している場合、性能は非常に良好でした。しかし、完全に独立した研究から得られ、異なる実験手法で処理されたサンプルでは精度が大きく低下し、この種のツールが技術的変動に非常に敏感であることが明らかになりました。1施設で単一のシーケンシング化学法を用いて生成されたより統制された「集中型」データセットは、多くの性能を回復させ、標準化されたプロトコルや非常に大規模で多様な訓練セットの必要性を示しています。
今後の診断と治療にとっての意義
一般向けの要点は、あなたの循環する免疫細胞が体の炎症の豊かなフィンガープリントを運んでいる、ということです。これらのフィンガープリントを細胞ごとに読み取ることで、本研究は多くの疾患を区別し、特定の症状を引き起こす可能性のある遺伝子を発見し、炎症性疾患を分類する汎用的な血液検査の構築を始められることを示しています。本研究はまだ臨床で即使用できる検査ではありません—研究間の技術的差異が信頼性を制限しています—が、簡単な採血で正しい診断と治療をより早く特定するのに役立つ将来の“リキッドバイオプシー”ツールの基盤を築いています。
引用: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
キーワード: 炎症, 免疫細胞, 単一細胞RNAシーケンシング, バイオマーカー, 機械学習