Clear Sky Science · ja
CD38は局所の抗原特異的制御性T細胞にストレス耐性を付与し、区画化された中枢神経系炎症を抑制する
脳を守る免疫細胞が重要な理由
多発性硬化症のような多くの自己免疫性の脳疾患は、くすぶる火のように振る舞います:最初の炎症の激しい波は静まるものの、数年後に再燃して損傷が進行することがあります。本研究は一見単純だが重要な問いを投げかけます:中枢神経系(CNS)での発作の後、平和を保っているのは何か、そして何が病態を再び悪化させるのか?著者らは、炎症後に脳や脊髄に定着する少数派の免疫細胞である制御性T細胞に着目し、苛酷な環境で生存し再発を防ぐために、単一の表面分子がどのようにそれらに能力を与えるかを解き明かします。
残留する免疫の平和維持者
研究者たちは、多発性硬化症の一側面を模したマウスモデルを用い、病勢がピークに達しその後回復期に入る際のさまざまなT細胞の挙動を追跡しました。症状が改善するにつれて炎症を駆動する通常のヘルパーT細胞の数は減少した一方で、免疫応答を抑える専門の制御性T細胞はCNS内に残りました。局所T細胞プールに占める彼らの相対的割合はむしろ増加し、脳脊髄液の空間や脳を覆う保護膜の周囲といった特定のニッチに集積していました。外から侵入するT細胞の由来を標識することで、回復後にはリンパ節から新たに来る制御性T細胞はごくわずかであることが示されました。むしろCNS内の集団は主に局所で維持されており、長期的に定着する“平和維持”部隊の存在を示唆します。 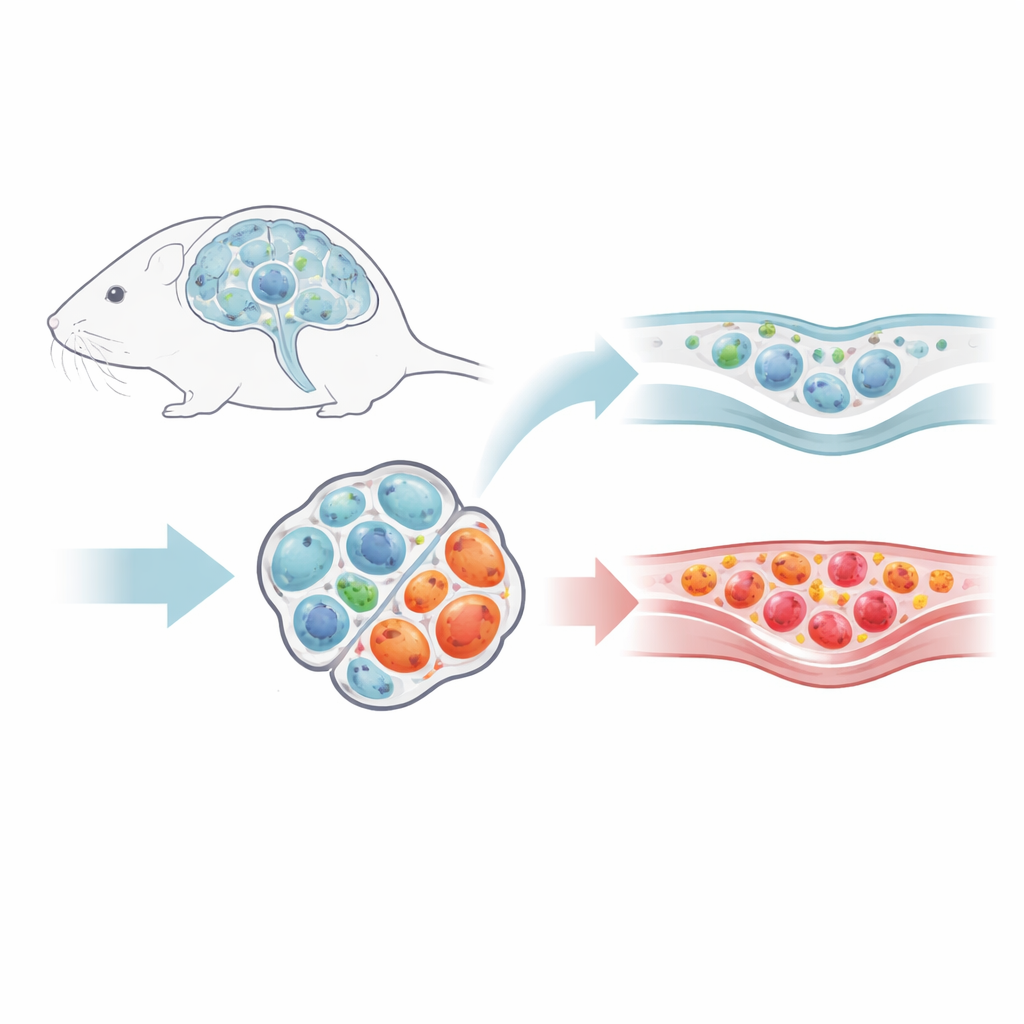
敵対的なニッチに耐える守護者たち
炎症後のCNSは、これら守護者にとって決して快適とは言えません。主要な病勢の波の後、制御性T細胞が強く依存する増殖シグナルであるインターロイキン-2(IL-2)のレベルは、通常のT細胞の多くが後退するため低下します。同時に組織には代謝分子NAD+が豊富に存在し、特定の酵素により修飾されると細胞死を誘発したり重要な表面受容体を鈍化させたりします。個々の制御性T細胞を遺伝的にタグ付けして追跡することで、著者らは同一性を保つ「安定」細胞と、特徴的なFoxp3プログラムを失う「不安定」細胞を区別しました。安定な細胞はIL-2シグナルの署名がはるかに強く、IL-2受容体の発現も高く、希少なIL-2を感知する能力がこのストレスの多い環境で生き残るために重要であることを示唆しました。
脳内から再発を局所制御する
これらの定着制御性T細胞が長期の病勢制御に本当に重要かを検証するため、研究者らは毒素を脳脊髄液へ直接投与してCNS内のそれらのみを選択的に除去し、体内の大多数の全身性制御性T細胞はほぼ温存しました。数日以内に回復していたマウスは重度の再発を起こし麻痺が再燃しました。対照的に、体内だけの制御性T細胞を枯渇させてCNS内のものを残した場合は再燃を誘発しませんでした。再発では、血液からの新規動員が阻止されていても、すでにCNS内に滞留していた効果器T細胞が急速に再活性化・増殖しました。これは、循環する制御性T細胞ではなく局所の制御性T細胞が、急性の攻撃が過ぎ去った後に残存する攻撃的細胞を抑えるうえで不可欠であることを示しています。
一つの酵素が制御細胞をどう守るか
さらに掘り下げると、著者らはストレス耐性のあるCNS内制御性T細胞を特徴づける分子を探しました。重要な因子として浮かび上がったのがCD38という細胞表面の酵素で、細胞外のNAD+を分解します。炎症を起こしたCNSでは、制御性T細胞は強くCD38を増加させる一方で、通常のT細胞ではそのような顕著な変化は認められませんでした。CD38を欠く髄鞘反応性制御性T細胞をマウスに移入すると、これらの細胞はCNSに到達するものの、正常な対照群と異なり病勢を抑えられませんでした。混合キメラ動物では、定着した制御性T細胞だけがCD38欠損である状況において、CD38を持つ分画を除去するだけで再発が誘発され、CD38が細胞内因性に作用して効果的な制御を可能にしていることが示されました。
生命線シグナルを守る
機構的な実験は、CD38がこの耐性をどのように付与するかを明らかにしました。CNSでの高いNAD+濃度は酵素ARTC2.2による表面タンパク質の化学修飾を促進します。敏感な標的の一つはIL-2受容体の高親和性サブユニットで、制御性T細胞は特に脳抗原を認識するときにこのサブユニットを非常に高レベルで発現します。NAD+に曝露されたCD38欠損制御性T細胞では、ほとんどのIL-2受容体が修飾され、下流の伝達分子STAT5の活性化が弱まりIL-2への応答性が低下しました。対照的に、CD38を発現する細胞は局所で周囲のNAD+を低下させ、この有害な修飾を抑えて強力なIL-2シグナルを保持していました。生体内でNAD+を脳に注入すると、この経路を介して大部分の制御性T細胞が選択的に死滅し、通常のT細胞は残存するという結果が得られ、保護酵素がなければニッチがいかに脆弱かを裏付けました。 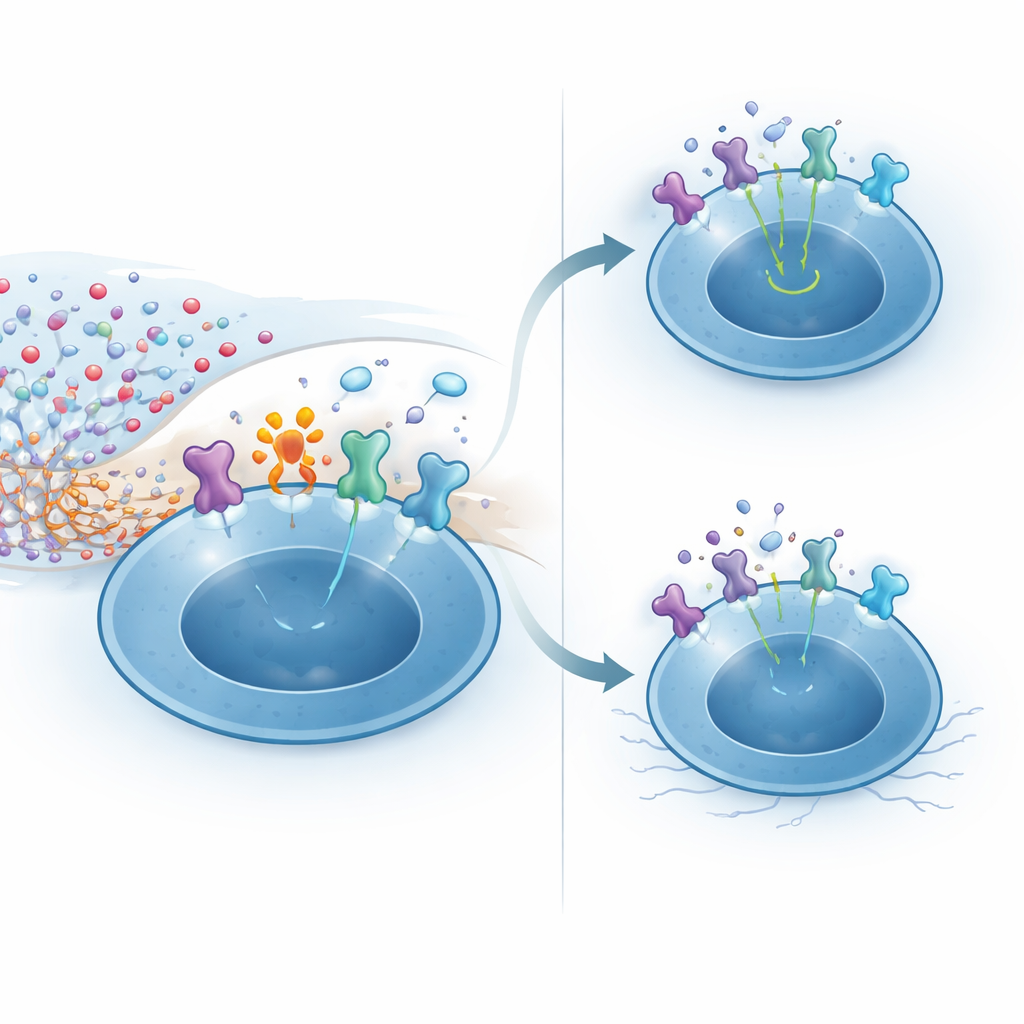
慢性の脳自己免疫にとっての意味
本研究は、慢性のCNS自己免疫を区画化された戦いとして描きます:残存する攻撃的T細胞の小さなクラスターが脳や脊髄に潜み、同等に特化した局所の制御性T細胞によって抑えられています。これらの守護者はCD38により高いNAD+環境でも生き残り、微量のIL-2を感知し続けることで「ストレス耐性」を獲得し、自己の同一性と抑制機能を維持します。一般向けの要点としては、多発性硬化症のような疾患の長期制御は、循環する免疫系よりも脳内に定着したこれらの平和維持細胞を育て守ること、すなわち制御性T細胞におけるCD38機能やIL-2感受性を高める経路を標的にする可能性に依存しているかもしれない、ということです。
引用: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
キーワード: 制御性T細胞, 多発性硬化症, 中枢神経系の炎症, CD38酵素, 免疫寛容