Clear Sky Science · ja
ヘパラン硫酸と複合体を形成するグリコRNAはVEGF‑Aシグナル伝達を調節する
細胞が体内の血管シグナルを精密に調整する仕組み
血管は成長シグナルが出現する場所にただ無差別に出現するわけではなく、腫瘍を助長したり失明を引き起こしたりしないように厳密に制御される必要があります。本論文は、主要な血管成長シグナルであるVEGF‑Aに対する予期せぬ「ブレーキ」を明らかにします。著者らは、糖やタンパク質と結合して細胞外面に飾られた小さなRNA断片がVEGF‑Aのメッセージを弱めることを示し、細胞表面で使われる言語に対する考え方を変えます。
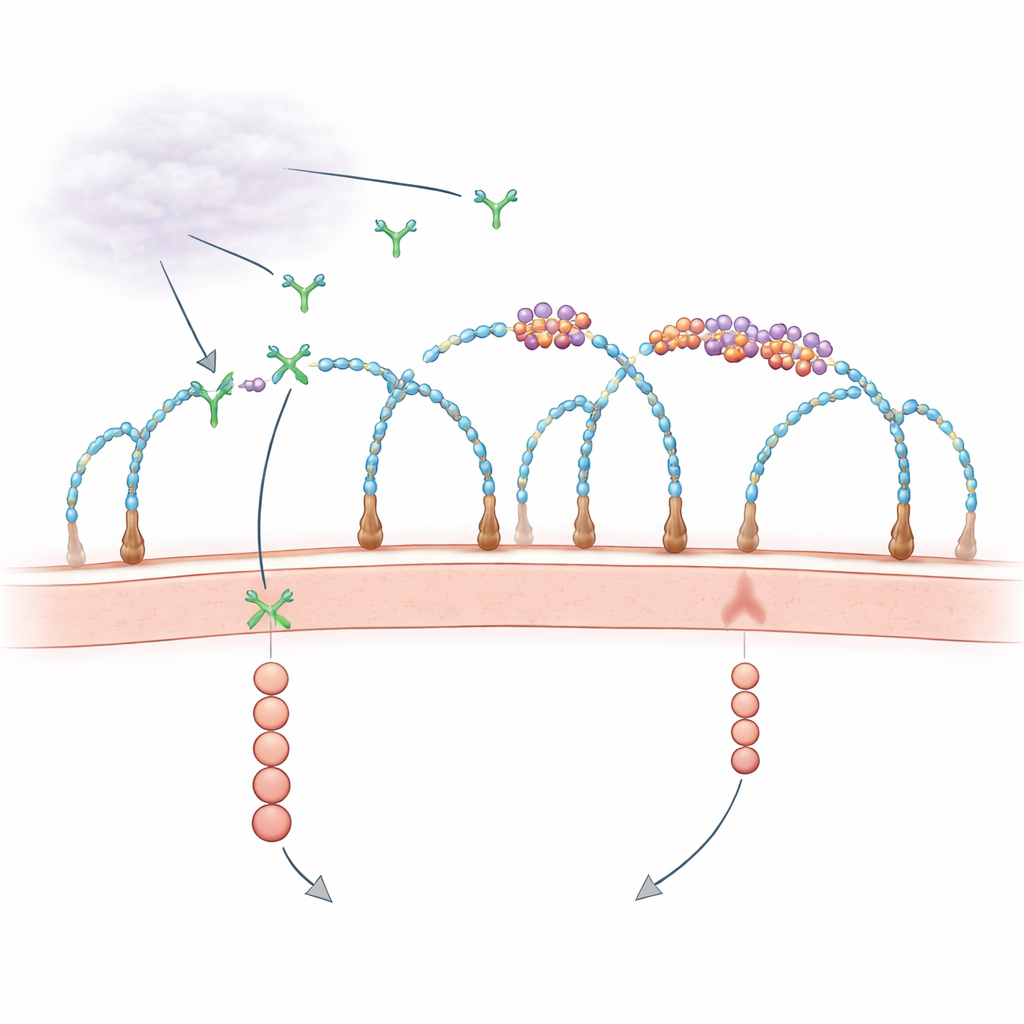
細胞表面に存在するRNAの驚くべき役割
何十年にもわたり、生物学者はヘパラン硫酸プロテオグリカンと呼ばれる糖修飾タンパク質に富む細胞の外被が成長因子を捕らえて受容体に提示するのを助けることを知っていました。一方で、細胞外のRNA断片が血管成長に影響を与えるかもしれないという断片的な観察もありましたが、関与する分子や機構は不明でした。最近の研究で、一部の小さなRNAが複雑な糖と化学的に結合して「グリコRNA」を形成し、特定のRNA結合タンパク質が細胞表面にも現れてこれらのRNAと共に集積することが明らかになりました。本研究は、膜上に存在するこれらの小さなRNA–タンパク質の島が実際にVEGF‑Aのような成長シグナルの受け取り方を制御しているのかを問い直します。
糖鎖でRNA–タンパク質のクラスターを作る
著者らはゲノムワイドのCRISPRノックアウトスクリーニングと高解像度顕微鏡を用いて、特定の硫酸化修飾を持つヘパラン硫酸が、彼らが細胞表面リボ核タンパク質(csRNPs)と呼ぶこれらのRNA–タンパク質クラスターを組み立てるための不可欠な足場であることを発見しました。ヘパラン硫酸を構築または硫酸化する主要な酵素を取り除くと、RNAおよびタンパク質自体は細胞内に存在していても、細胞表面上のグリコRNAとその相方タンパク質のクラスターは消失しました。表面からヘパラン硫酸鎖を切り取る酵素や硫酸化を化学的に阻害する処置も同様の効果を示しました。これらの結果は、完全で適切に硫酸化されたヘパラン硫酸鎖がcsRNPを膜上のナノスケールの島として組織化することを示しています。
RNAクラスターは強力な血管成長シグナルのブレーキとして働く
研究チームは次に血管を内張りしVEGF‑Aに応答するヒトの内皮細胞を調べました。これらの細胞にもヘパラン硫酸に固定されたcsRNPクラスターが存在することが分かりました。生細胞をRNA分解酵素(RNase)で処理すると、糖鎖はそのままにRNA成分だけが除去されました。その条件下で、VEGF‑Aの最も一般的でヘパラン結合性のあるアイソフォーム(VEGF‑A165)は下流のERKシグナル経路を格段に強く活性化しましたが、ヘパラン結合尾部を欠く短いアイソフォーム(VEGF‑A121)には影響がありませんでした。RNA除去後により多くのVEGF‑A165分子が細胞表面に結合したにもかかわらず、受容体の発現量は変わりませんでした。3Dマイクロフルイディクス装置内では、RNaseに曝露された内皮細胞がコラーゲンゲル内へより深く伸び、管状構造をより強固に形成し、表面RNAを破壊することで血管新生促進的な挙動が解き放たれることを示しました。
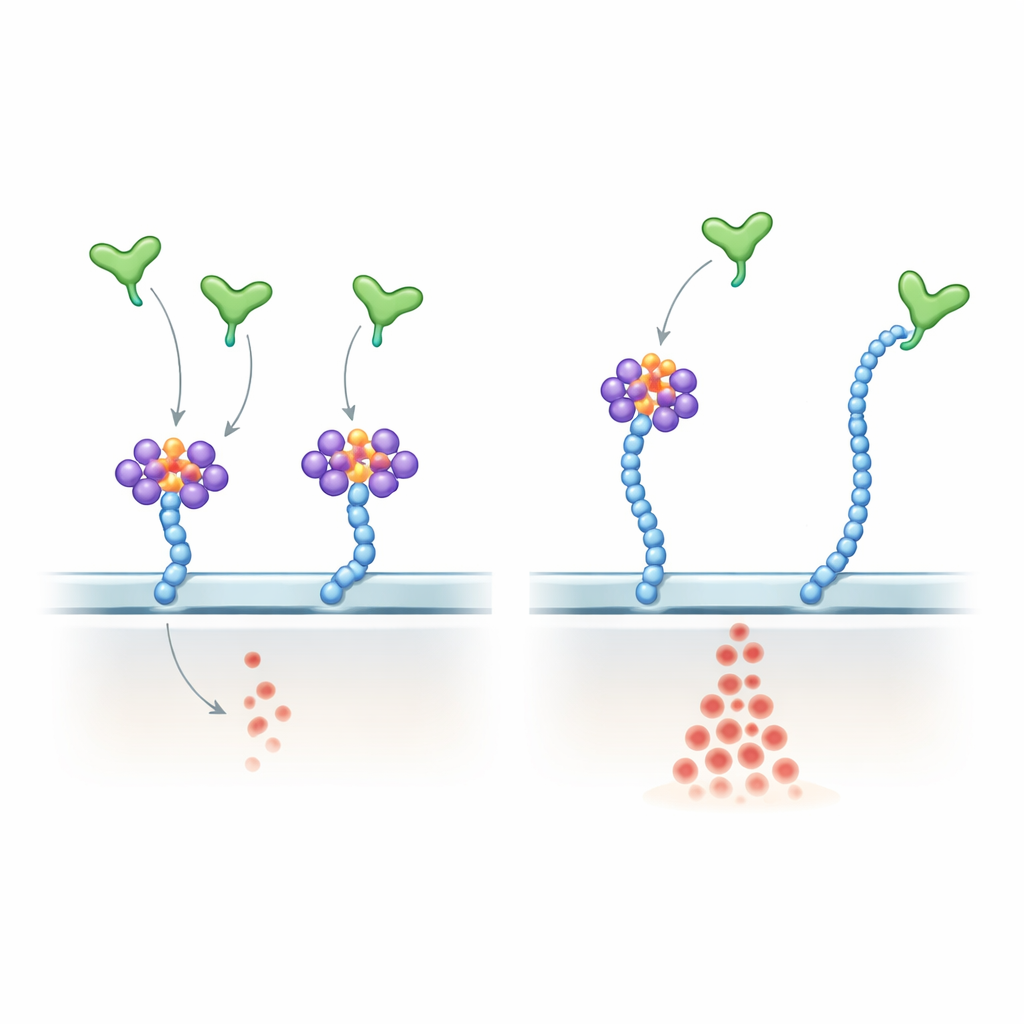
VEGF‑AがRNAと糖をどのように感知するかの解剖
機構を探るために、著者らはVEGF‑A165がその正に帯電したC末端領域を介して多くの既知のグリコRNAを含む選択的な小分子RNAに直接結合することを示しました。この領域はヘパラン硫酸に結合する同じ領域です。著者らはこの尾部の主要なアルギニン残基をリシンに置換した微妙な変異体VEGF‑A165を設計しました。この変異体は全体的な正電荷を維持しヘパラン硫酸鎖には依然として結合しましたが、グリコRNAへの結合は乏しく、RNase処理に対してほとんど感受性を失いました。内皮細胞では、この変異体は通常のVEGF‑A165よりも強く、かつRNase耐性の高いERK活性化を引き起こし、細胞表面のRNAを除去した場合に近い効果を示しました。生きたマウスに変異体を眼内注入すると、通常のタンパク質よりも網膜血管成長がより旺盛に誘導されました。ゼブラフィッシュ胚では、変異型Vegfaを過剰発現させると正常な血管パターンが乱れ、内皮細胞数が増加しました。
基礎機構から広範な示唆へ
最後に、著者らはVEGF‑Aのヘパラン結合尾部を無関係のシグナル蛋白Wnt3aに融合させることでWnt活性を方向付けられることを示しました。正常な尾部を付加するとWnt駆動の発生変化が減少し、RNAに不感な尾部を付けるとそれらが増強されました。これらの実験は、特異的に硫酸化されたヘパラン硫酸に支えられたcsRNPクラスターがVEGF‑Aや関連因子を結びつけてその活性を抑えるというモデルを支持します。RNA成分が除去されるか成長因子がRNAを感知する能力を失うと、複数種でシグナルが強まり血管発生が変化する方向に均衡が傾きます。
健康と将来の治療への意義
専門外の読者にとっての主要メッセージは、細胞がタンパク質や糖だけでなく、表面に提示された小さなRNAも用いてVEGF‑Aのような強力な成長シグナルを精密に調整しているという点です。これらの糖に固定されたRNA–タンパク質クラスターは血管形成に対する調節可能なブレーキとして機能し、新しい血管が必要な場所と時期に芽生えることを助けます。この均衡を崩すこと—表面RNAを分解したり、成長因子のRNA結合特性を変えたりすること—は血管成長を過度に促進または誤誘導する可能性があります。この新たに明らかになった制御層を理解することは、表面RNA、その糖足場、あるいは成長因子のRNA感知領域を標的にして、がん、眼疾患、創傷治癒、再生医療における血管新生をより精密に調節する治療法の扉を開くかもしれません。
引用: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
キーワード: 血管新生, 血管内皮増殖因子, ヘパラン硫酸, 細胞表面RNA, グリコRNA