Clear Sky Science · ja
ポリアミン依存の代謝シールドが選択的スプライシングを制御する
小さな分子が細胞の遺伝情報の読み方を助ける仕組み
すべての細胞の中で、同じDNAの台本は多様な読み方が可能であり、限られた遺伝子数から膨大な種類のタンパク質が生み出されます。この柔軟性は、RNAをタンパク質に翻訳する前に編集する「選択的スプライシング」と呼ばれる過程に依存します。本論文は、ポリアミンと呼ばれる小さく正に帯電した分子が、この編集段階をひそかに方向付ける――細胞がどのRNAバージョンを作るかを決める保護的なシールドのように働く――ことを明らかにしました。選択的スプライシングはがん、脳機能、幹細胞で重要なため、この制御の隠れた層を発見したことは健康と病気に広範な影響をもたらします。
すべての細胞にある小さな帯電ヘルパー
ポリアミンは複数の正電荷をもつ小さく柔軟な分子で、細胞は基本的な栄養素からこれらを合成します。特に増殖の速い細胞、例えば腫瘍では成長や生存を支える因子として古くから知られてきました。著者らは、ポリアミンが燃料だけでなくシグナルとしても働くかを問いました。前立腺がん細胞とマウスでポリアミン合成を部分的に阻害し、時間に沿ってタンパク質やRNAの変化を計測しました。その結果、総ポリアミン量が劇的に低下するずっと前に、タンパク質のリン酸化(スイッチを入れたり切ったりする化学タグ)に強い変化の波が生じ、特にスプライソームなどRNA編集機構の構成要素で顕著でした。
細胞のRNA編集装置の配線替え
RNAに着目して、チームは深いシーケンシングを用い、ポリアミン合成が阻害されたときの選択的スプライシングを追跡しました。がん細胞株、正常な細胞種、マウス組織において何百ものRNA領域がスキップされたり取り込まれたりといった変化が起きました。これらの変化は、単に細胞分裂が遅くなった副産物でも、あるいはヒプシネーションと呼ばれる既知のポリアミン依存プロセスの結果でもありませんでした。代わりに、研究者が外部からポリアミンを補給すると多くのスプライシング変化が正常方向へ戻りました。薬剤と遺伝学的手法の双方でポリアミンを低下させると同様のスプライシングパターンが観察され、薬剤併用でさらにポリアミンを低下させると変化が強まり、効果がポリアミン供給に密接に結びついていることが確認されました。
隠れた標的:SF3スプライシングモジュール
ポリアミンがスプライシング機構のどこで働くかを特定するため、著者らはポリアミン低下によるスプライシング署名を、300以上の既知のスプライシング因子を個別にサイレンシングして作られた大規模な参照マップと比較しました。最も近い一致は、RNA中の重要なシグナルを認識するのを助けるスプライソームの特定部分、SF3サブコンプレックスを指しました。公開されているタンパク質–RNA結合データの計算解析もこの関連を支持しました:ポリアミン欠乏でスプライシングが変化したRNAは、特にSF3タンパク質に結合されやすい傾向がありました。チームがSF3成分を遺伝学的にあるいは薬剤で部分的に無効化すると、ポリアミン枯渇によるスプライシング効果はほとんど消失し、SF3の正常な活性がこの新たな制御経路に不可欠であることが示されました。 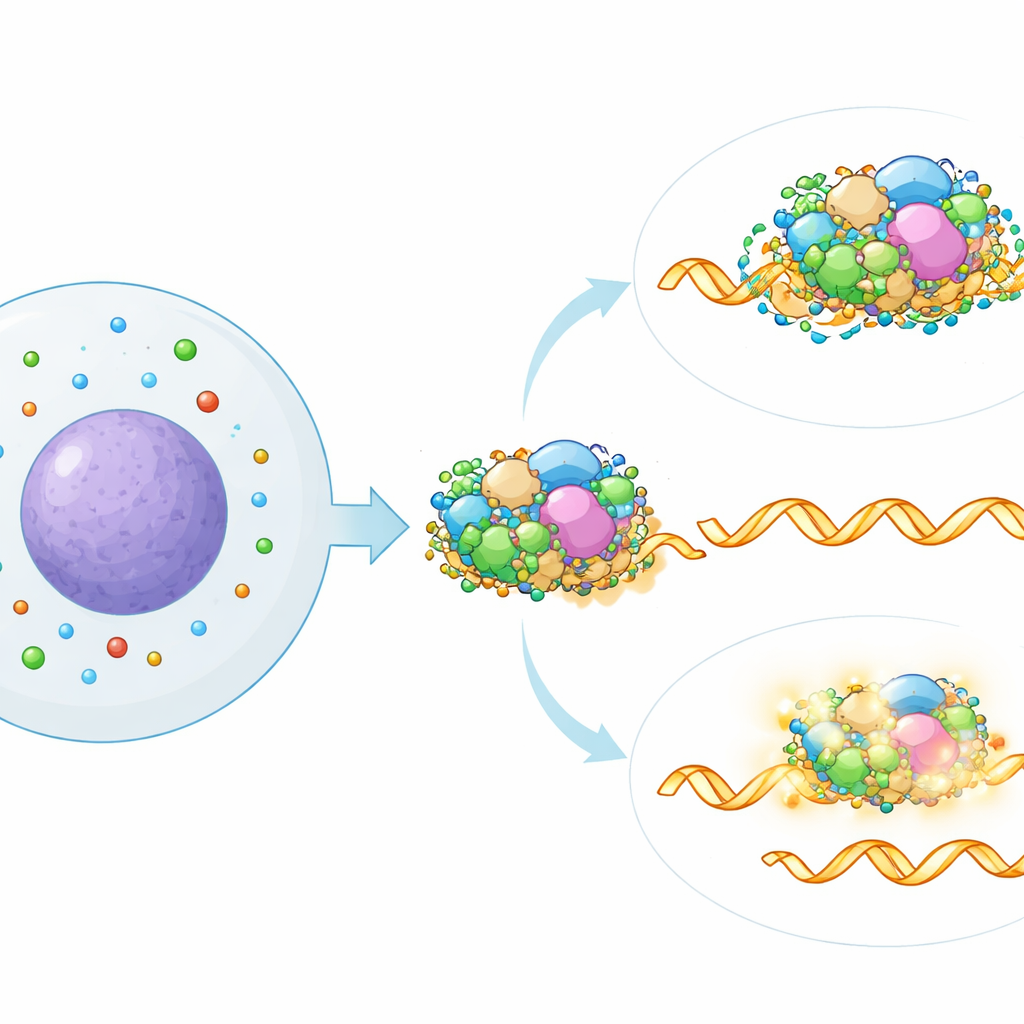
代謝シールド:ポリアミンがタンパク質のタグ付けを阻む仕組み
さらに掘り下げると、SF3タンパク質で最も強く影響を受けたリン酸化部位は、負に帯電したアミノ酸が豊富な短い領域に集中していることが分かりました。分子モデリングと核磁気共鳴の実験は、ポリアミンがこれらの酸性パッチに入り込み、複数の静電相互作用を形成し、通常リン酸が付く近傍のセリン残基を部分的に覆うことを示しました。この物理的な「抱擁」は、リン酸を付加するキナーゼ(酵素)がそれらの部位にアクセスすることを難しくします。試験管内実験では、ポリアミンの添加がCK1というキナーゼによるSF3タンパク質のリン酸化を直接阻害しました。細胞内ではCK1と近縁のCK2を阻害するとポリアミン欠乏によるスプライシング変化が抑えられ、SF3A3タンパク質の三つの主要なリン酸化部位を欠くように遺伝子改変したマウスはポリアミン依存のスプライシング変化にほとんど鈍感になりました。 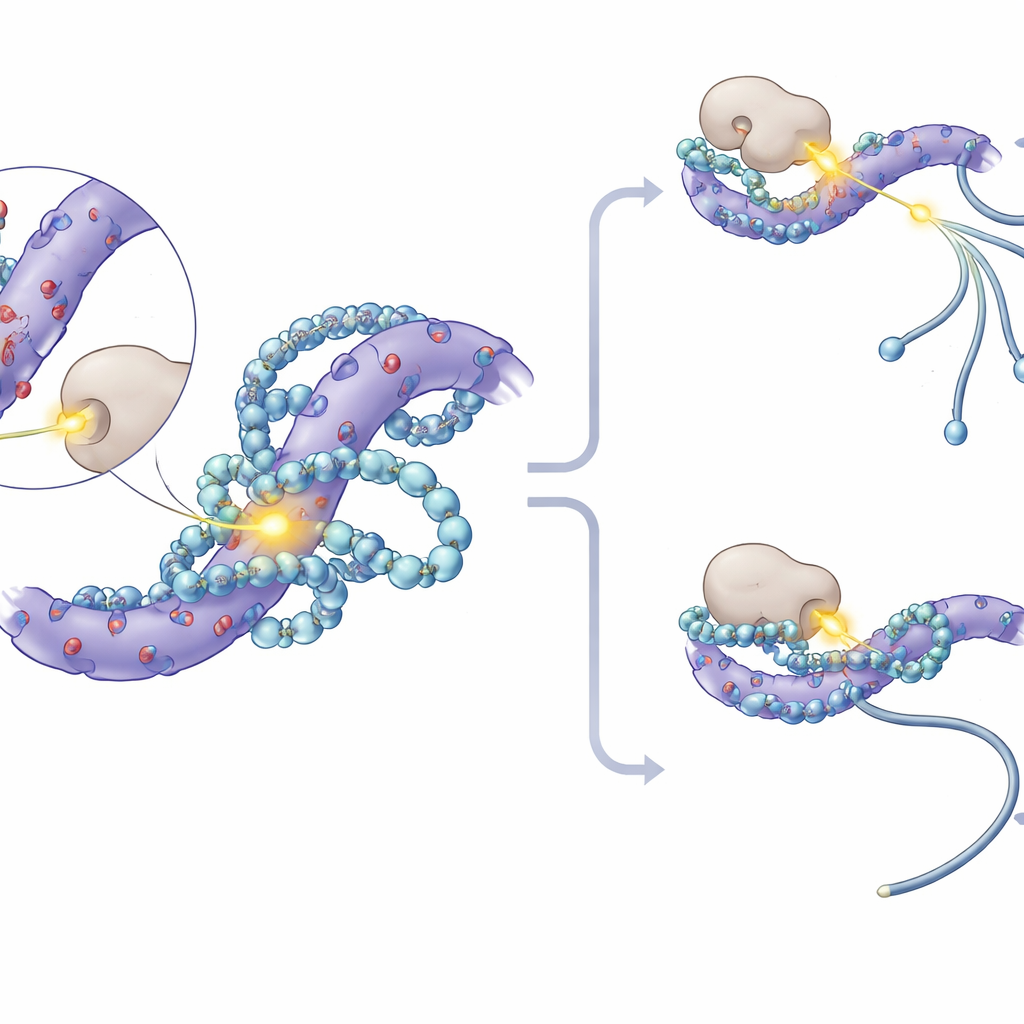
役割を分離するデザイナーモレキュール
研究はまた、BENSpmというポリアミン様薬剤を紹介します。これはより強い正電荷を持ちながら、同時に細胞自身のポリアミン産生を抑える性質を持ちます。BENSpmはSF3の酸性パッチに強く結合してキナーゼ作用を阻害し、天然のポリアミンと同様に働きましたが、実際のポリアミンが不足しているときに細胞増殖を回復させることはできませんでした。これにより、成長や代謝を支える古典的なポリアミンの機能と、新たに定義されたシールド作用を切り分けることができました。マウス胚性幹細胞では、ポリアミンを枯渇させると幹性マーカーNanogが失われる方向に細胞が傾き、スプライシングの景観が変化しました。BENSpmは正常なポリアミン合成が抑えられたままでもスプライシングプロファイルとNanog発現の両方を回復させ、代謝シールドが幹細胞同一性を維持する上で重要であることを示しました。
この発見が重要な理由
平たく言えば、本研究はポリアミンが主要なスプライシングタンパク質の敏感な部位を取り巻く小さな保護手袋として働くことを示しています。手袋がはまっているとキナーゼはそれらの部位を容易に掴んでタグ付けできず、RNA編集は正常に進みます。ポリアミンが低下すると手袋が外れ、リン酸化が急増してスプライシングパターンが変わり、がん細胞や幹細胞に影響を及ぼします。「代謝シールド」というメカニズムを定義し、それを選択的に模倣するツール分子を提示することで、DNA自体を変えずに遺伝情報の読み方を調節する新たな手法への道が開かれ、がんや再生医療におけるスプライシング標的治療の将来の発展を促す可能性があります。
引用: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
キーワード: ポリアミン, 選択的スプライシング, RNA処理, 代謝シグナル, 幹細胞制御