Clear Sky Science · ja
リガンド特異的な活性化経路が細胞内でのGPCRシグナル伝達を決定する
一つの受容体が多様なスイッチのように振る舞う仕組み
現在の多くの医薬品は、Gタンパク質共役受容体(GPCR)と呼ばれる大きな細胞膜上タンパク質群に作用します。これらの受容体は心拍、気分、呼吸など無数の生体機能に影響を与えます。長年、GPCRは単純なオン/オフスイッチとして扱われてきました:薬が結合すればスイッチが入り、細胞内に信号が流れる。しかし本研究は、現実ははるかに複雑であることを示します。受容体に直接組み込んだ新しい種類の蛍光“スパイ”を用いて、生きた細胞内で異なる薬が同じ受容体を別々の活性化経路に導き――都市の異なるルートを選ぶように――異なるシグナルパターンを生み出す様子を観察しました。こうした隠れた経路を理解することで、望ましい効果を与えつつ副作用を避ける薬の設計に役立つ可能性があります。
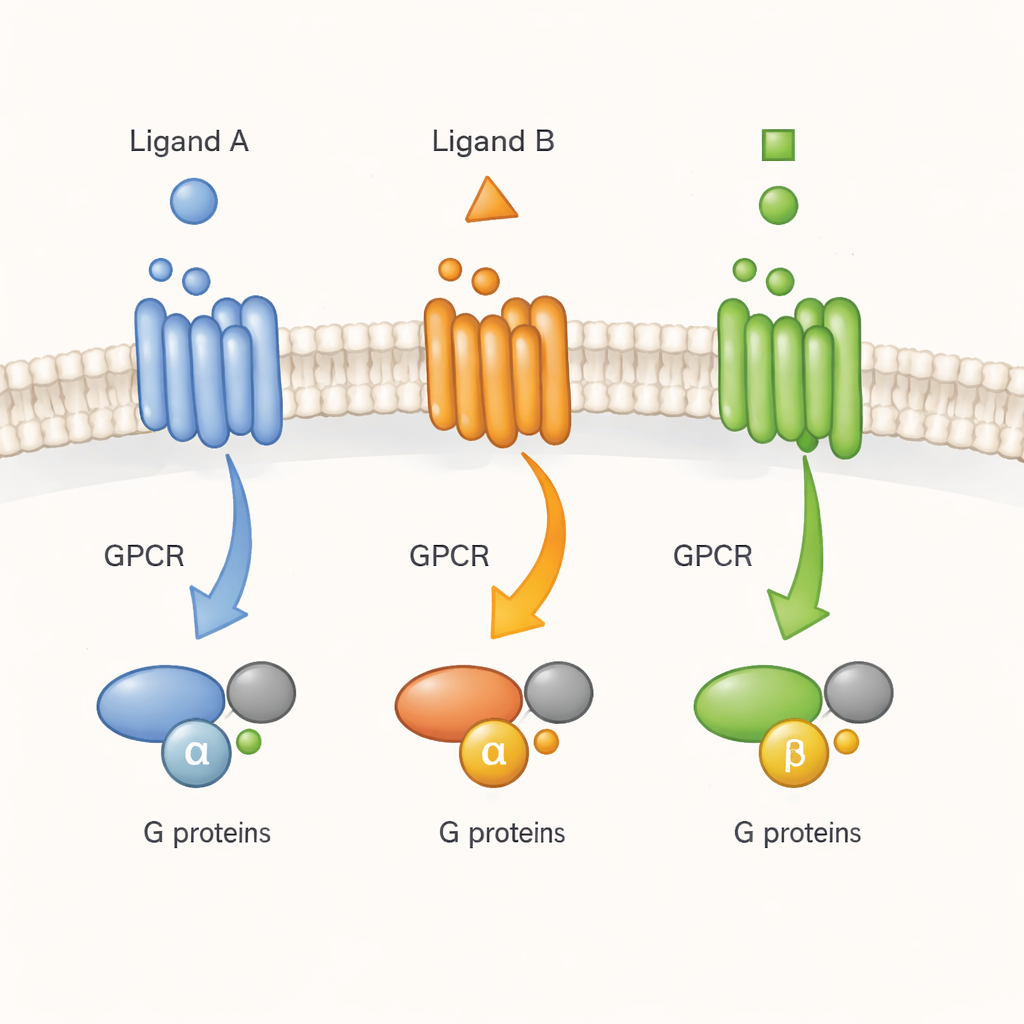
細胞の“ドアベル”をリアルタイムで観察する
GPCRはしばしば分子のドアベルのように表現されます:外側からシグナル分子(リガンド)が鳴らし、受容体が内側のGタンパク質にメッセージを渡します。精製した受容体を界面活性剤中で調べた以前の研究は、GPCRが単に一つの不活性形と一つの活性形の間で切り替わるだけではないことを示唆していました。代わりに多数の形を採り、薬がそれらを異なる程度に安定化するのです。しかし、混み合い動的な生細胞環境でも同じ複雑さが存在するかは不明でした。本研究では、代表的な受容体であるM2ムスカリン性アセチルコリン受容体に着目し、異なるリガンドが実際の細胞シグナル伝達に影響する異なる活性形へと受容体を導くかを問いかけます。M2は心臓や神経活動の重要な調節因子です。
受容体表面に小さな光の報告子を構築する
受容体の動きをその機能を乱さず追跡するために、研究チームは遺伝暗号拡張という技術を用いました。これは受容体の外側表面の特定位置に特殊な設計アミノ酸を挿入できる方法です。この化学的“アンカー”は生細胞内で小さな蛍光色素とクリック反応で結合させられます。72箇所をスキャンし、なお通常の受容体として振る舞う位置のみを残すことで、外ループの異なる部位にそれぞれ一つの色素を持つ7種類のM2受容体バリアントのパネルを作製しました。天然のメッセンジャーであるアセチルコリンを適用すると、これらの部位で色素の明るさが特徴的に上がったり下がったりし、シグナル開始時に受容体外側表面の各部位がどのように変化したかが明らかになりました。重要なのは、これらの標識受容体が依然としてGタンパク質を活性化し、正常な内在化を行えたことで、報告子が破壊的ではなく忠実であったことを示しています。
薬は固有の「立体配座フィンガープリント」を残す
研究者らは次に、いずれもM2受容体を活性化するが強さの異なる幾つかの薬を比較しました:体内のアセチルコリン、非常に強い合成作動薬イペロキソ、そして二つの弱い部分作動薬アレコリンとピロカルピンです。各薬は7つの報告子部位全体で固有の蛍光変化パターン――立体配座フィンガープリントを生み出しました。多くの位置では、動きの大きさは薬が受容体をどれだけ強く活性化するかに対応しました。しかし二つの部位では関係が逆転しており、弱い薬ほど大きな変化を示し、最も強い薬ではほとんど変化が見られませんでした。このような振る舞いは単一の活性状態では説明できません。むしろ、生きた細胞内で同じ受容体がいくつか異なる活性形を取り、強い薬が好む形もあれば弱い薬が好む形もあることを示しています。
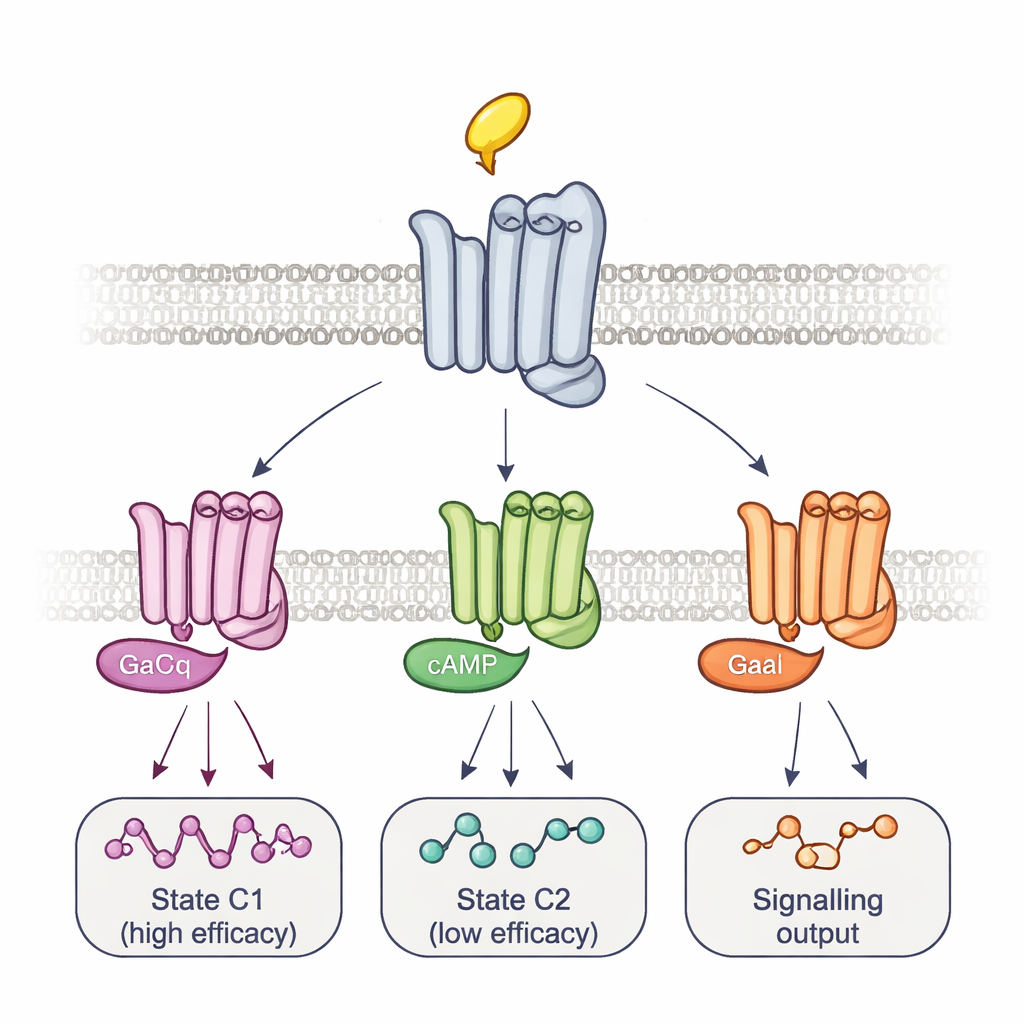
複数の複合体と時間に沿ったシグナル経路
これらの形状を実際のシグナル伝達に結びつけるため、チームはGタンパク質自体を操作しました。受容体と非常に強く長時間結合する変異Gタンパク質を過剰発現させると、いくつかの報告子部位からの信号が選択的に消え、他の部位の信号は強化されました。このパターンと蛍光変化の時間経過から、少なくとも二つの主要な受容体–Gタンパク質複合体が明らかになりました:速やかに形成され高効力を示す複合体と、遅く形成され低効力の複合体です。異なる薬はこれらの複合体間のバランスを変え、そこに到達するために異なる中間段階を用いることで薬特異的な活性化軌跡を描きました。14種のGタンパク質サブタイプのパネルを監視する別の生物発光アッセイを用いて、これらの平衡状態が単に薬の全体的な活性度を決めるだけでなく、どの正確なGタンパク質がオンになるかを決定するのに寄与することを示しました。例えば、アレコリンは特定のGoタンパク質を優先的に活性化し、一方ピロカルピンは低効力複合体を強く支持しました。
なぜこれがより良い医薬品に重要なのか
専門外の人への要点は、単一の受容体が一つのスイッチではなく、異なる経路から到達できる関連するスイッチの集まりであり、それぞれがわずかに異なる下流効果に結び付いているということです。本研究は、試験管内の単純化した系ではなく、完全な細胞内でそれらの経路と状態を直接的に可視化しました。特定の薬が受容体を特定の複合体やGタンパク質パートナーへどのように偏らせるかを地図化することで、研究者は有益な信号を駆動しつつ副作用に結びつく状態を避けるよう受容体を誘導する“賢い”薬の設計のための設計図を得られます。ここで開発された蛍光バイオセンサー戦略は多くの他の受容体にも適用可能であり、生きた細胞における薬作用のリアルタイムな振付けへの窓を開くでしょう。
引用: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
キーワード: GPCRシグナル伝達, リガンド効力, Gタンパク質, 立体配座バイオセンサー, 創薬