Clear Sky Science · ja
双方向CRISPRスクリーニングがGLIS3依存の線維化細胞回路を解読する
治癒が有害な瘢痕化に変わるとき
腸は日々の擦り傷や刺激から自らを修復するようにできています。しかしクローン病や潰瘍性大腸炎のような慢性疾患では、この修復過程が暴走し、腸管を狭め手術を必要とすることがある厚く硬い瘢痕組織を生じます。本研究は、腸内の免疫細胞と構造細胞の間に潜む対話がこの瘢痕化を駆動していることを明らかにし、回路を断つ手がかりとなるスイッチ、GLIS3という遺伝子を特定しています。
炎症を起こした腸内の隠れたネットワーク
なぜ一部の患者で頑固な炎症や線維化が起きるのかを解明するため、研究者たちはヒト腸の細胞「アトラス」を作成しました。個々の細胞で発現している遺伝子を読むシングルセルRNAシーケンシングと、実際の組織切片上でそれらの細胞の位置をマッピングする空間プロファイリングを組み合わせています。クローン病、潰瘍性大腸炎、健常対照のサンプルを用いて腸壁全体で400万を超える細胞を描き出しました。その群の中で際立っていたのが1つの線維芽細胞サブグループ、炎症関連線維芽細胞(IAF)です。これらの細胞は活動性かつ慢性の大腸炎領域に集まり、標準的な抗TNF療法に抵抗する遺伝子署名を示しており、治療困難な疾患で中心的な役割を果たしていることが示唆されます。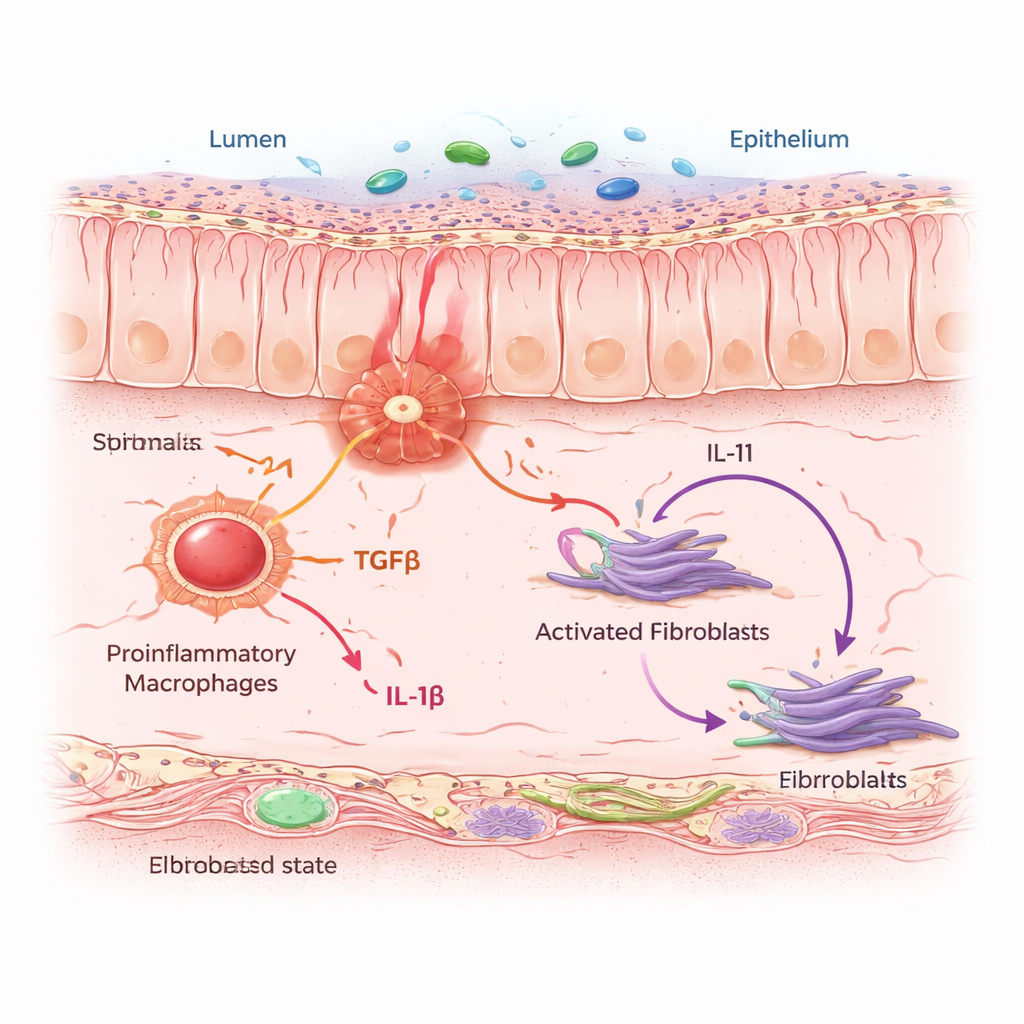
マクロファージが囁き、線維芽細胞が瘢痕を作る
IAFは単独で動いているわけではありませんでした。これらは炎症促進性マクロファージが濃密にいる「近隣」に集まっていました──危険を感知して警報信号を放出する免疫細胞です。計算モデルと細胞共培養実験を用いて、マクロファージが炎症状態に駆動されると、TGFβとIL-1βという2つの主要なシグナル伝達タンパク質を分泌することが示されました。近傍の線維芽細胞はこれらのシグナルを特定の受容体で受け取ります。両方のシグナルが同時に到来すると、線維芽細胞はIAF状態にスイッチし、既に線維化促進に関与すると疑われていたサイトカインIL-11に加え、コラーゲンやその他のマトリックスタンパク質を産生して腸壁を厚く硬くします。慢性大腸炎処置を受けたマウスでは、IL-11を阻害するか線維芽細胞で選択的にIL-11を欠失させると、初期の炎症を抑えずにコラーゲン沈着が減少し、IL-11が瘢痕化段階の重要な駆動因子であることが示されました。
GLIS3:線維化線維芽細胞のマスタースイッチ
相関から機構へ進むために、著者らは強力な全ゲノムCRISPRツールを用いました。IL-11産生を蛍光タグでモニターできるように改変したヒト線維芽細胞を作成し、全ゲノムで遺伝子を破壊するスクリーニングと活性化するスクリーニングを並行して行いました。TGFβとIL-1βで刺激した後に異常に多いまたは少ない量のIL-11を産生する細胞を分取することで、この応答を制御する遺伝子を同定しました。多くのシグナル成分の中で、1つの転写因子――GLIS3――が主要な調節因子として浮上しました。GLIS3を無効化すると線維芽細胞のIL-11産生は大幅に減少し、GLIS3を増強するとIL-11は急増しました。追加実験では、GLIS3はマクロファージシグナルに応答して線維芽細胞の核内に移行し、IL11遺伝子近傍を含むDNAに直接結合して、コラーゲンやさらに免疫細胞を惹きつける因子を含む広範な炎症・線維化遺伝子プログラムを活性化することが示されました。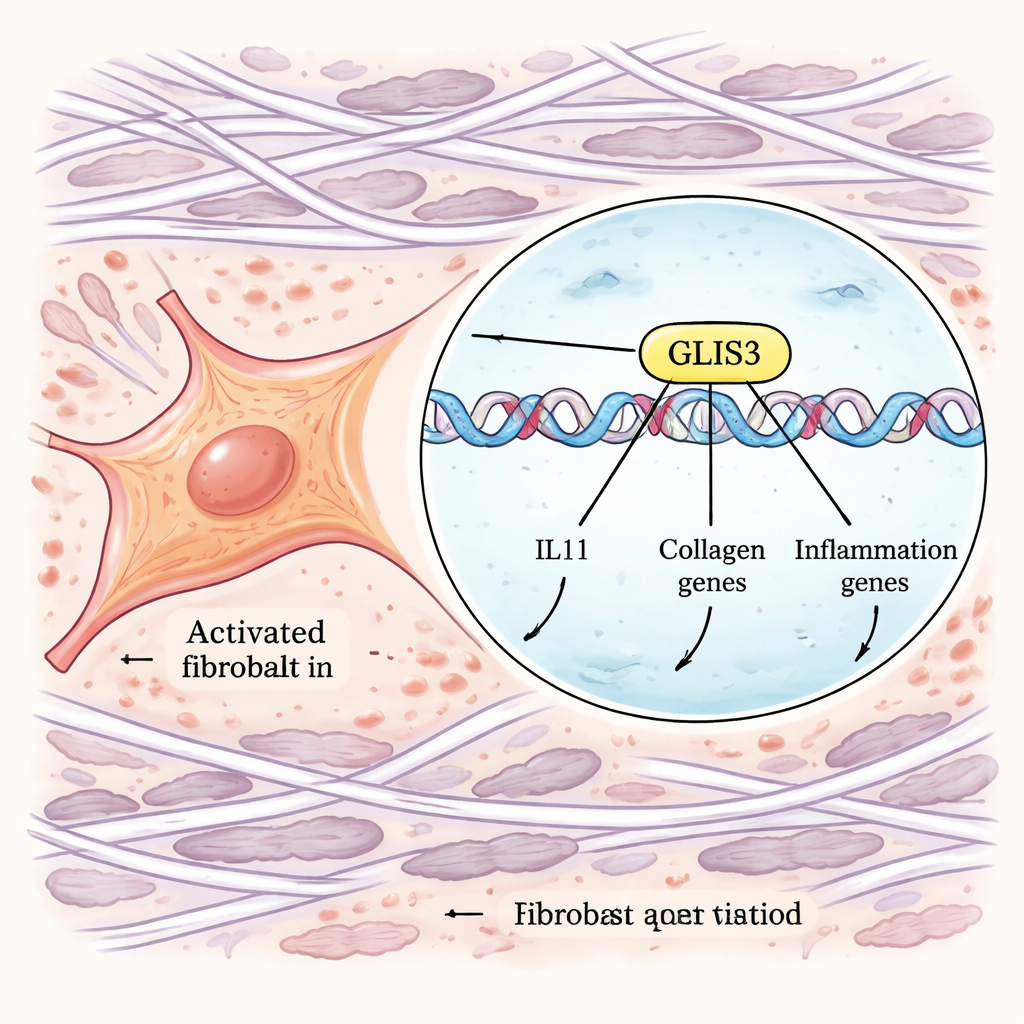
マウスモデルから患者の重症度へ
次に、このGLIS3駆動プログラムが生体で重要かどうかを検証しました。マウスではGLIS3を線維芽細胞からのみ除去できる系統を作成しました。この動物に慢性大腸炎を与えると、腸の瘢痕化が抑えられ、コラーゲンと線維化遺伝子の発現が低く、正常マウスと比べて炎症も軽減しました。空間マッピングは、GLIS3欠損マウスがIL-11産生線維芽細胞や近傍の活性化マクロファージや好中球が少ないことを確認し、GLIS3を妨げることが炎症―線維化回路全体を弱めることを示しました。小児潰瘍性大腸炎の大規模コホートに目を向け、著者らは50遺伝子からなるGLIS3「シグネチャ」を抽出し、その活動が大腸生検における疾患重症度やIAFおよび活性化マクロファージの豊富さと密接に一致することを示し、この経路が患者の転帰に直接関連していることを示しました。
炎症と瘢痕化の悪循環を断つ
専門外の方にとっての要点は、本研究が自己強化するループを明らかにしたことです:炎症性マクロファージが線維芽細胞を瘢痕形成するIAFへと誘導し、これらのIAFはGLIS3の制御下でIL-11、コラーゲン、組織を再構築しさらに炎症細胞を惹きつける因子を大量に産生します。免疫系を広く抑える標準薬はこのループを完全には断てない可能性があり、それが多くの患者が既存療法に最終的に失敗する理由の一つを説明します。GLIS3とIL-11産生線維芽細胞の状態を炎症―線維化回路の中心ノードとして特定したことで、この研究は免疫細胞だけでなく線維芽細胞を標的にしたより選択的な戦略が、将来的に炎症性腸疾患や他の慢性炎症疾患における瘢痕化を予防または逆転させる可能性を示しています。
引用: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
キーワード: 炎症性腸疾患, 腸管線維症, 線維芽細胞, マクロファージ, GLIS3