Clear Sky Science · ja
ストレスはヒストンH3のユビキチン化を介してヘテロクロマチンの継承を制御する
細胞はどのようにストレスを記憶するか
私たちの細胞は、熱、栄養欠乏、薬剤暴露など過去のストレスを「記憶」しておく方法を必要とします。そうすることで次回はより速く応答できます。強力な記憶システムの一つがヘテロクロマチンで、DNAを高密度に折りたたんで特定の遺伝子を多くの細胞分裂にわたって不活化したままにします。本稿は、細胞がストレスに応じてその記憶を能動的に調整する仕組みを検討し、環境情報を長期的な遺伝子活性の変化につなぐ分子ハブを明らかにします。この制御系の理解は、真菌が薬剤耐性を進化させる仕組みや、ストレスが私たち自身の細胞のエピジェネティックな景観をどのように再形成するかを説明する手がかりとなる可能性があります。
ゲノムにかけられた錠
ヘテロクロマチンは、ある領域のDNAにかけられた分子的な錠のように考えられ、近傍の遺伝子を沈黙させます。その錠は主にヒストンタンパク質に付く化学的標識、特にH3K9me3と呼ばれるマークによって構築されます。一度確立されると、DNA複製のたびに自分自身をコピーでき、基礎となるDNA配列を変えずに遺伝子抑制のパターンが継承されます。これまでの研究では、この自己複製は主に「読み取り–書き込み」のフィードバックループに依存するという考えが支配的でした:酵素複合体が既存のH3K9me3マークを認識して隣接するヒストンに同じマークを付け、静的ドメインを徐々に広げるというものです。しかしこのモデルだけでは、環境条件がヘテロクロマチンの拡張を促進したり遅らせたり方向付けたりする仕組みを十分に説明できませんでした。
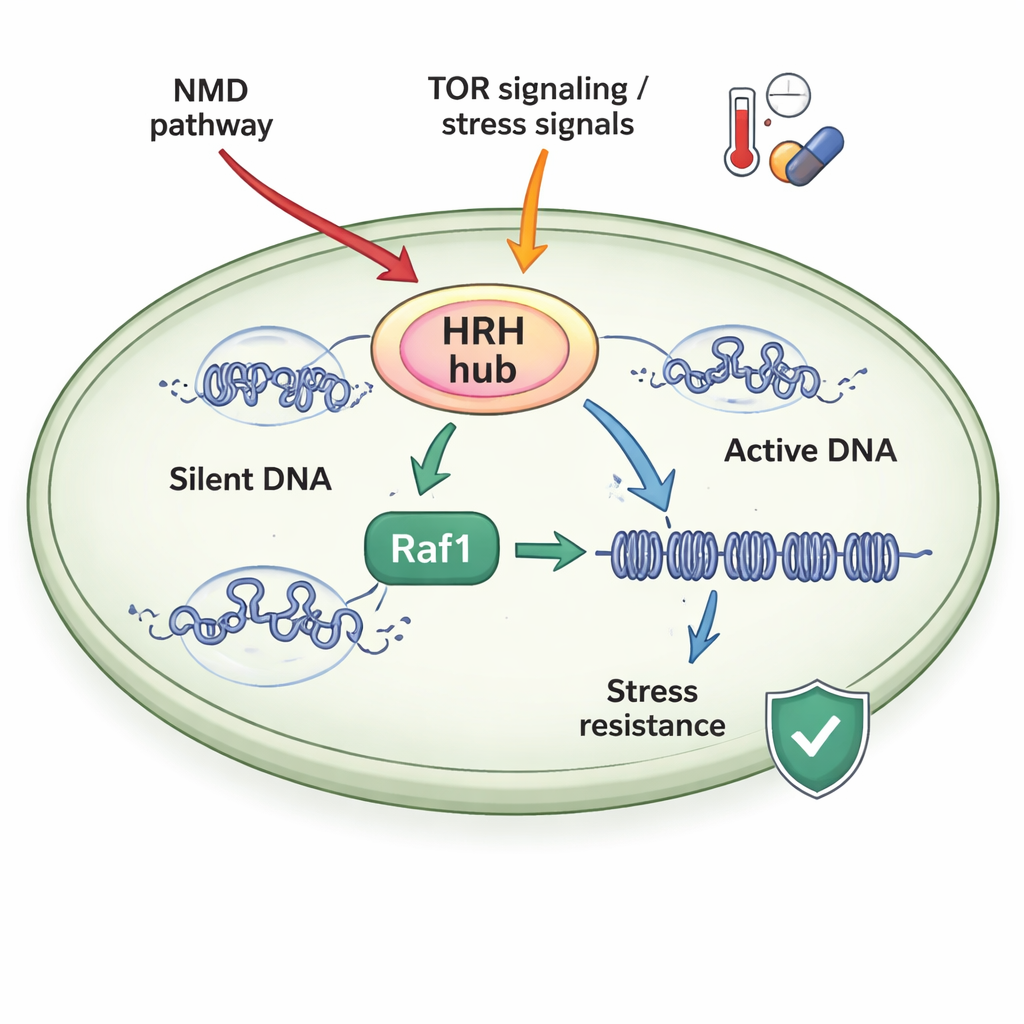
ストレス感受性の制御ハブ
著者らは、クロマチン機構がより高等な生物によく似ている単純なモデル生物、分裂酵母を用いて研究しました。彼らは、H3K9me3マークを「書く」だけでなく、ヒストンH3の別の部位に小さなタンパク質ユビキチンを付加する複合体Clrc(ClrCと表記されることもある)に着目しました。ClrCの重要なサブユニットであるRaf1は、制限的な「門番」として機能します:Raf1が不足すると、主要な酵素であるClr4の多くがクロマチン上の複合体に参加せずに遊離し、沈黙ドメインの広がりが失敗します。逆にRaf1が十分に存在すると、より多くのClrCが組み立てられてDNAに安定に結合し、H3K14ubとH3K9me3のマークが染色体に沿って伸びて遺伝子サイレンシングを強化します。
ユビキチンで錠を微調整する
ゲノム全体でクロマチン標識をマッピングした結果、H3K14ubはヘテロクロマチンが形成される場所に強く濃縮しており、Raf1が除去されるとこの標識はほぼ消失することが示されました。ユビキチン付加の段階を阻害する変異(出発点ではH3K9me3は残る)を持つ細胞では、沈黙ドメインは外側へ広がることができません。言い換えれば、H3K14ubは単なる飾りではなく、ヘテロクロマチンの前線を押し進めるために必須です。生化学的およびイメージング実験はその理由を示します:H3K14ubはClr4酵素の活性を大きく高め、複合体全体をクロマチン上に留めるのに寄与して、局所的なH3K9me3密度を安定継承に必要な閾値以上に引き上げます。注目すべきは、Raf1レベルの上昇が通常はこれらの沈黙ドメインの維持に必要な他のいくつかの因子を回避できることで、Raf1駆動のユビキチン化が中心的な制御レバーであることを強調しています。
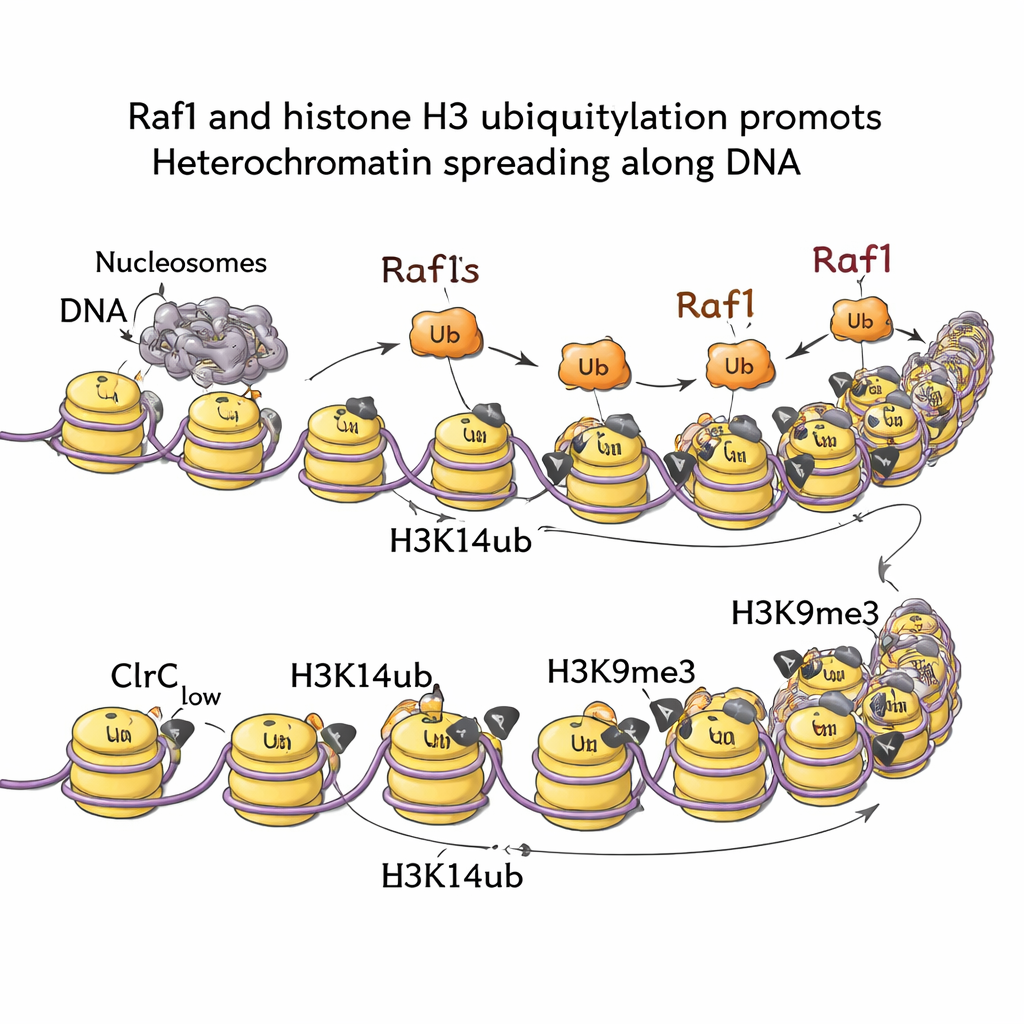
RNA分解と成長経路からのシグナル
細胞はRaf1レベルを偶然に任せてはいません。本研究は、2つの主要なストレス応答系が著者らがヘテロクロマチン継承性制御ハブ(HRH)と呼ぶ、Raf1を中心としたハブに情報を供給していることを示します。まず、欠陥のあるmRNAを分解することで知られるナンセンス媒介mRNA分解(NMD)経路は、Raf1をコードするメッセンジャーRNAを標的にし、通常条件ではRaf1レベルを低く保ちます。NMDを無効にするとRaf1 mRNAが安定化してRaf1タンパク質量が増加し、沈黙ドメインを維持できない変異株でのヘテロクロマチンの広がりが回復します。第二に、キナーゼGad8を介して作用する成長およびストレスのセンサーであるTORC2は、Raf1の発現を促進します。高温はこの経路をオフにし、Raf1レベルを下げ、ヘテロクロマチンを弱め、Raf1が実験的に増強されない限り細胞が沈黙状態を維持するのを難しくします。
ストレス、薬剤耐性、そして広範な含意
著者らはこの分子ハブを現実世界の適応と結びつけます。カフェインに酵母をさらすと、カフェインは他の系でもNMDを鈍らせることが知られており、Raf1レベルが上昇してヘテロクロマチンが新しい部位に広がりやすくなります。その中には、サイレンシングされるとカフェインや抗真菌薬に対する耐性を与える遺伝子群も含まれます。同様に、人工的にRaf1を高めた細胞は、一般的な抗真菌薬であるフルコナゾールやクロトリマゾールに対してより耐性を示します。逆に、熱やTORC2–Gad8シグナルの喪失でRaf1が低下するとヘテロクロマチンは不安定になり、エピジェネティック記憶は消えやすくなりますが、Raf1が回復すれば元に戻ります。Raf1様タンパク質、ClrC複合体、H3K14ubマークはいずれも病原性真菌や哺乳類に相当物が存在するため、類似のストレス感知型エピジェネティックハブが多くの種で薬剤耐性、発生、疾患に影響を与えている可能性が示唆されます。
なぜ重要か
日常的な観点から見ると、この研究はクロマチンによる遺伝子サイレンシングが硬直した錠ではなく、賢く調整可能なシステムであることを示しています。細胞は中心的なハブを用いて環境の手がかり―温度変化、栄養状態、化学的ストレス―を読み取り、Raf1を上下に調節します。すると、どれだけのゲノムが長期的な沈黙に包まれるか、そして細胞がDNAを変えることなくどれほど容易に「再プログラム」されうるかが決まります。この過程におけるヒストンH3のユビキチン化とRaf1量の重要な役割を明らかにしたことで、ストレスがどのように迅速にエピジェネティックな景観を再形成するかの設計図が提示され、真菌の薬剤耐性やヒト疾患における異常な遺伝子サイレンシングに影響を与える新たな手法の示唆となります。
引用: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
キーワード: ヘテロクロマチン, エピジェネティック継承, ヒストンのユビキチン化, ストレス適応, 真菌の薬剤耐性