Clear Sky Science · ja
改変した腫瘍細胞から作製された生体模倣小胞が術後がん免疫療法のための個別化ワクチンとして機能する
腫瘍の残りを第二の防御線に変える
固形腫瘍の多くの患者にとって、手術は長い闘いの最初の一手にすぎません。腫瘍の大部分が取り除かれても、ごく小さながん細胞の塊が残って後に致命的な転移を引き起こすことがあります。本研究は、患者自身の腫瘍細胞を個別化ワクチンに変えるという工夫に満ちた方法を探り、術後にこうした残存細胞を追跡して免疫系ががんの再発を阻止するのを助けることを目指しています。
残存がん細胞が消しづらい理由
標準治療は、外科医が主要な腫瘍塊を除去した後に残る細胞に対して苦戦します。これらの散在する細胞はしばしば遠隔の臓器に潜み、薬剤や免疫の攻撃から遮蔽されています。既存の免疫ベースのワクチンは樹状細胞と呼ばれる特殊な免疫細胞を使って体に腫瘍マーカーを認識させようとしますが、これらの生きたワクチンは製造が難しく、主要な免疫器官に効率よく到達せず、臨床での効果は控えめでした。中心的な課題は、各患者のがんが独自の変異の組み合わせを持つため、画一的なワクチンは重要な標的を見逃しがちであることです。
がん細胞をより目立たせる隠れたスイッチ
研究者たちは、細胞が内部の情報を免疫の監視役に示す能力を高める自然のスイッチを探すことから始めました。彼らはシンタキシン11と呼ばれるタンパク質に注目しました。このタンパク質は通常免疫細胞に豊富に存在しますが、多くの腫瘍では乏しいことが知られています。マウスモデルの攻撃的な乳がん細胞でこのタンパク質を増強すると、がん細胞は専門的な免疫監視役のように振る舞い始め、分子の“名札”や補助信号を細胞表面により多く表示するようになりました。つまり、腫瘍細胞は隠れるのではなく、独自の特徴を免疫系により明確に示すように再プログラムされたのです。
小さな模倣免疫メッセンジャーの構築
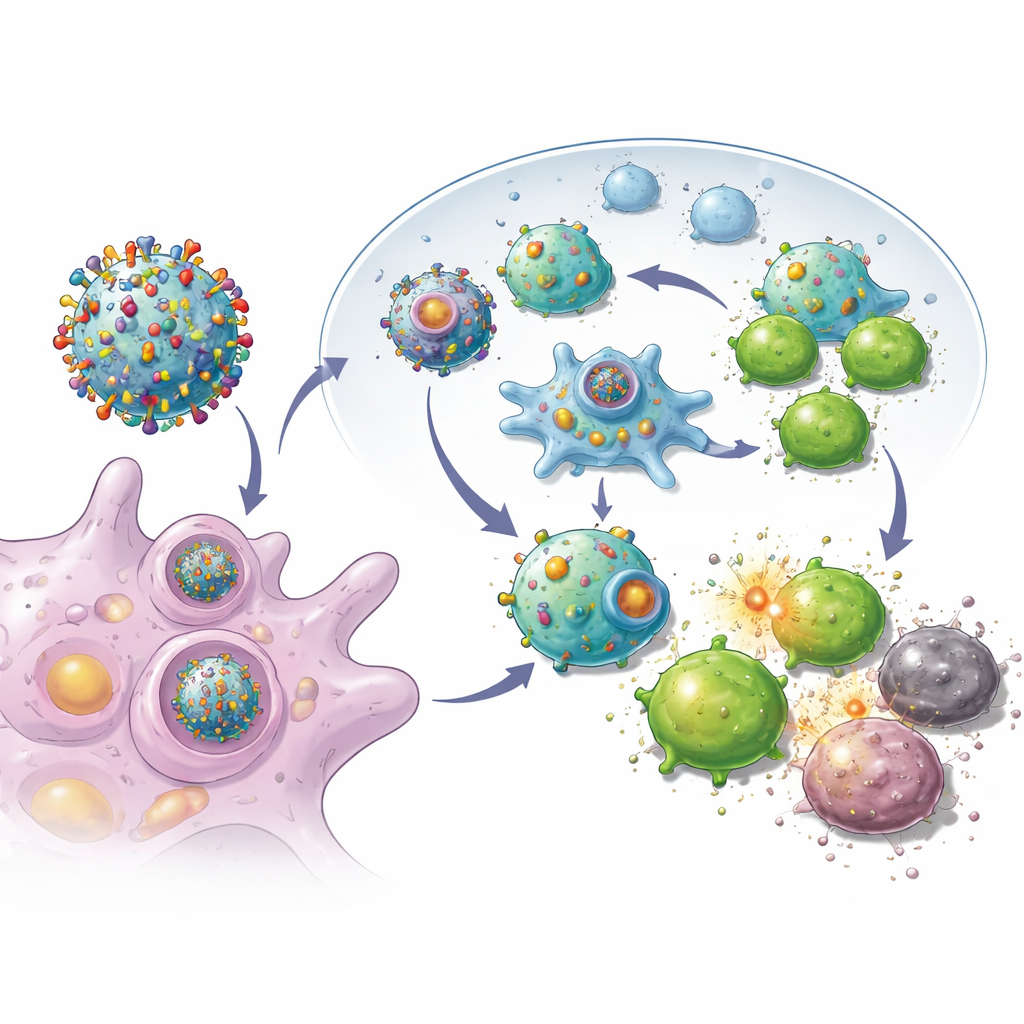
この再プログラムされた腫瘍細胞を得たチームは、細胞の外膜を剥ぎ取り、それを生分解性ナノ粒子にコーティングしました。そのナノ粒子には小さな免疫刺激薬が充填されています。その結果、その腫瘍に特有のマーカーをすべて含み、さらにキラーT細胞向けの“作動”信号を内包したナノスケールの小胞群が得られました。これらを手術後にマウスの皮下に注射すると、小胞は近傍のリンパ節へ効率的に移動し、そこは免疫細胞が教育される場です。そこで小胞は直接キラーT細胞を活性化したり、自然の免疫監視細胞に取り込まれて応答をさらに増強したりしました。実験では、これらの小胞にさらされたT細胞はより激しく増殖し、単純なナノ粒子設計で訓練されたT細胞よりもがん細胞を破壊する能力が高いことが示されました。
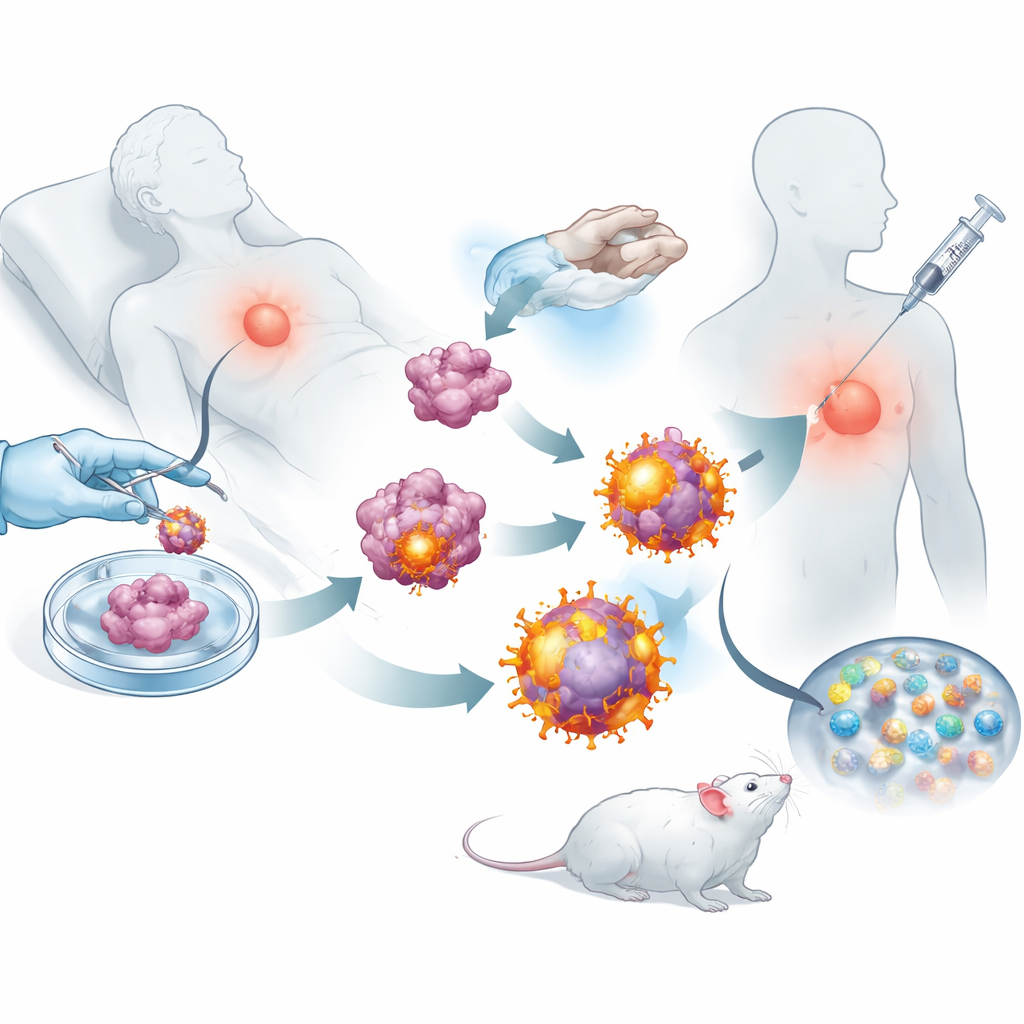
術後にがんを抑える
研究者たちは、乳がんおよび黒色腫のいくつかのマウスモデルで、このテーラーメイドワクチンが実際に病状を変えられるかどうかを検証しました。乳腺腫瘍の大部分が外科的に切除された動物では、ワクチン接種を受けたマウスは再発が小さく、肺転移も未治療群よりはるかに少なかった。処置を受けたマウスのリンパ節、脾臓、腫瘍には活性化したキラーT細胞と長期間存在する記憶細胞があふれており、免疫系が目覚めて長期にわたって訓練されたことを示唆していました。腫瘍がT細胞を麻痺させるのを防ぐ既承認のチェックポイント阻害抗体と組み合わせると、ワクチンは持続的な腫瘍制御をもたらし、多くのマウスで完全退縮と長期生存が得られました。
個別化治療を速める
この概念を実臨床に移す上での障害の一つは時間です。遺伝子ベースの方法で腫瘍細胞を再プログラムするのは時間がかかる場合があります。これに対処するため、チームは天然化合物をスクリーニングし、デオキシポドフィロトキシンという小分子を発見しました。これはスイッチとなるタンパク質と同じ免疫刺激的な表面マーカーのレベルを迅速に上昇させます。この近道を用いることで、彼らは短時間で同様の小胞被覆ナノ粒子を作製しつつ、強力で腫瘍特異的な免疫応答を呼び覚ます能力を保ちました。試験では、この薬剤を使って作られたワクチンは遺伝子ベースの方法で作成したものと同等に効果的であり、その有益性は一般的ながん細胞毒性ではなく、正しい腫瘍型を認識することに依存していることが示されました。
将来のがん医療にとっての意義
非専門家に向けた要点は、患者自身の腫瘍を免疫系のための小さな訓練ツールに作り替えられる可能性があるということです。がん細胞を豊富で個別化された情報源に変え、その情報を堅牢なナノスケールの担体に載せることで、このアプローチは手術で残された細胞を掃討し、新たな増殖の定着を防ぐことを目指します。人に対してこうしたワクチンを日常的に提供する前には、安全性と有効性の立証や信頼できる製造パイプラインの構築など多くの段階が残されていますが、本研究は術後に高い個別化を実現し、外科が始めた治療を免疫系が完了する道筋を示しています。
引用: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
キーワード: がんワクチン, 免疫療法, ナノ医療, 術後治療, 個別化腫瘍学