Clear Sky Science · ja
生体内でのDNA折り紙の構造的完全性と薬物動態の解明
体内で小さなDNA機械を観察する
DNAは紙のように折って小さな三次元形状を作ることができ、これをDNA折り紙と呼びます。これらのナノ構造体は、薬物、ワクチン、あるいはシグナル分子を精密に運ぶように設計できます。しかし一度体内に注入されると、それらは十分長く完全な形で残るのか、あるいはすぐに崩れてしまうのかは明確ではありません。本記事は、生きた動物内でこれらのDNA機械がどのくらい生き残るか、血流中をどのように移動するか、さらには各構造のどの部分が先に壊れるかを明らかにする、新しい観察法を紹介します。
なぜDNAの折り畳みが医療を変える可能性があるのか
DNA折り紙は、遺伝情報を保持する塩基対のルールを利用しつつ、それをナノスケールの物体を組み立てるために転用します。研究者はこれらの物体上にタンパク質、薬物、免疫賦活シグナルをレゴのプレート上の突起のように配置でき、がんや自己免疫疾患、感染症に対する高度に制御された治療を作り出せます。こうした精密治療を安全かつ効果的にするためには、規制当局や研究者がこれらの構造体が体内でどの程度完全な形を保つか、またどれくらい速く除去されるか(薬物動態)を把握する必要があります。従来の追跡法は蛍光色素を結合したりDNA断片を単に数えたりすることが多く、分解した破片があたかも完全なナノ構造体であるかのように見えてしまうことがあります。これまで、生体内で元のDNA折り紙形状自体が依然として完全かどうかを実用的に識別する方法はありませんでした。
DNA折り紙のための分子“完全性テスト”
著者たちはPLASTIQと名付けた手法を開発しました。これはproximity ligation assay for structural tracking and integrity quantificationの略です。重要な発想は、DNA折り紙自身にその状態を報告させることです。各構造の特定位置には、折り紙が適切に折り畳まれているときにらせん沿いに肩を並べるように隣接する短いステープル(補助鎖)対を配置します。各対のうち一方には、小さな化学タグが付けられており、それらは酵素的に結合(ライゲーション)できるようになっていますが、それは元のスキャフォールド鎖によって近接が保たれている場合に限られます。構造が溶ける、切断される、あるいは酵素により分解されると、これらの断片は離れ、もはや結合できなくなります。ライゲーションの後、結合された対は標準的なポリメラーゼ連鎖反応で増幅され、感度の高いqPCRやシーケンシングで定量されます。これにより、血液のわずかなマイクロリットルからでも、局所的に完全なセグメントが存在するかどうかを測定可能な信号に変換できます。
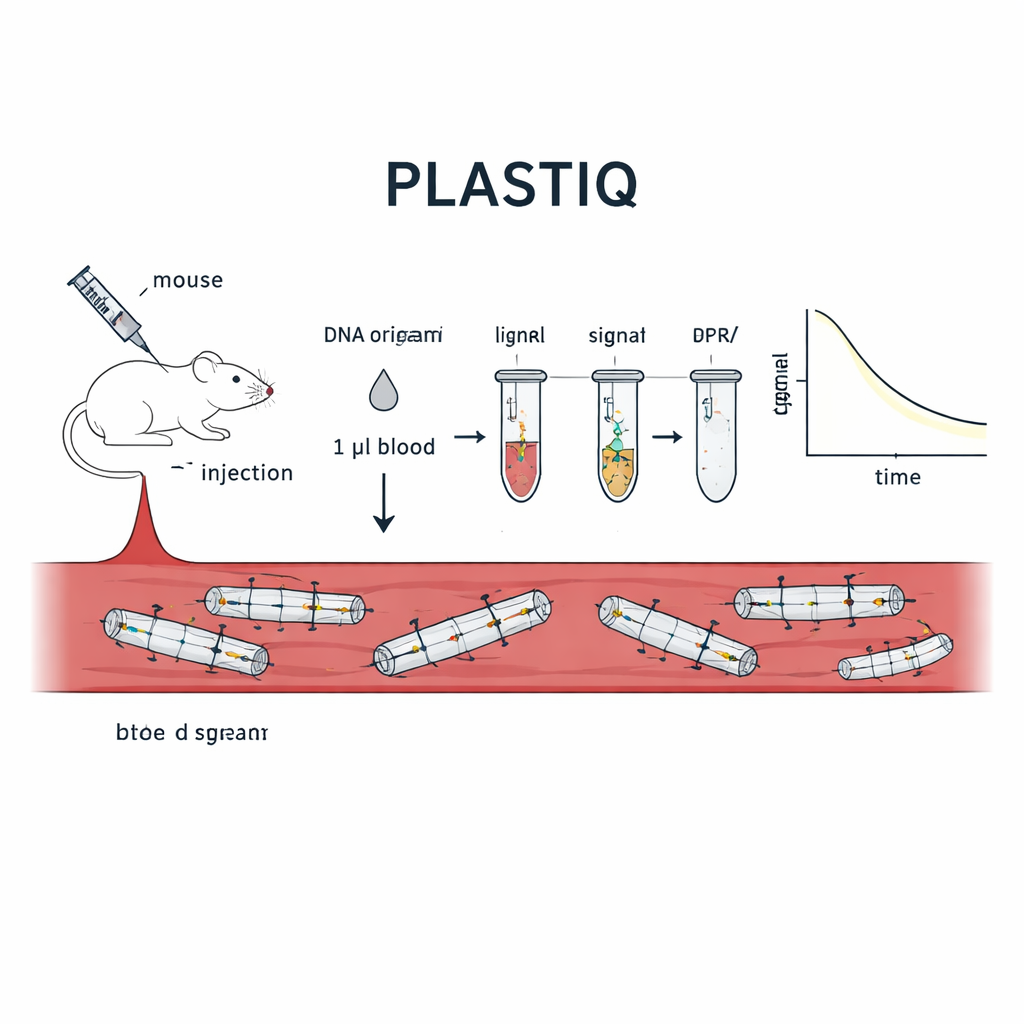
生きたマウスでテストを実施する
PLASTIQが本当に構造的完全性を測定できることを示すため、著者らはまず試験管内で単純なロッド状DNA折り紙設計に適用しました。信号はロッドが完全なときにのみ現れ、熱による展開後には消えましたが、従来のDNAベースのアッセイは形状にかかわらずDNAを検出し続けました。次にこれらのロッドをマウスにさまざまな経路で注入しました—血流への直接注入、腹腔内、筋内、皮下注入—そして各時点でわずか1マイクロリットルの血液を採取しました。PLASTIQは、注入経路によって完全な構造体の濃度がどのように急増してから減衰するかを明らかにし、薬物動態の一般的な期待と一致しつつもはるかに細かい構造情報を示しました。この方法は0.01フェムトモーラーまで感度があり、それでいて必要な血液量は最小限で、同じ動物から時間を追って繰り返しサンプリングできます。
保護コーティングと隠れた弱点の検証
多くの研究グループはPEGなどのポリマーでコーティングしたり、紫外線で鎖を架橋したり化学的結合剤を加えたりしてDNA折り紙を保護しようとしますが、これらの工夫が実際に生体内でどれだけ有効かを観察するのは難しいことでした。PLASTIQを用いて著者らは、血流中のPEG被覆ロッドは裸のものよりわずかに長く完全性を保つが、循環に入るとより速く除去されること、そしてそのコーティングはPLASTIQの酵素の作用を妨げないことを示しました。PLASTIQを単純な数学モデルと組み合わせることで、注入経路やコーティングごとの吸収率と除去率を抽出し、反復投与レジメンのシミュレーションすら可能にしました。さらに二重層の樽型折り紙のようなより複雑な構造にも手法を適用し、内側が外側よりも密に詰められた設計を検証しました。PLASTIQの測定は、露出した外側のステープルが内側の空洞に面したものよりも速く完全性を失うことを示し、埋もれたらせんが血中の分解酵素から遮蔽されていることを直接的に確認しました。
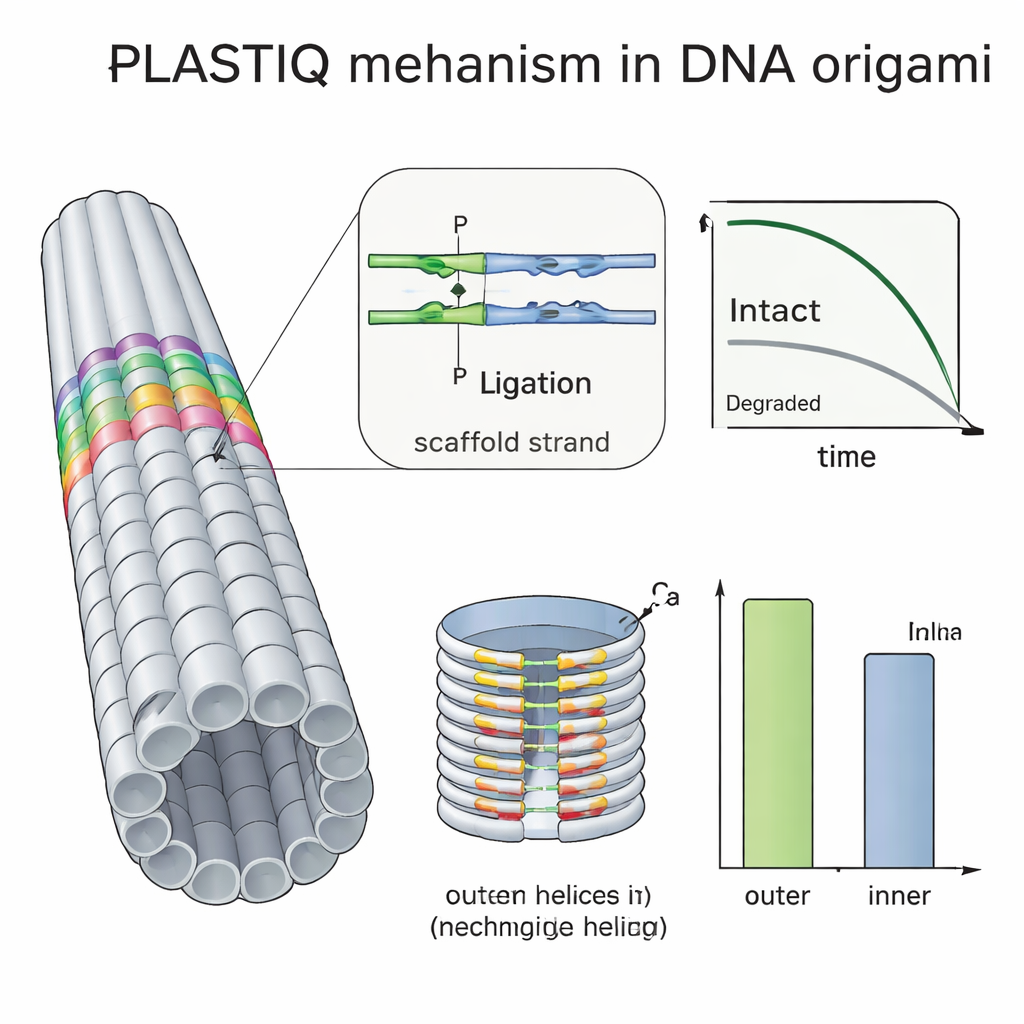
将来のDNAベース治療への意味
非専門家にとって、PLASTIQは体内を移動するナノスケールのDNAデバイスのための構造的な健康チェックと見なせます。「ここにDNAがあるか?」という問いだけでなく、「このDNAは我々が設計した正確な物体としてまだ折り畳まれているか?」と問います。微量の血液サンプルから高感度にその問いに答えることで、PLASTIQはDNA折り紙ベースの医薬品やワクチンの設計、コーティング、投与量を最適化する手段を薬剤開発者に提供します。時間とともに、こうしたナノ構造体が実際の生物環境でどのように振る舞うかに関する詳細で定量的な洞察は、DNA折り紙を優雅な実験室の概念から信頼性が高く規制対応可能な治療へと変える助けとなるでしょう。
引用: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
キーワード: DNA折り紙, ナノ医療, 薬物送達, 薬物動態, ナノテクノロジー