Clear Sky Science · ja
モノバレント擬天然物質がIDO1をその本来のE3であるKLHDC3で強力に分解する
がんに都合のいい酵素を停止させる
私たちの免疫系は常にがん細胞を監視していますが、腫瘍はしばしば体内の化学反応を乗っ取り反撃します。この綱引きにおける重要な役者の一つがIDO1という酵素で、腫瘍が免疫細胞の働きを奪うのに役立ちます。本研究はIDO1の活性を単に阻害するだけでなく、細胞にその酵素を完全に除去させる新しいクラスの低分子を報告します。細胞の自然な廃棄機構を利用することで、これらの化合物は従来薬では成し得なかったかたちで腫瘍に対する免疫攻撃を復活させる可能性があります。
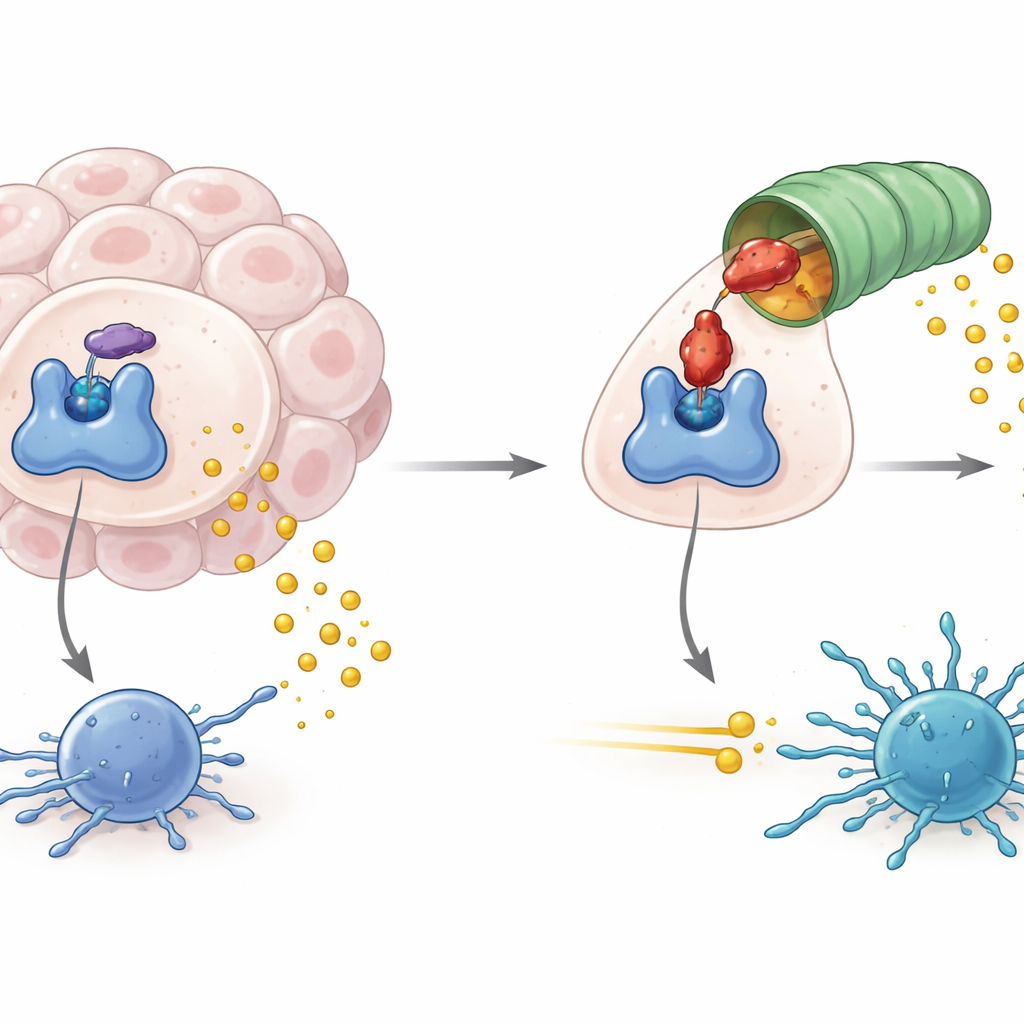
腫瘍が代謝の門番を悪用する仕組み
IDO1はアミノ酸トリプトファンをキヌレニンという産物に分解する代謝経路の入り口に位置します。IDO1が豊富で活性が高いとトリプトファンが減少しキヌレニンが上昇して、腫瘍に対抗するT細胞を含む免疫細胞の働きを弱める化学的環境が生じます。高いIDO1活性は抗腫瘍免疫の低下だけでなく、ウイルス性リンパ腫や一部の神経変性疾患にも関連しています。したがって薬剤開発者はIDO1の酵素活性を阻害することに注力し、この免疫抑制シグナルを断ち既存のがん免疫療法の効果を高めようとしてきました。
なぜ単純な酵素阻害薬は限界があったのか
動物実験では有望でも、従来のIDO1阻害剤の臨床試験は失望を招きました。そこから浮かび上がってきた説明の一つは、IDO1は単なる触媒以上の存在であるという点です。化学反応が遮断されても、タンパク質自身がシグナルのハブとして働き、依然として腫瘍の成長や転移を促進することがあります。ある阻害剤はむしろIDO1を安定化させ、細胞内のタンパク質量を増やしてしまうことさえあります。言い換えれば、触媒機能を止めるだけでは酵素以外のがん促進的な役割を放置するか、場合によってはそれを強化してしまう可能性があるのです。
自己分解を誘導する化合物の設計
著者らは大規模な「擬天然」分子ライブラリを探索しました—天然物に着想を得た断片を合成的に組み替えた化合物群です。そこでiDegsと名付けられた分子群を発見しました。これらは(−)-ミルタノールと呼ばれる植物様の構成要素に由来します。iDegsはIDO1のヘム(鉄含有補因子)が結合する通常のポケットに結合し、ヘムを置換します。ヘムを置き換えることでiDegsはキヌレニン産生能を弱めるだけでなく、重要なことにタンパク質の尾部の一部の構造を再形成させます。高分解能の結晶構造は、iDegsがヘム部位を占めるときに、通常はコンパクトで保護された構造をとるC末端ヘリックスが緩み部分的に秩序を失うことを明らかにしています。
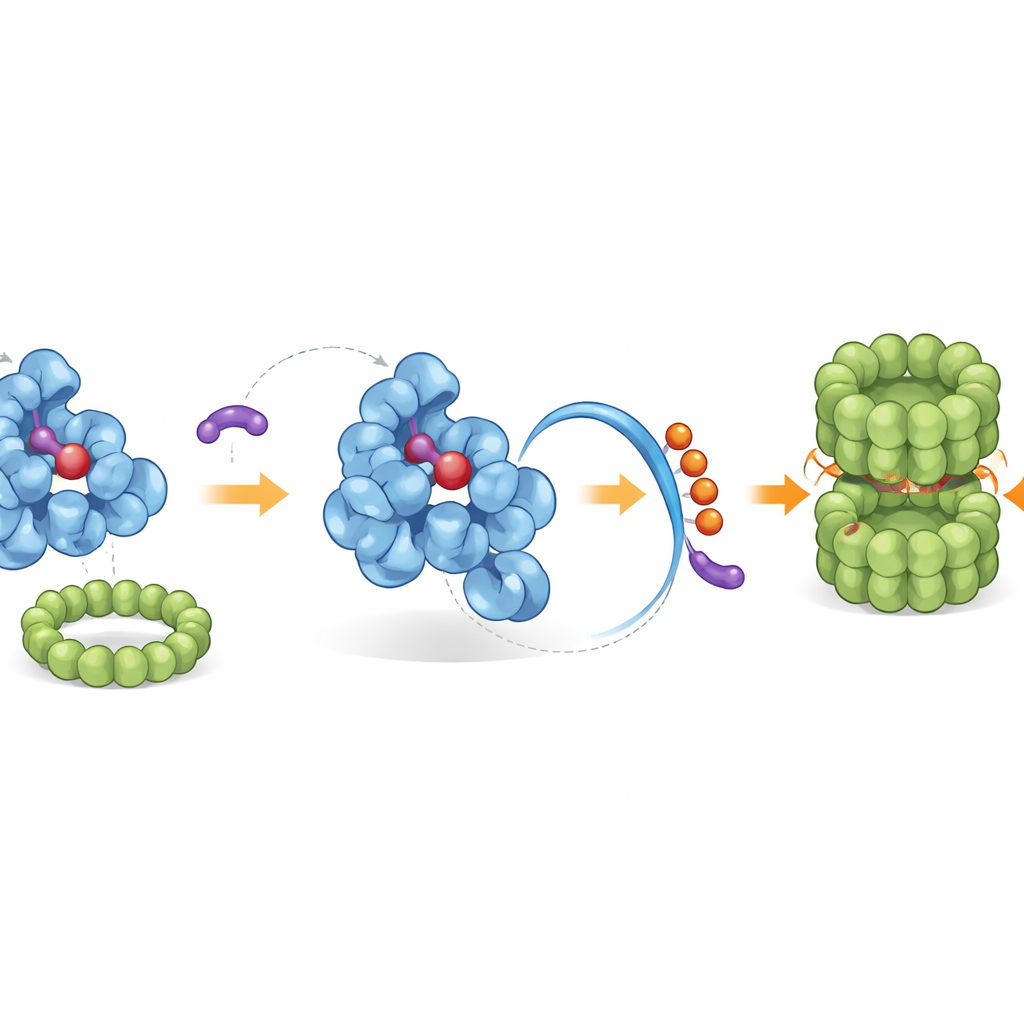
細胞の本来の清掃チームを呼び寄せる
再構成された尾部は細胞の廃棄機構が認識する内在の「終端タグ」を露出させます。遺伝学的スクリーニングと生化学的再構成により、研究者らは特定のリガーゼ複合体、CRL2–KLHDC3がID01の露出した尾部に小さなユビキチンの“フラグ”を自然に付加し、プロテアソーム—細胞の分子シュレッダー—による分解へと導くことを同定しました。通常はヘムが存在しないフォームのIDO1だけがこの方法で効率的にタグ付けされ、ヘム結合型IDO1は保護されます。iDegsはヘム非結合型にのみ結合してこのバランスを傾け、自然な分解経路を増幅します。シリーズ中の強力な化合物はキヌレニン生産を阻害するだけでなく、IDO1へのユビキチン付加を増強し、複数のがん細胞種でそのタンパク質量を劇的に低下させます。
IDO1の運命と免疫反応の転換
この二重作用は重要な機能的帰結をもたらします。卵巣がん細胞を用いた遊走アッセイでは、酵素を安定化させることが知られる臨床探索中のIDO1阻害剤は細胞移動をむしろ促進し、これはIDO1の酵素以外のがん促進的役割と一致します。対照的に、あるiDeg化合物は移動を遅らせ、酵素阻害とタンパク質自体の消失の双方と整合しました。したがってこの研究はIDO1を操作する新たな方法を明らかにします:巨大な設計分子で別のリガーゼに無理やり引き寄せるのではなく、細胞内で既に存在するネイティブな分解経路を“過電流化”することで達成するアプローチです。
将来のがん治療にとっての意味
専門外の読者に向けた要点は、重要なのは阻害の量だけでなく質だということです。これらの新しい低分子は精密なスイッチのように作用し、IDO1を細胞が破壊するのに適した脆弱な形に固定して、その代謝的およびシグナル伝達的寄与の両方を断ち切ります。iDegsはコンパクトで医薬品的性質を備え、IDO1の除去には細胞自身のリガーゼを利用するため、従来の“タンパク分解薬”よりも繊細で広く応用可能なアプローチを提供する可能性があります。同様の戦略が他の問題となるタンパク質にも適用できれば、本研究は病的な細胞が自らの分子兵器を解体するよう促す新世代の治療法の可能性を示唆しています。
引用: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
キーワード: IDO1, がん免疫療法, 標的タンパク質分解, ユビキチンリガーゼ, 低分子分解剤