Clear Sky Science · ja
ディープラーニングを用いた時間分解能の高い機能ゲノミクスが示すオートファジーの全体的な階層的制御
細胞は自分自身をどう再利用し、いつ止めることを知るのか
細胞は飢餓の時期を乗り切るために、自らの部品をオートファジー(文字どおり「自己食」)と呼ばれる過程で再利用します。再利用が足りないと損傷した構成要素が蓄積し、過剰だと細胞は自らを食いつくしてしまいます。本研究は一見単純だが老化や疾患に大きな示唆を持つ問いを投げかけます:栄養が増えたり減ったりする中で、生きた細胞はどのようにしてオートファジーを適切な瞬間にオン・オフするのでしょうか?
数千の細胞を飢餓から回復まで追う
この問いに取り組むため、研究者たちは酵母をモデルに用い、飢餓と回復を通じて約6,000種類の異なる変異株を観察しました。各酵母株にはオートファジーに関わる構造を標識する蛍光タグが導入され、高性能顕微鏡が栄養を除去してから戻すまでの間、毎時画像を取得しました。こうした画像を手作業で分類する代わりに、チームはディープラーニングアルゴリズムを訓練して、画像の特徴のみから細胞がオートファジー状態にあるかを識別させました。これにより、ほぼ全ゲノムにわたるオートファジー活性の精密な時間経過が得られ、各変異株が栄養変動に対してどの程度、どの速さで応答するかが明らかになりました。 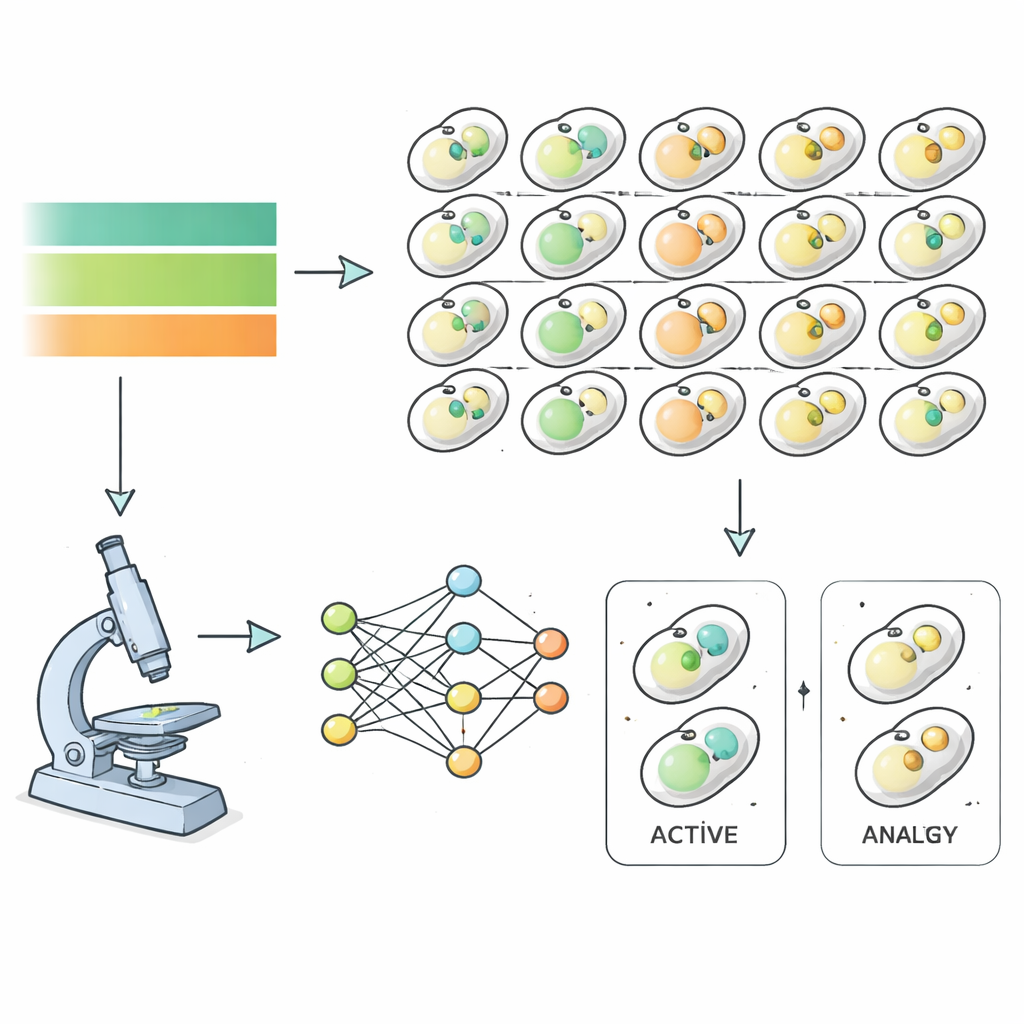
再利用がうまくいかない6つの異なる様式
これらの時間経過を数理的にフィッティングすることで、著者らは各変異株について詳細な「動的指紋」を抽出しました――オートファジーがどれだけ速くオンになるか、どれだけ長く高い状態を保つか、そしてどれほど急速にシャットダウンするか。これらの署名をグループ化すると、6つの大まかな挙動タイプが浮かび上がりました。飢餓と栄養回復に対して非常に素早く反応する「超感受性」な変異株もあれば、反応が鈍い「低感受性」なものもありました。基礎的な再利用が異常に高い「過活性」群や、そもそも適切な応答を起こせない群も複数ありました。重要なのは、既知のコアオートファジー遺伝子が最も重篤なクラスに入っていたことで、手法が測定ノイズではなく実際の生物学を捉えていることが裏付けられた点です。
オートファジーを支配する階層の地図化
オートファジーは孤立して起こるものではなく、細胞の広い制御ネットワークに組み込まれています。チームは得られた動的プロファイルを、酵母における大規模な遺伝およびタンパク質相互作用の地図に重ね合わせました。喪失が強いオートファジー欠損を引き起こす遺伝子は、これらのネットワーク上で既知のオートファジー「コア機構」に近い位置にある傾向があり、より間接的な制御はより遠くに位置していました。各挙動クラスでどの細胞プロセスが豊富に含まれるかを調べると、飢餓による活性化はRNA、タンパク質合成、エネルギー代謝を扱う経路によって強く形作られる一方、栄養が戻った後のシャットダウンは、再利用小胞をクリアする膜輸送や融合のステップにより強く依存していることが示されました。
小胞の形成とクリアランスの詳細を拡大して観察
オートファジーは主に二つの段階を経て進行します:荷物を詰めた小胞の形成と、それらを分解するために細胞のリサイクリング区画と融合させる段階です。これらの段階を解きほぐすため、研究者たちはニューラルネットワーク内部の「潜在空間」――画像を識別するために圧縮された表現――を解析しました。この内部表現を二次元マップに射影すると、細胞集団が小胞のない領域から多数の自由小胞を持つ領域、そして最終的に小胞がクリアされた領域へと移動する様子が可視化されました。異なる段階で固定された参照変異株と統計的に比較することで、各遺伝子が主に小胞形成、または小胞クリアランス、あるいはその両方に影響するかを定量化しました。この解析により、小胞形成の制御は時間に沿った窒素レベルに対して非常に感受性が高い一方、クリアランス機構は比較的安定しており、しばしば全体の再利用フラックスの主な制限因子であることが示されました。 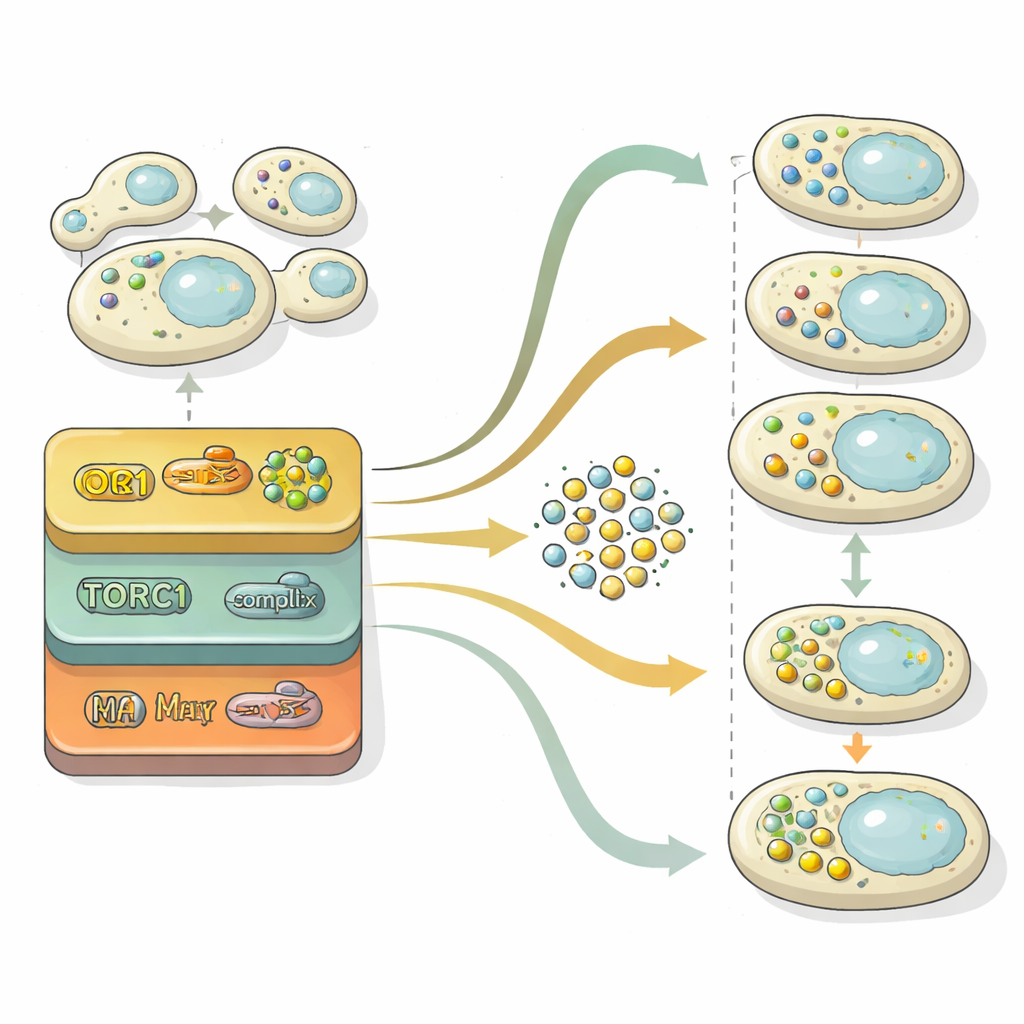
再利用にかけられた隠れたブレーキ:逆行性経路(RTG)
最も注目すべき発見の一つは、ミトコンドリアから核へ信号を伝えるいわゆる逆行性(RTG)経路に関するものでした。RTG構成要素を欠く酵母は、栄養が十分にある状態でも過剰なオートファゴソームを生成し、栄養が戻ってもそれらをうまくクリアできませんでした。追試実験により、この経路は特にマスターイニシエーターであるATG1を含む主要なオートファジー遺伝子の発現を制御しており、ラパマイシンの標的として知られるTORC1栄養センサーとは大部分独立して働くことが示されました。実質的に、RTGシグナルは豊富な条件下で暴走するオートファジーを防ぎ、条件が改善したときに応答を終わらせる時間変動するブレーキとして機能しているのです。
健康と治療にとっての意義
総じて、本研究は栄養条件の変化に応じて細胞がオートファジーをどのように調整するかのゲノムワイドで時間分解能の高い地図を提供します。活性化と終了は鏡像の関係ではなく、再利用の開始に影響を与える遺伝子は停止に影響する遺伝子よりはるかに多く、長期的なバランスは小胞のクリアランスやRTG経路のような転写的ブレーキに大きく依存することが明らかになりました。一般読者にとっての重要な要点は、細胞の自己捕食が層状の階層的制御下にあり、我々が今やこれらの層を高精度で図示できるようになったということです。この種のシステムレベルの見方は、特定のフェーズでオートファジーを調節して有益な再利用を促進しながら、慢性的で制御不能な自己消化の有害な影響を避けるような、より精緻な治療設計に繋がる可能性があります。
引用: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
キーワード: オートファジー, ディープラーニング, 酵母遺伝学, 栄養感知, 細胞の再利用