Clear Sky Science · ja
ワクチン応答の精緻な表現型化が中和抗体の異質性を決めるトランスクリプトームの要因を明らかにする
なぜ同じワクチンでも人によって効き方が違うのか
私たちがCOVID-19の予防接種を受けるとき、多くの人は免疫系が同じように反応すると考えがちです。しかし現実には、どれだけ速く強く防御的な抗体を作るかは人によって大きく異なります。本研究は不活化SARS-CoV-2ワクチンを受けた成人を追跡し、ワクチン応答が明確に異なるパターンに分類され、それぞれが遺伝子発現や血中免疫細胞に記された異なる初期の免疫シグナルに駆動されていることを示しました。こうしたパターンを理解することは、将来的にすべての人が必要な保護を得られるようワクチン接種スケジュールを個別化する手がかりになる可能性があります。
同じ接種で示される保護への三つの経路
研究者たちは不活化COVID-19ワクチンを2回接種した73人の健康な成人を追跡しました。彼らは接種前、2回目接種の1週間後、さらに約1か月後にウイルスを阻止できる中和抗体を測定しました。単純に「高反応」か「低反応」に分けるのではなく、抗体レベルの時間経過に基づいてデータ駆動型の手法で人々をグループ化しました。その結果、三つの明瞭なパターンが現れました。抗体の上昇が遅く控えめな「低・遅延」群、抗体が急速に上昇して安定する「急速・安定化」群、そして抗体が継続的に上昇して最も高い水準に達する「継続的上昇」群です。これらのパターンは年齢、性別、体重では説明できず、接種された不活化ワクチンの製品差でも一部しか説明されませんでした。
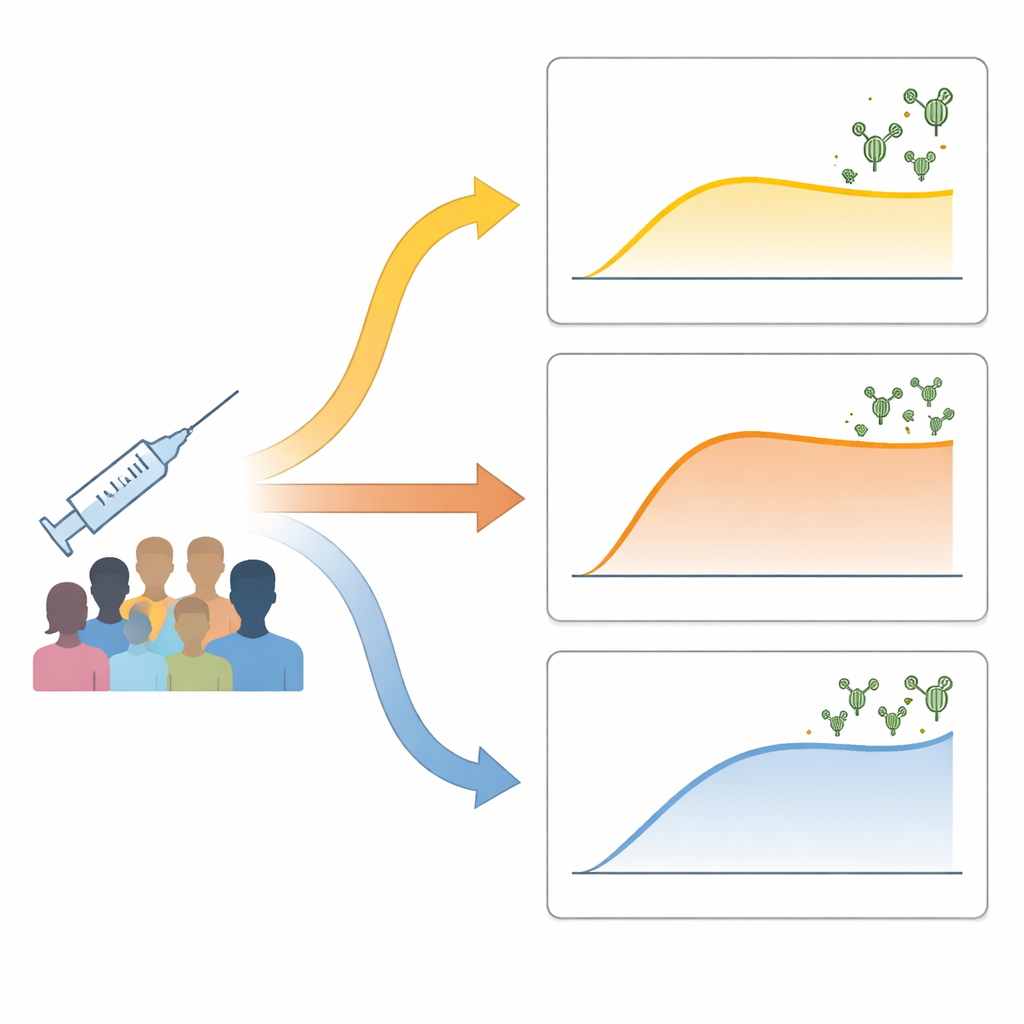
初期の免疫活動が結果をどう形作るか
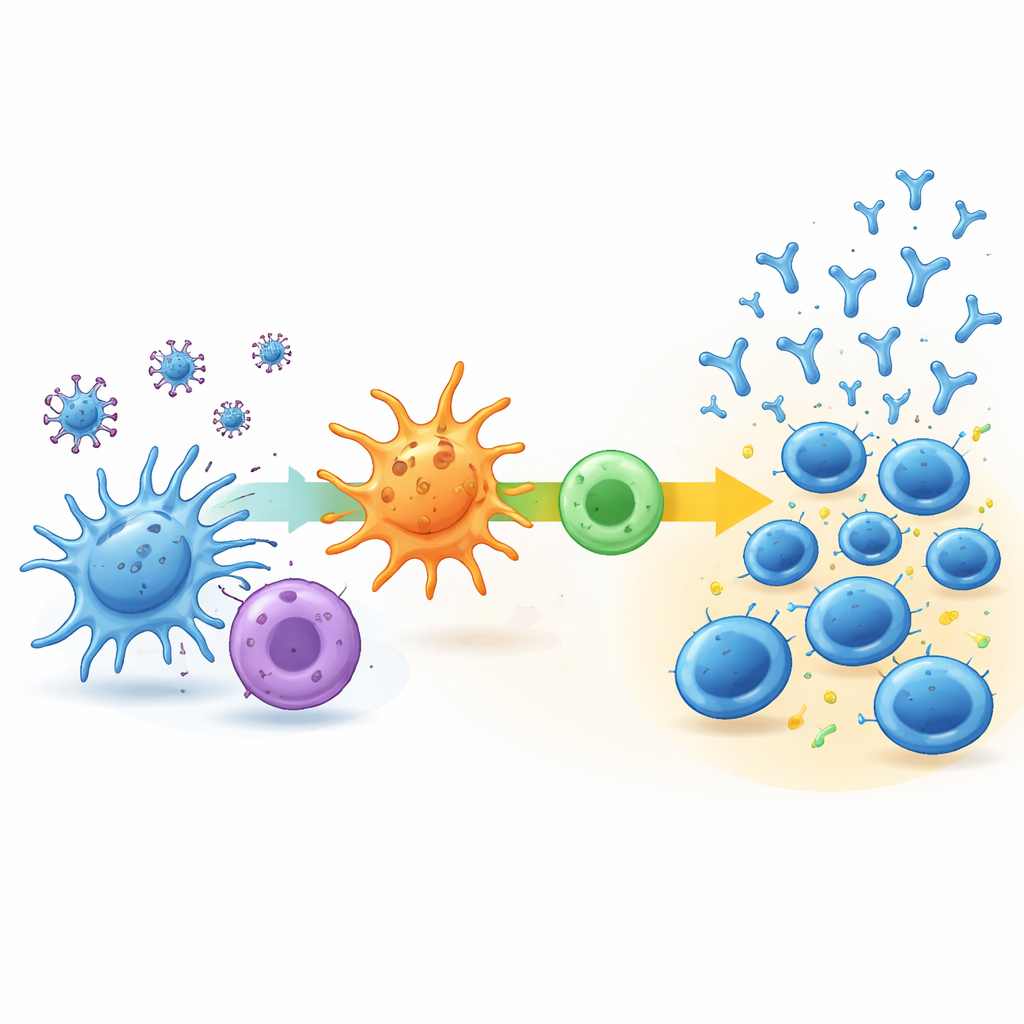
これらの異なる経路を駆動する要因を調べるために、研究チームは血中の免疫細胞の遺伝子発現を、接種開始時と2回目接種の1週間後に解析しました。低・遅延群ではほとんど変化が見られませんでした。主要な免疫経路はほとんど活性化せず、血中の免疫細胞の構成も大きくは変わりませんでした。対照的に、急速・安定化群と継続的上昇群は初期の免疫活性化の明確な兆候を示しました。最も強い応答を示した人々では、ウイルス断片を処理し他の免疫細胞に提示する経路や、抗体産生を促進すると知られるヘルパーT細胞型の応答を支えるネットワークが調和して活動していました。これらの人々はまた、反応準備が整ったナイーブB細胞やヘルパーT細胞が相対的に多く、後にはウイルス特異的なT細胞活性もやや強い傾向が見られました。
RNAとB細胞に潜む制御の層
単純な遺伝子のオン・オフ変化を超えて、研究者たちはDNAとタンパク質の間にある中間分子であるRNAに埋め込まれたより微妙な制御層を調べました。最高応答群では、ウイルス断片を免疫系に提示することに関与する免疫遺伝子が異なる「スプライシング」パターンや短い3'末端領域を示しました。これらの特徴は特定のタンパク質を作りやすくし、強いシグナル維持に寄与すると考えられています。チームは同じ血液サンプルから抗体産生細胞のユニークなアンテナであるB細胞受容体のレパートリーも再構築しました。全体的な多様性は群間で似ていましたが、各応答パターンはわずかに異なる組み合わせや形状の受容体を用いており、最も強い応答者はコロナウイルスのスパイク蛋白に対して強力な抗体と以前に関連づけられた受容体タイプを好む傾向がありました。
接種前に低反応者を見つける
標準的な接種スケジュールの後に十分な保護を得られない可能性がある低・遅延群を事前に特定できるかを研究者たちは検討しました。彼らは弱い応答者と強い応答者の間でベースラインでわずかに差があった少数の遺伝子に着目しました。機械学習の手法を用い、接種前に測定されたわずか8遺伝子の発現に基づくモデルを構築しました。このモデルはデータセット内で低・遅延応答者を高い精度で識別でき、基本的な細胞シグナル伝達と炎症に関与する2つの遺伝子が予測力の大部分を担っていました。もっと大規模で多様な集団で検証する必要はありますが、単純な血液検査が将来より個別化されたワクチン計画を導く可能性を示唆しています。
今後のワクチンにとっての意義
総じて、本研究は人々が単に「強い」か「弱い」抗体応答を示すのではなく、初期の目に見えにくい免疫イベントによって形作られた異なる時間経過をたどることを示しています。最も保護を受ける個人はワクチンを素早く認識して耐久性のある抗体を構築するための遺伝子と細胞の協調したネットワークを立ち上げる一方で、低反応者は初期反応が抑制されています。こうした内部の違いをマッピングし、反応が乏しい人を予測するツールを構築することで、早めのブースターやリスクの高い人向けの代替製剤など、個別化された接種戦略の基盤が整い、ワクチンの恩恵をより公平に広げる道が開かれます。
引用: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
キーワード: ワクチン応答, 中和抗体, COVID-19 ワクチン接種, 免疫の異質性, 個別化ワクチン