Clear Sky Science · ja
抗原の交差提示を強化するがんワクチン用アジュバント:T細胞の増強と抗PD-1との相乗効果
免疫系を精密な腫瘍攻撃機に変える
がんワクチンはしばしば免疫系に腫瘍を認識して破壊するよう「教育する」ものと説明されますが、実際にはその約束を果たすことはまれでした。本研究は、こうしたワクチンを“超強化”して、より強力で持続的なキラーT細胞を生み出し、抗PD-1のような一般的な免疫療法薬とより良く協調して働く新しい手法を検討しています。生物学的薬剤、ワクチン、免疫工学を組み合わせた明日のがん治療に関心のある読者に対し、次世代の高精度免疫療法がどのような姿を取るかを垣間見せる内容です。
なぜがんワクチンはより強力な支援を必要とするのか
治療目的のがんワクチンは病気の予防ではなく、既に腫瘍を有する患者を治療することを目指し、強力で腫瘍特異的な免疫応答を誘導します。主役はCD8の“キラー”T細胞で、腫瘍細胞が示す特徴的な抗原を認識して破壊できます。しかし残念ながら、腫瘍抗原は体内の自己タンパク質の変化型にすぎないことが多く、刺激性が弱いのです。がんの発生過程での持続的な暴露はT細胞を疲弊や寛容状態にし、ワクチンの効果を鈍らせます。これを克服するために、ワクチンはアジュバント――自然免疫を活性化し、抗原提示を改善し、大きく回復力のある腫瘍特異的T細胞プールを構築する補助成分――と組み合わせる必要があります。
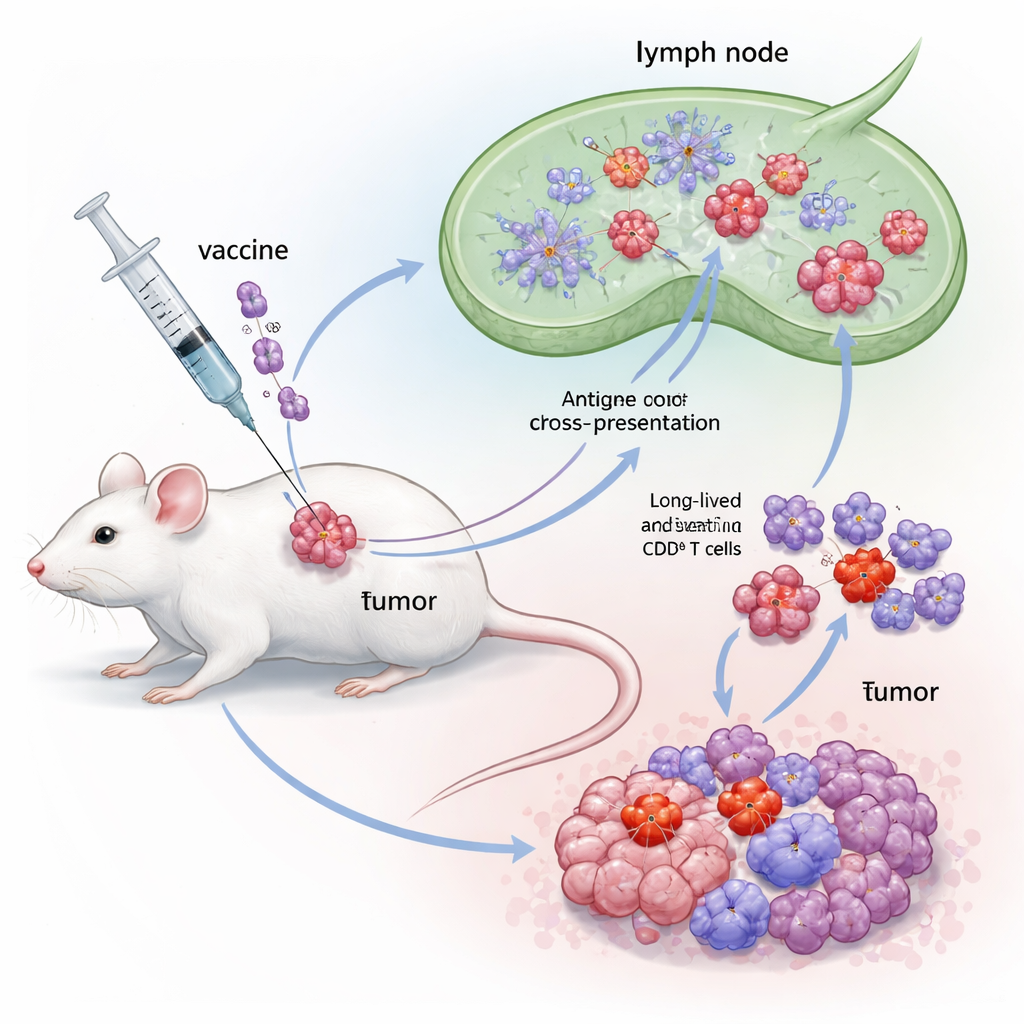
二つの強力なシグナルを融合したハイブリッド免疫増強剤
研究者たちはFlt3LとFlaBという二つの免疫賦活分子を単一タンパク質に融合して、Flt3L-FlaB(略してFB)というハイブリッドアジュバントを設計しました。片方のFlt3Lは樹状細胞、特にcDC1と呼ばれる特殊な集団を拡大する天然の増殖因子です。cDC1は「交差提示」に長けており、腫瘍由来の断片を取り込みCD8 T細胞に提示して強い応答を誘導します。もう片方のFlaBは細菌の鞭毛タンパクフラグメントで、TLR5という自然免疫センサーを活性化し強力な危険信号として作用します。これらを連結することで、cDC1を増やすだけでなくそれらを高活性状態へ切り替え、腫瘍抗原の提示とその持続性を改善することを狙いました。
腫瘍モデルで新アジュバントを検証する
FBを検証するため、チームはヒトパピローマウイルス(HPV)由来の発がんタンパク質を運ぶよう設計された細胞を用いる確立されたマウス腫瘍モデルを使用しました。マウスにはまず小さな腫瘍が移植され、その後HPV E7抗原を含む治療用ワクチンが投与され、併用するのはFlt3L単独、FlaB単独、あるいは新しいFB融合体のどれかでした。すべてのワクチンは腫瘍近傍に投与されました。各単独アジュバントも腫瘍増殖をやや遅らせましたが、FBベースのワクチンは際立っていました:腫瘍進行をはるかに遅延させ、生存期間を有意に延ばし、かなりの割合のマウスで完全な腫瘍消失をもたらしました。免疫解析では、FBワクチン接種が血中、リンパ節、脾臓において異常に強いE7特異的CD8応答を誘導し、高レベルのインターフェロン-ガンマと頑健なT細胞増殖を示しました――融合体は単に両成分の効果を足し合わせただけでないことを示す証拠です。
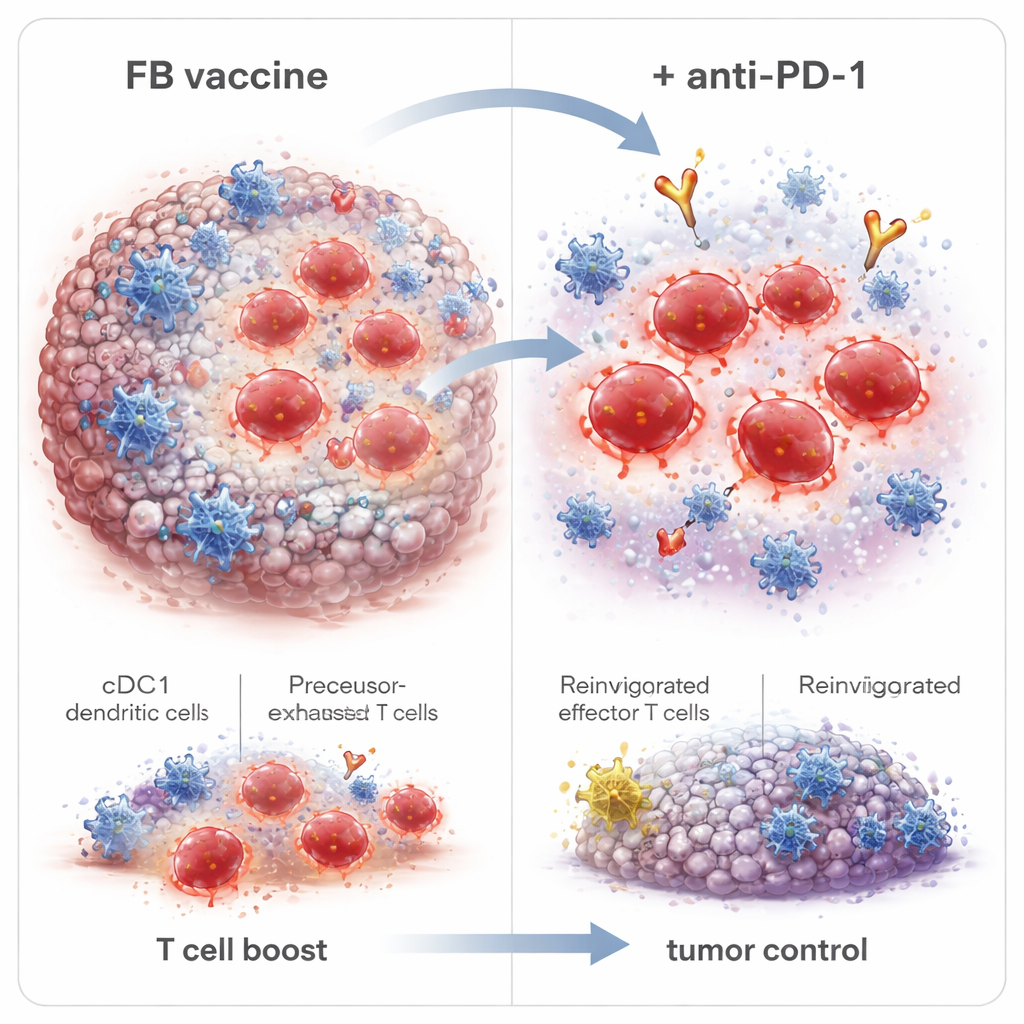
持続する免疫記憶の構築と抗PD-1のより良いパートナー
さらに掘り下げると、FBは単に出現するCD8 T細胞の数を増やすだけでなく、その質も変えていました。即座に腫瘍を攻撃する短命のエフェクター細胞に加え、将来にわたって持続し再応答できるメモリー前駆および幹様メモリー細胞を増強しました。重要なのは、FBが腫瘍内で前駆疲弊(Tpex)T細胞と呼ばれる集団を拡大した点です。これらの細胞は疲弊と活動の境界に位置し、抗PD-1薬に特に反応しやすいとされています。ワクチン後長期にわたり腫瘍消失した個体を高用量のがん細胞で再チャレンジしたところ、大部分が再増殖を防ぎ、持続的な免疫記憶を示しました。リンパ節からの免疫細胞の放出を遮断するとFBの利点は消失し、腫瘍を殺すT細胞はcDC1によってリンパ節で樹立されそこから腫瘍へ移動することが示唆されました。
より強力な組み合わせ:ワクチンとチェックポイント遮断
抗PD-1療法は既に反応性のあるT細胞プールが存在する場合に最も効果的なため、チームはFBアジュバントワクチンと抗PD-1抗体を併用しました。HPV腫瘍モデルでは、FBワクチンに抗PD-1を追加すると腫瘍増殖の遅延がさらに進み、完全に癌を消失したマウスの割合が増え、極めて高用量の腫瘍再チャレンジに対しても完全な防御を提供しました。タイミングの調整が重要で、抗PD-1を1回目ではなく2回目のワクチン投与後に開始すると完全根絶がわずかに改善し、これはTpex細胞が拡大するまで待つことの利点と一致します。FBアジュバントはペプチドベースワクチン、例えば結腸がんモデルの腫瘍特異的ネオアンチゲンに対しても応答を改善し、この戦略がHPV関連疾患に限らず広く応用可能であることを示唆しています。
将来のがん医療にとっての意義
非専門家向けに言えば、本研究の要点は免疫系にがんと戦う方法を“教える”やり方を洗練したことにあります。樹状細胞の増殖因子と強力な危険信号を一つの安定したタンパク質に組み合わせることで、FBアジュバントは適切な抗原提示細胞を増やし、腫瘍抗原の提示をより効果的にし、現在強力でありながら後のチェックポイント療法にも応答可能なキラーT細胞集団を形成します。これらの結果はマウスで得られたものであり、人での使用には多くの段階が残されていますが、本研究は明確なロードマップを示します:交差提示とT細胞の幹様性を調整する賢いアジュバントにより、治療用がんワクチンは抗PD-1のような薬剤とより強力なパートナーになりうる――患者でより深く、長期の腫瘍制御につながる可能性があるのです。
引用: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
キーワード: がんワクチン, 免疫療法, 樹状細胞, PD-1遮断, HPV関連腫瘍