Clear Sky Science · ja
人工抗体に触発されたヒトコロナウイルスのための普遍的広域粘膜ワクチン設計
なぜより良いコロナウイルスワクチンが依然重要なのか
COVID-19が季節性の感染症へと移行しつつある一方で、新たな変異株の波は繰り返し現れ、他の複数のヒトコロナウイルスも依然として重篤な疾患を引き起こしています。現行ワクチンは重症化予防に有効ですが、特にウイルスが最初に定着する鼻や咽頭などの部位で、感染や伝播の阻止には限界があります。本研究は、設計された抗体に着想を得た新しいタイプの鼻噴霧ワクチンを示し、粘膜という第一防御線で多くのコロナウイルスに対して広範かつ長期の保護を目指しています。
より賢いワクチン足場の構築
研究者たちは既知の分子、すなわちヒトIgG1(多くの承認済み抗体医薬で使われる主要な抗体タイプ)を出発点としました。彼らはその重鎖を再設計し、ウイルスが細胞に結合する部位であるスパイクタンパク質受容体結合ドメイン(RBD)を提示するための柔軟な「足場」として機能させました。通常の軽鎖を除去し、特定の変異を導入することで、サイトカインストームのような副作用に関連する免疫受容体への結合を減らしつつ、新生児Fc受容体(FcRn)への結合を強化しました。FcRnは粘膜表面に豊富に存在し、抗体をバリアを越えて運搬し、抗体の持続性を高める役割があります。この最適化された骨格に、SARS、MERS、季節性コロナウイルス、ならびにオミクロン系統を含む複数のSARS-CoV-2変異株からの1〜4種類のRBDを結合させ、モノ、バイ、トリ、テトラバレントのワクチン候補を作製しました。
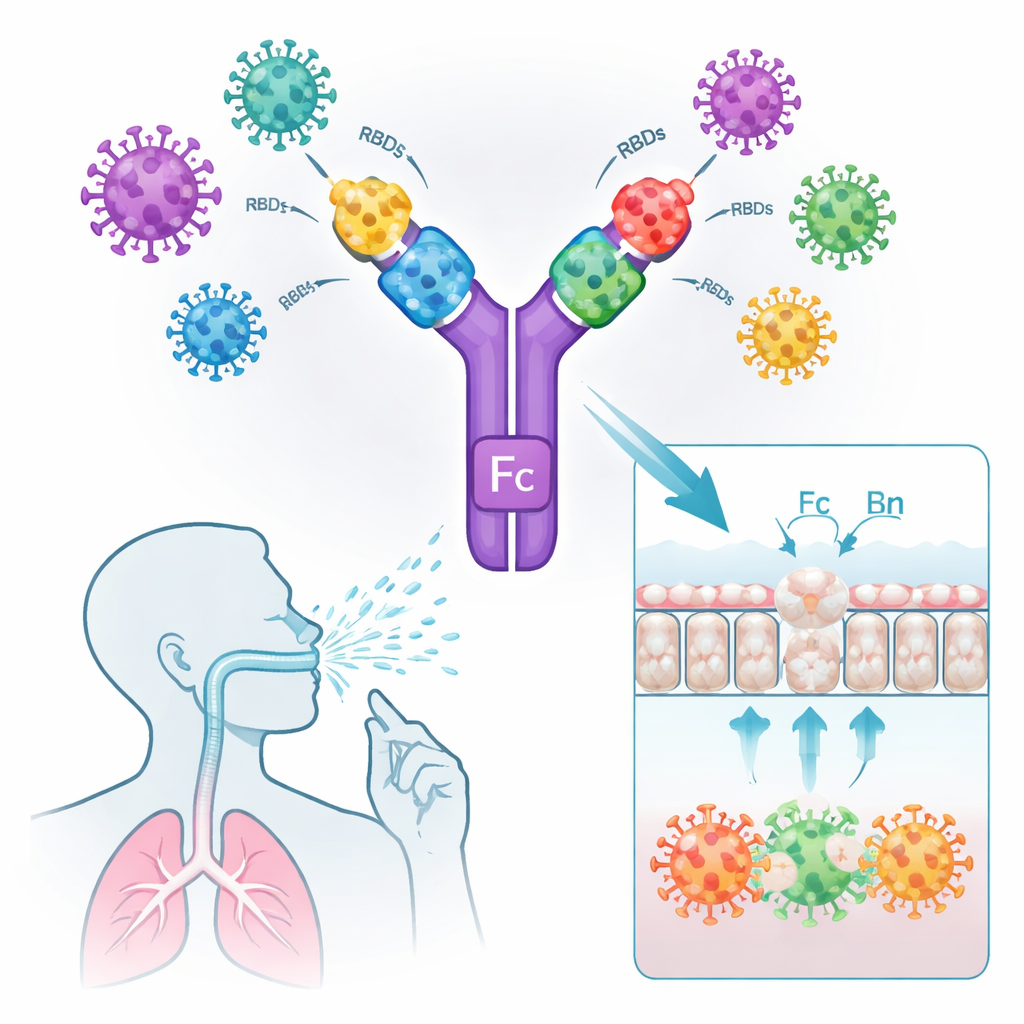
粘膜バリアを越え局所防御を活性化する
鼻スプレーとして機能するには、ワクチン抗原が気道上皮に到達して留まり、免疫細胞に効率よく認識される必要があります。細胞培養系では、Fcをもつ構成体はACE2(SARS‑CoV‑2の侵入受容体)およびヒト・マウスのFcRnに強く結合し、粘膜細胞層を能動的に横断しました。Fcを欠く同等のRBDダイマーは横断に失敗しました。ワクチンの蛍光標識版をマウスの鼻腔に投与すると、Fc含有の抗原は肺粘膜に数時間残存した一方で、裸のRBDダイマーは速やかに消失しました。顕微鏡観察では、Fc修飾ワクチンが粘膜下の抗原提示細胞を引き寄せ活性化し、免疫マーカーCD80の増加やFcRnとの共局在が示されました。
必要な場所で抗体とT細胞を増強する
次に、研究チームはマウスに対して筋注と鼻腔投与を比較しました。いくつかの製剤において、Fcベースのワクチンは原型SARS‑CoV‑2株およびオミクロンXBB.1.5に対する血中IgG抗体を非常に高レベルで誘導しました。特に、現代的なSTINGアゴニスト(CF501)を用いたアジュバントと併用した鼻腔投与は、血中だけでなく鼻分泌物や肺洗浄液中においても強力なIgA応答を生み、粘膜保護が最も重要な部位での防御を際立たせました。Fc含有の構成体はまた、裸のRBDダイマーより強力な細胞性免疫を誘導し、ヘルパーT細胞、キラーT細胞、および肺における長寿命の組織常在メモリーT細胞を拡大しました。これらの細胞型は呼吸器ウイルスの排除や脳などの感受性の高い臓器への拡散防止に重要と考えられています。
多くの変異株と種に対する広域保護
中心的な試験は、原型ウイルスとオミクロンXBB.1.5のRBDを組み合わせた二価ワクチン(XBB.1.5 + PT‑Fcと呼ばれる)が、複数のウイルス挑戦から動物を保護できるかどうかでした。ヒトACE2を発現するマウスに低用量の鼻腔投与を2回行うと、この候補は強力な中和抗体を誘導し、原型ウイルスおよびXBB.1.16による致死感染から完全に動物を保護しました:ワクチン接種マウスは体重を維持し生存し、脳、肺、鼻組織にウイルスは検出されませんでしたが、対照群は発病し死亡しました。同じワクチンは、ベータ、デルタ、いくつかのオミクロン亜系統を含む主要変異株に対する病気と死亡も阻止しました。ハムスター(伝播研究に適したモデル)では、接種動物は直接挑戦後のウイルス量が劇的に低く、共飼育実験では空気伝播から概ね保護されました。マウスとハムスターの両方で、抗体レベルとメモリーT細胞は少なくとも48週にわたり高水準を維持し、接種からほぼ1年後の致死的挑戦に対しても動物は完全に保護されていました。
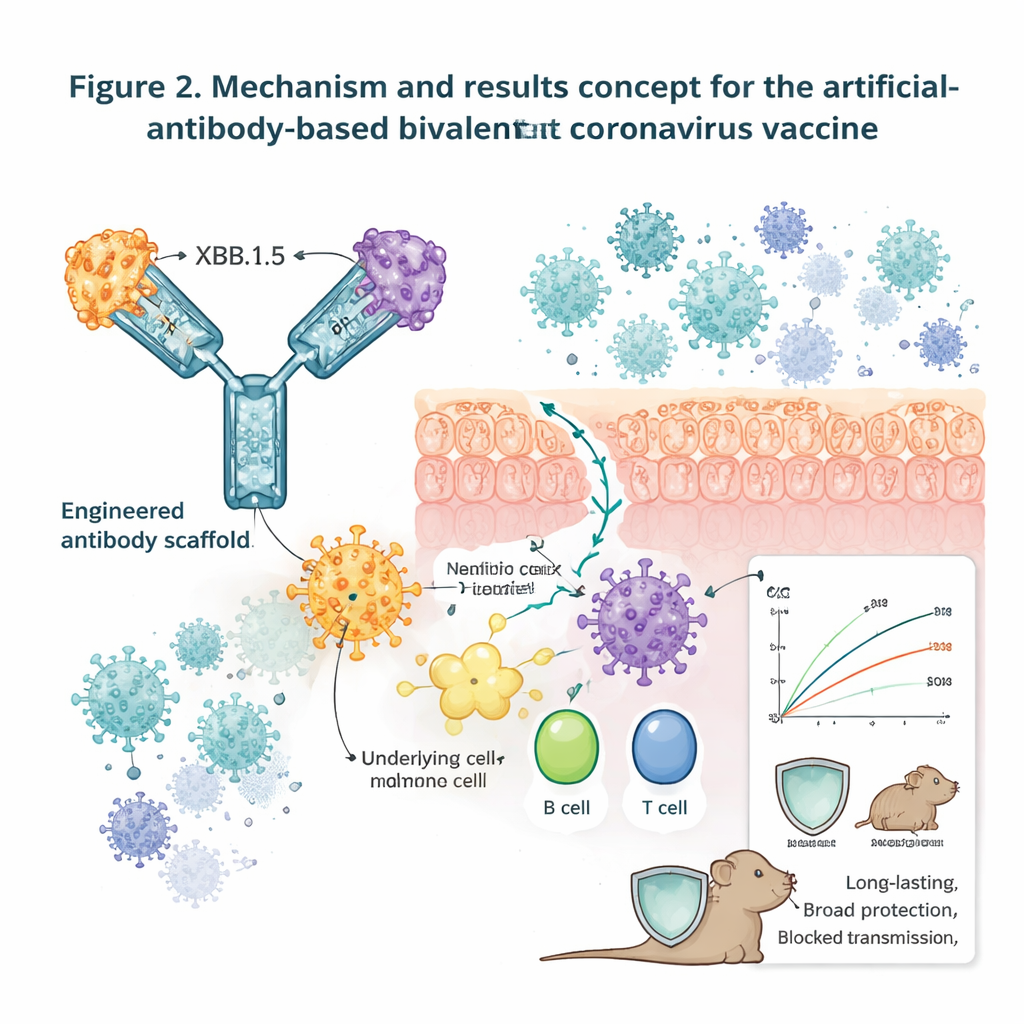
普遍的なコロナウイルス鼻スプレーに向けて
最後に、研究者らはプラットフォームを本当に普遍的な設計へと押し進めました。彼らはSARS‑CoV‑2、SARS、MERS、および複数の季節性コロナウイルスをカバーするいくつかの二価構成体を混合し、さらに単一の足場上に4つの異なるRBDまたはスパイク断片を載せたテトラバレント分子も作製しました。これらの組み合わせは広範なヒトコロナウイルスパネルを認識する抗体を上昇させ、マウスの挑戦実験では、流行性ウイルス(NL63を含む)を含む複数の代表株でウイルス量を低下させました。よりヒトに近いモデルや最終的な臨床試験でのさらなる評価は必要ですが、本研究は設計された抗体骨格が多様なコロナウイルス抗原を安全に鼻腔バリアを越えて運び、強力な局所および全身免疫を刺激し、広範かつ持続的な保護を提供し得ることを示しています。専門外の読者に向けた要点は、将来の「普遍的」コロナブースターは必ずしも注射ではなく、多くの医薬で既に安全性が示された同じ抗体フレームワークに基づく穏やかな鼻スプレーである可能性がある、ということです。
引用: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
キーワード: 鼻腔内ワクチン, 広域コロナウイルス, 粘膜免疫, 人工抗体足場, SARS-CoV-2変異株