Clear Sky Science · ja
ヘテロログス免疫はMPER/リポソームワクチンにおけるヘルパーペプチドとMPERセグメント間のB細胞エピトープ競合を調節する
このHIVワクチン研究が重要な理由
効果的なHIVワクチンの設計は極めて困難であり、その一因はウイルスが急速に変異し、免疫系から最も脆弱な部分を隠すことにあります。本研究は、MPER領域と呼ばれるそのような隠れた弱点に免疫を向けさせる巧妙な方法を検討しています。具体的にはMPERをリポソームと呼ばれる小さな脂質の泡に包み、接種ごとに“ヘルパー”成分を変えるという手法です。マウスを用いた研究であり、まだ実用的なワクチンが得られているわけではありませんが、希少で保護的な抗体を誘導しやすくし、注意をそらす標的から遠ざけるための実践的なルールを明らかにしています。
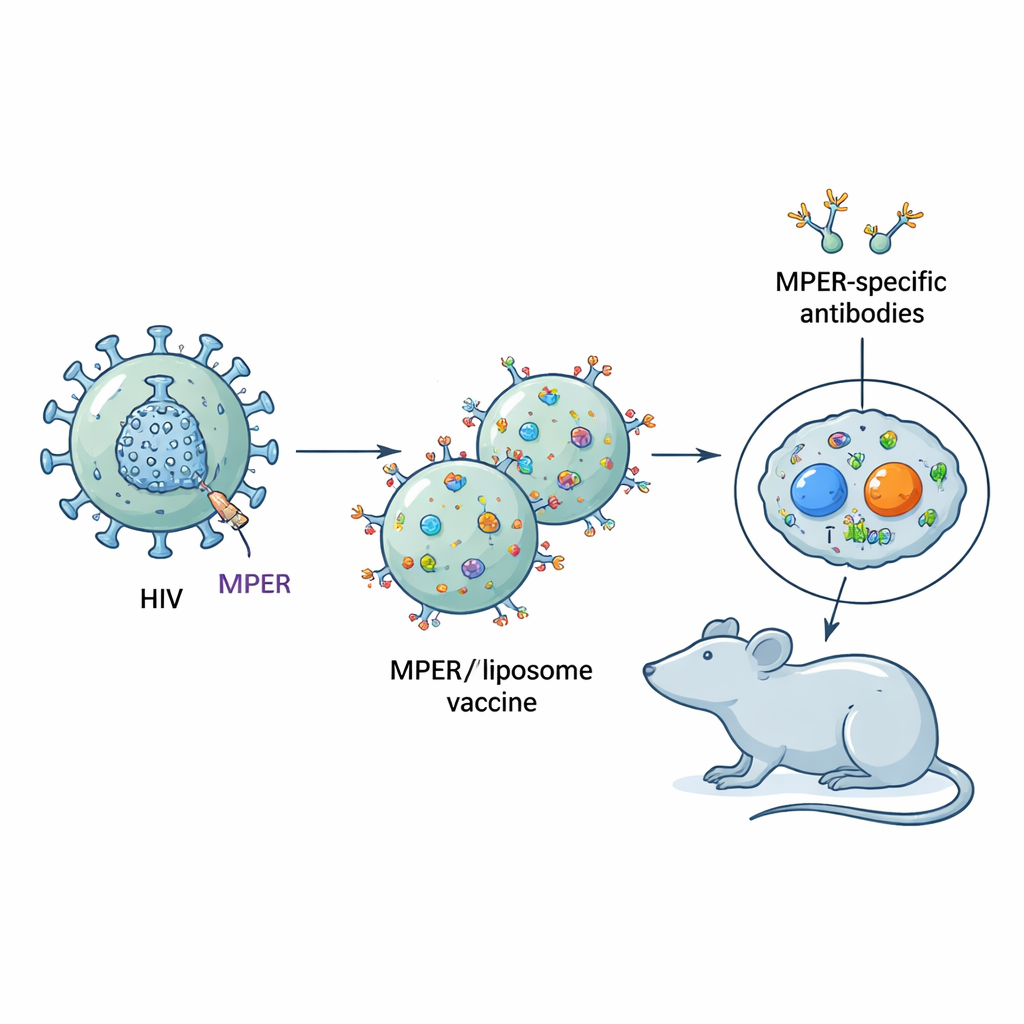
ウイルスの隠れた弱点
HIVは突起のあるタンパク質被膜に覆われており、これらの突起を使って細胞へ侵入します。突起の多くの部分は容易に変異し、抗体の回避を助けます。対照的に、突起タンパク質の基部近くに位置する短い領域、膜近接外部領域(MPER)はHIV株間で高度に保存されており、長期感染者の一部に見られる非常に強力な中和抗体に認識されます。しかしMPERはウイルス膜に隣接しており部分的に埋もれているため、B細胞(抗体を作る細胞)は感染時や標準的なワクチン接種後にこれを十分に認識しづらいという問題があります。
MPERを小さなワクチン粒子で模倣する
研究者らは合成MPER断片をリポソーム表面に高密度に固定化したワクチンを構築し、MPERがウイルス上に見える環境により近づけました。同じリポソームの内部または付随に、CD4 T細胞に認識される短い“ヘルパー”ペプチドも含めました。これらのヘルパーT細胞は、抗体産生細胞が競合し、変異して結合を改善する免疫系の訓練場である胚中心においてB細胞を支援するのに不可欠です。重要なひねりとして、LACKと呼ばれるペプチドのように、いくつかのヘルパーペプチド自身が強いB細胞標的であり—つまりそれ自体に対して容易に抗体ができてしまい—MPERから注意を奪ってしまう可能性がある点が挙げられます。
有益な標的と気を散らす標的の競合
マウスにMPERをリポソームに乗せ、LACKヘルパーペプチドと一緒に初回接種を行うと、免疫系はLACKに対して強い応答を示した一方で、MPERに対しては弱く低親和性の応答しか示しませんでした。胚中心B細胞と抗体結合の測定は、LACK特異的B細胞が内在的な親和性上の有利さを持ち、T細胞の支援を巡ってMPER特異的B細胞に勝って抗体応答を支配していることを示しました。これは、MPERを強調することを意図したワクチンであっても、技術的理由で付加されたヘルパーペプチドのようなオフターゲットエピトープが免疫学的な“注目の奪取者”になり、望ましい応答を損ね得ることを示唆します。
免疫系を再焦点化するミックスアンドマッチブースターの利用
次に研究チームは、後の接種でMPERの形態とヘルパーペプチドの同定を変更する“ヘテロログス”なプライム–ブースト法を試しました。MPER/LACKでプライミングした後、いくつかのマウス群は異なるMPER構築体に入れ替え、LACKをB細胞標的としてそれほど優勢でない代替のヘルパーペプチド(HIV30やOVA)に置き換えるブースターを受けました。これらのミックスアンドマッチブースターは骨髄中のMPER特異的長期在住形質細胞を著しく拡大し、MPER抗体の量と結合強度を増加させる一方でLACKに対する抗体を減少させました。詳細なマッピングにより、これらのレジメンが抗体を特定のMPER残基へとシフトさせ、細胞表面の全長HIV Envタンパク質への結合を改善したことが示されました。これは広範な中和にはまだ至っていないものの、実際のウイルスを認識する方向への重要な一歩です。
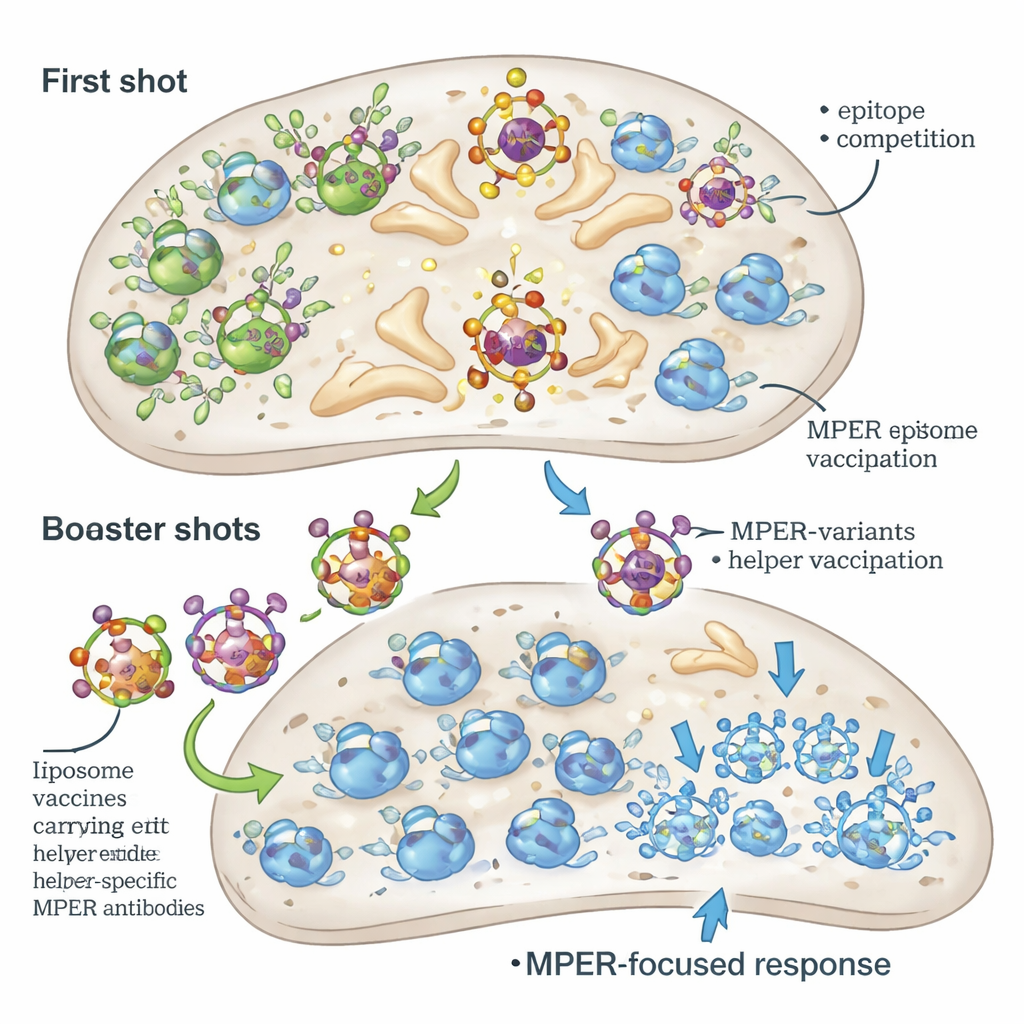
支援と競合のバランス
興味深いことに、最も有益だったブースト戦略は単に全体として最も大きなTヘルパー応答を生んだものではありませんでした。LACKを使い続けたブーストは強い胚中心活性を生んだものの、それでもLACK特異的B細胞をMPERよりも優先しました。対照的に、代替ヘルパーペプチドを用いたブーストは全体としてやや弱いT細胞ヘルプを提供しましたが、MPER特異的B細胞とヘルパーペプチド特異的B細胞間の親和性ギャップを狭め、MPER標的の細胞がより成功裏に競合できるようにしました。ヘルパーペプチドが単に封入されるのではなくリポソーム表面に固定化された場合、圧倒的なB細胞標的になることなく強固なT細胞ヘルプを提供し、MPER抗体の親和性をさらに改善しました。
今後のHIVワクチンにとっての意味
一般読者にとっての主なメッセージは、ワクチンはウイルスの弱点を認識させるだけでなく、それを他の多くの誘惑的な標的よりも優先させるように免疫系を訓練しなければならないということです。本研究は、接種間でヘルパー成分を慎重に選択・入れ替え、ナノ粒子上で抗原の表示方法を調整することにより、気を散らす反応を抑え、保存されたMPER領域に対する希少で望ましい反応を増幅できることを示しています。ここで得られたマウス抗体は依然として広範なHIV中和能を示していませんが、本研究は今後のHIVワクチンや急速に変化するウイルスに対する他のワクチンのための具体的な設計原則を示しています:エピトープ競合を制御し、ブースターを戦略的に変化させ、スマートな免疫原デザインと同等に賢い免疫スケジュールを組み合わせること。
引用: Khan, R.A., Chen, J., Donius, L. et al. Heterologous immunization modulates B-cell epitope competition between helper peptides and the MPER segment in MPER/liposome vaccines. npj Vaccines 11, 51 (2026). https://doi.org/10.1038/s41541-026-01371-6
キーワード: HIVワクチン, MPER抗体, リポソーム免疫, ヘテロログスブースト, B細胞エピトープ競合