Clear Sky Science · ja
Spatial FBAは腎腫瘍における不均一なワールブルグニッチと結腸直腸がんにおける乳酸消費を明らかにする
腫瘍代謝を空間で見ることが重要な理由
同じ腫瘍内でもがん細胞は均一に振る舞うわけではありません。血管に近い場所にいる細胞もいれば、栄養が乏しい深部にいる細胞もあり、そうした位置が燃料の取り込み方や利用の仕方に影響を与えます。本研究は、最新の空間的遺伝子発現データからその隠れた「代謝マップ」を読み取る新しい方法を提示します。これにより、さまざまな腫瘍が重要な分子である乳酸を扱う意外なパターンが明らかになり、がんが乳酸を単に廃棄するだけだという従来の見方に挑戦しています。
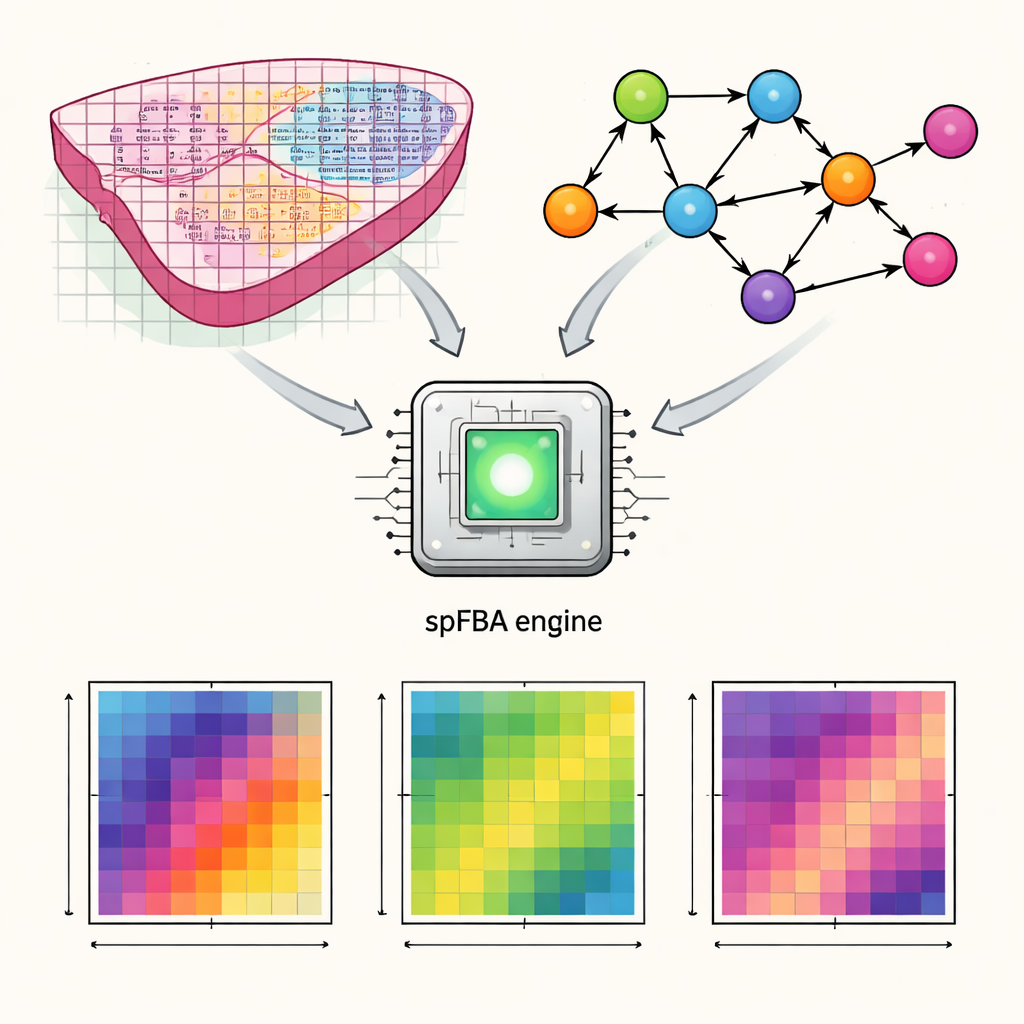
遺伝子マップを代謝活動に変換する
著者らはspatial Flux Balance Analysis、略してspFBAと呼ばれる計算フレームワークを開発しました。空間トランスクリプトミクス技術は、組織の薄切片にわたる数千の微小スポットでどの遺伝子が活性化しているかを測定します。spFBAはこれらの空間的な遺伝子活動マップを、人間の代謝の詳細なモデルと組み合わせます。これらのモデルは、グルコース、酸素、アミノ酸などの栄養素が細胞内でどのように変換されるかを記述します。組織のすべての領域が同じ代謝目標を共有していると仮定する代わりに、spFBAは各スポットを独立して扱い、化学と質量保存の法則の下でどのような反応パターンが可能かを探索します。出力は各位置について、どの代謝反応がどの程度の強さで流れ、どの方向に向かう可能性があるかを示す「フラックス濃縮スコア」の集合です。
腎腫瘍での方法の検証
spFBAが生物学的に妥当な結果を出すかを確かめるため、研究チームはまず透明細胞型腎細胞癌(clear cell renal cell carcinoma)に取り組みました。これは糖分解(解糖)と乳酸放出に強く依存することで知られる腎がんで、ワールブルグ効果の代表例です。10検体の公開空間データを用いて、予測された代謝パターンが組織の既知の構造と一致するかを検証しました。スポットを推定された代謝フラックスでグループ化すると、顕微鏡で見える組織学的構造や遺伝子発現だけに基づくクラスタとよく一致しました。重要なのは、spFBAが腫瘍と正常腎組織の間に予想される代謝コントラストを再現したことです:腫瘍領域はより高いグルコース利用、強いバイオマス生成(細胞増殖の指標として)、および顕著な乳酸分泌を示しました。同時に酸素利用もかなり残っており、同一腫瘍の異なる部位が局所的な血流状況に応じて発酵と呼吸を混在させうることを示しています。
結腸直腸がんで示された異なる乳酸像
研究者らは同じ解析パイプラインを、原発性の結腸直腸がんとそれに一致する肝転移からの高解像度空間データセット、および別技術で生成された公開の独立結腸直腸データにも適用しました。ここで得られた結果は著しく異なっていました。乳酸を廃棄物として放出するのではなく、ほとんどの結腸直腸がん領域—原発腫瘍と肝転移の双方—は周囲から乳酸を取り込むと予測されました。近傍の支持組織にいる間質細胞は少量の乳酸を放出する傾向があり、腫瘍細胞は強い消費者として振る舞っていました。反応レベルのフラックスパターンを追跡することで、著者らはこれらの転移細胞が単にミトコンドリア内の通常のエネルギー産生サイクルで乳酸を燃やしているわけではないことを示しています。むしろ、乳酸を脂質など細胞増殖に必要な成分を作る経路へ供給する原料に変換しており、乳酸を生合成用の原料に変える「疑似逆ワールブルグ効果」と言える振る舞いを示しています。
代謝ニッチと腫瘍-間質の境界
spFBAは空間的配置を保持するため、特定の代謝交換がどこで起きているかを特定できます。腎腫瘍では、この手法は共存する代謝上の「近隣領域」を明らかにしました:酸素供給が比較的良好で血流の豊かな境界部ではがん細胞が呼吸と発酵の両方を行い、より深部で血管が乏しいコアでは発酵により依存する、という対照です。結腸直腸肝転移では、腫瘍と間質の境界でグルタミン酸や乳酸の取り扱いが方向を変える鋭いコントラストが強調され、浸潤前線で激しい交換が起きていることを示唆しました。すべてのデータセットを通じて、予測された増殖関連フラックスは増殖を示す独立した遺伝子ベースの指標と相関しており、モデルの生物学的現実性を支持しています。重要な点は、同じアルゴリズムが腎がんでは乳酸分泌を、結腸直腸がんでは乳酸取り込みを予測したことで、観察された違いがモデルの固定的なバイアスではなくデータに由来することを示している点です。
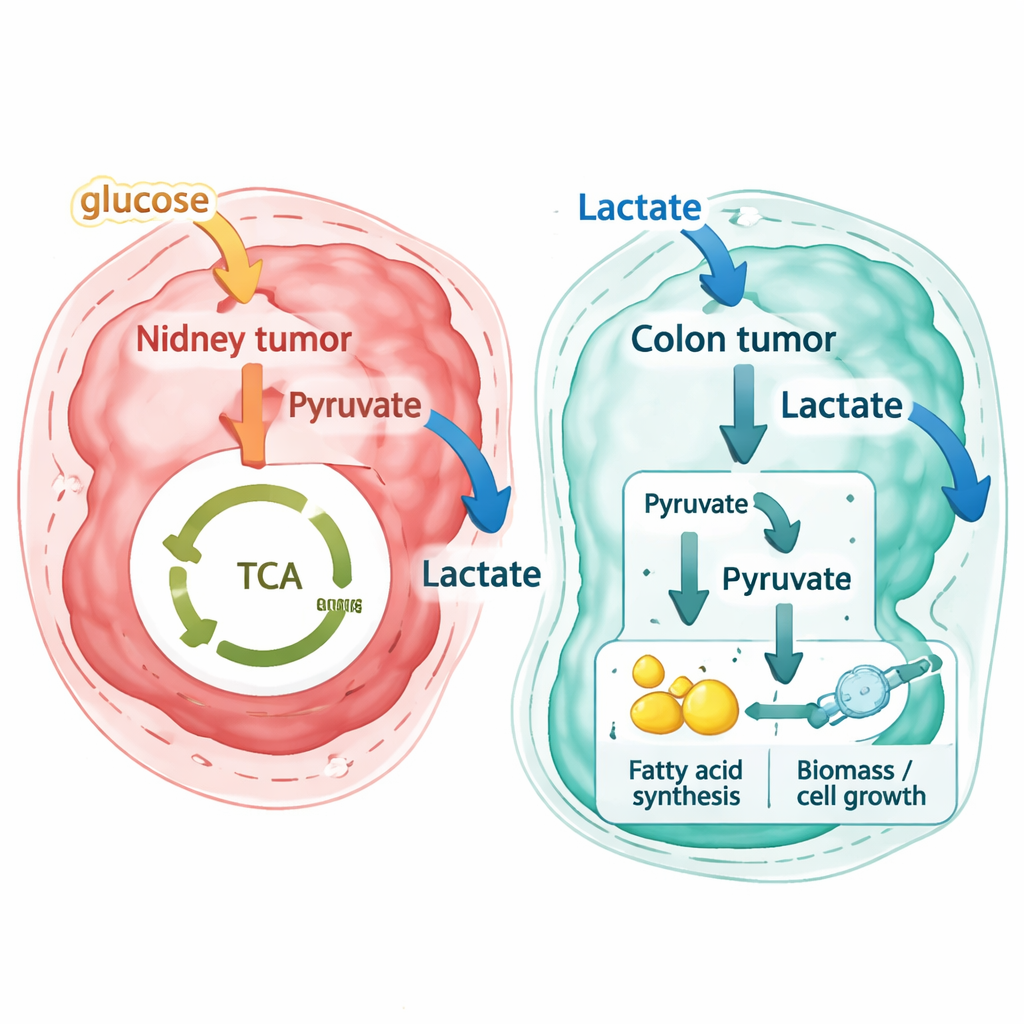
がん理解と治療への示唆
専門外の読者への要点は、がん代謝が単に異常であるだけでなく、非常に局所的であるということです。同一腫瘍内に複数の代謝ニッチが存在し、似た外見の腫瘍でも臓器によって同じ分子を逆に使うことがあります。本研究は、空間的な遺伝子発現を詳細な代謝モデルに重ねることで、腫瘍がどこで特定の栄養素(例えば乳酸)を強く必要としているかを推定できることを示しました。結腸直腸がんで腫瘍細胞が乳酸を大規模に消費し、それを増殖関連のプロセスに回しているという発見は、食事、腸内微生物、肝臓自身の代謝が疾患進行にどう影響するか、あるいは乳酸の利用を遮断することがこれらの腫瘍を治療に対してより脆弱にできるかどうかといった新たな疑問を投げかけます。
引用: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
キーワード: がん代謝, 空間トランスクリプトミクス, 乳酸, ワールブルグ効果, 結腸直腸がん