Clear Sky Science · ja
動的ネットワーク解析は、強化された免疫原性の根底にあるpMHC界面での長距離残基結合を明らかにする
ごく小さなウイルス断片がいかに免疫防御を導くか
キラーT細胞は感染やがんの兆候を探して体内を巡回しています。彼らはMHCクラスIとして知られる分子が細胞表面に提示するペプチドと呼ばれる微小なタンパク質断片をスキャンすることでこれを行います。本研究は微妙だが重要な問いを投げかけます:こうしたペプチドの一か所にあるほんの小さな変化が、なぜT細胞の反応を大幅に強めたり、逆にほとんど反応させなくしたりするのか?答えは静的な構造だけでなく、分子複合体全体が時間を通じてどのように動き、たわむかに関わっていることがわかります。
鍵と錠前、そして動く部品たち
本研究を理解するには、ペプチド–MHC(pMHC)複合体を錠前、T細胞受容体(TCR)を鍵と想像するとわかりやすいでしょう。ペプチドはMHC分子の溝に収まり、両者でTCRが探る表面を形成します。これまでの研究は、正確なペプチド配列と特定のMHC変異型の両方がT細胞が反応するかどうかを強く左右することを示してきました。研究者たちは免疫応答を調整するために小さな変化を持つ「変化ペプチドリガンド」を設計してきており、がん免疫療法でも応用されています。しかし、これら複合体の静的な形状については多くが分かっている一方で、ペプチドのある点での運動がTCRが実際に結合する界面の離れた部分にどのように影響するかについてはほとんどわかっていません。
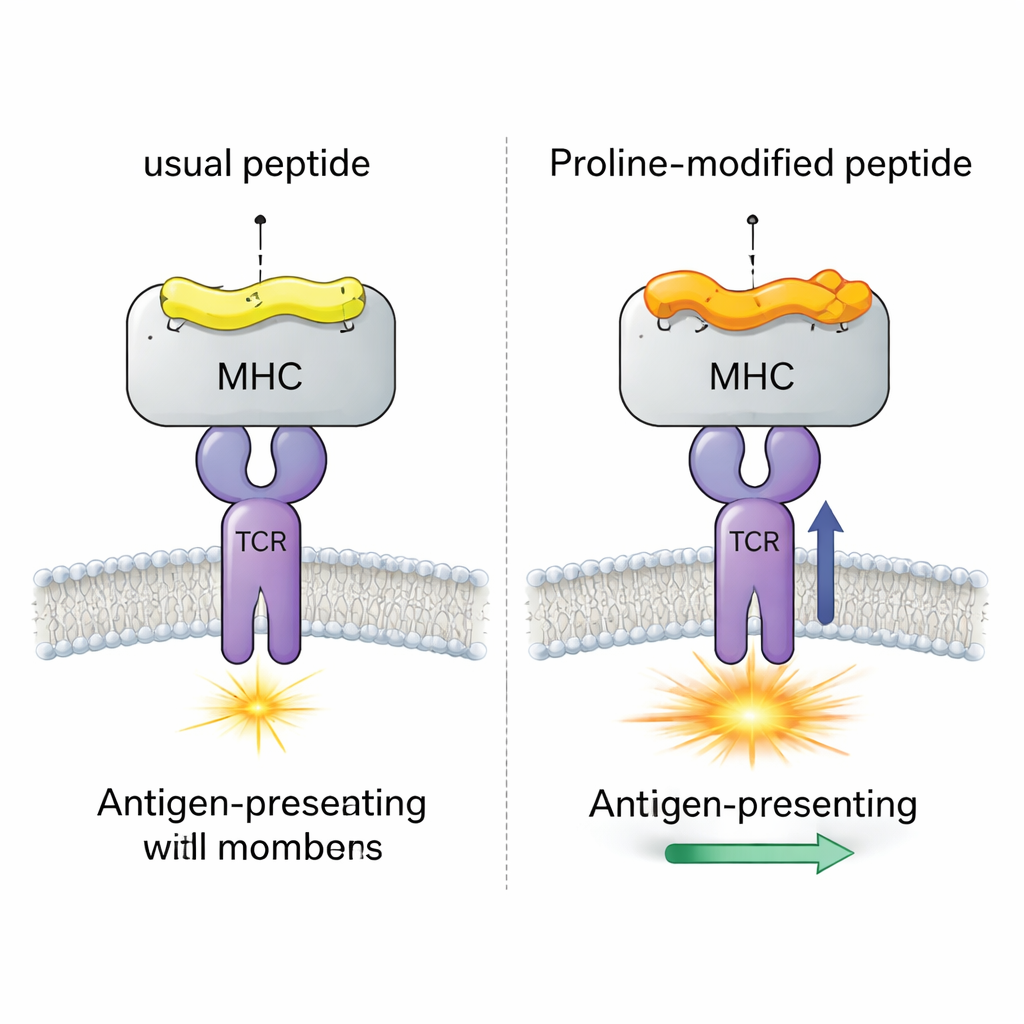
ほとんど同一の四つのペプチドを用いたウイルステストケース
研究チームは、通常強いCD8+ T細胞反応を引き起こすペプチドgp33を含む、よく研究されたマウスウイルス(LCMV)システムに注目しました。彼らは同じMHC分子(H-2Db)に結合した非常に近縁な四つのバージョンのペプチドを比較しました。一つは元のウイルスペプチド、もう一つはT細胞がほとんど認識しない免疫逃避変異を持つもの、そして二つはペプチドの開始近くの単一のアミノ酸がプロリンに置換された「プロリン変化」ワクチン候補です。以前の実験は、このプロリン置換がpMHC複合体の結合の強さとモデルTCR(P14と呼ばれる)の応答を高めることを示していましたが、詳細なメカニズムは不明でした。
分子の揺らぎを観る:シミュレーションと結晶学の融合
何が起きているかを明らかにするために、著者らは高解像度の結晶構造と、各pMHC複合体の長時間にわたる原子レベルのコンピュータシミュレーションを組み合わせました。彼らは各アミノ酸残基が時間を通じてどれだけ変動するか、そしてペプチドの3番目の位置がプロリンに変換されたときにこれらの変動がどのように変わるかを調べました。多数の対になったシミュレーション間で運動パターンを相関させることで、たとえ空間的に離れていても一緒に動く残基の「動的マップ」を構築しました。次にこのマップをネットワークに変換し、各残基をノード、エッジを統計的に連動する運動として表現し、ソーシャルネットワーク解析で使われるようなグラフ理論ツールで解析しました。
免疫の錠前内部における長距離通信
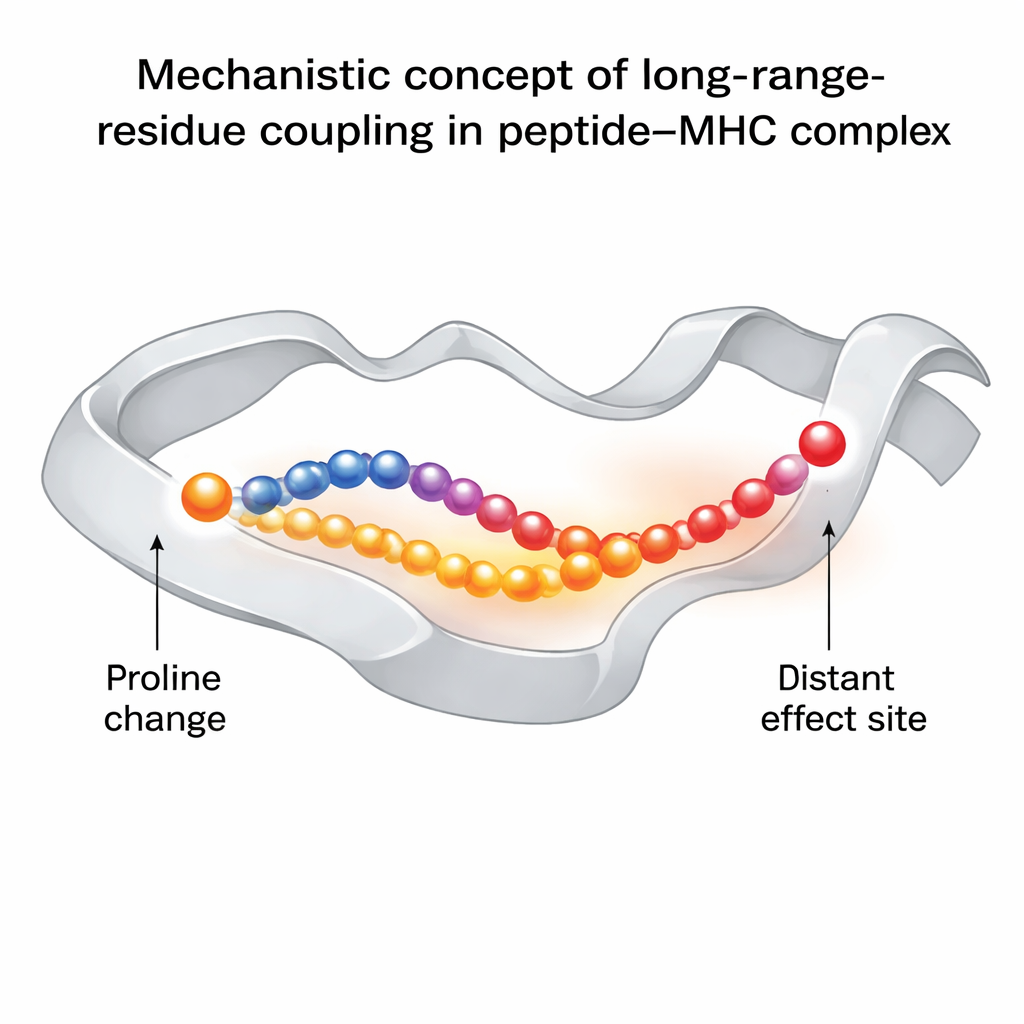
中心的な発見は、ペプチドの3番目残基をプロリンに変えることが単にその局所部位を硬くする以上の効果を持つということです。それはペプチド結合溝に隣接するMHCの一つのヘリックスに沿って運動が伝わる様子を変えます。これが結果としてTCRの足跡の直下に位置し認識に重要なペプチドの別の残基、6番目の振る舞いに影響します。「良好な」プロリン改変バージョンでは、この残基はTCR結合に最適な構造を含めより広い範囲の立体配座をサンプリングします。プロリンを持たない免疫逃避変異体では、その残基はより固定されやすく、TCRに適合する向きをとることはめったにありません。ネットワーク解析は、この影響がMHC溝の特定のアミノ酸を介して伝播し、プロリン変化の部位をTCR接触領域に結ぶ動的に結合した残基の連鎖を形成していることを明らかにします。
ワクチンと免疫療法にとっての意義
これらの結果は、免疫原性―ペプチドがどれだけ強くT細胞を引き起こすか―が単一瞬間の形状の適合だけで決まるわけではなく、複合体が時間を通じてどのように呼吸し、たわむかにも依存することを示しています。ある位置での微妙な変化は分子ネットワークを通じて波及し、重要な接触残基がTCRに適合する姿勢をとりやすくする可能性があります。著者らの計算ワークフローは、そのような長距離結合を体系的に検出する方法を提供し、ワクチンやがん治療のための変化ペプチド設計の指針に役立つ可能性があります。簡単に言えば、どこをどのようにペプチドを調整するかを慎重に選ぶことで、免疫システムの鍵がより開きやすい動的状態へと錠前全体をそっと誘導できることを示しています。
引用: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
キーワード: T細胞認識, ペプチドMHC, タンパク質ダイナミクス, 変化ペプチドリガンド, 免疫原性