Clear Sky Science · ja
前部前腸内胚葉から肺上皮前駆細胞への分化のインシリコモデリング
幹細胞を肺をつくる細胞に変える
研究者たちは、患者自身の幹細胞を置換用の肺組織へと誘導する方法を解明しつつあり、将来的にはCOPD、線維症、重篤な感染症による損傷の修復に役立つ可能性があります。本稿は、計算機モデルを用いてその過程の重要な一段階──前部前腸内胚葉と呼ばれる中間的な細胞型を初期の肺上皮前駆細胞に変える過程──をマッピングし、微調整した研究について解説します。肺上皮前駆細胞は最終的に気道や肺胞を形成する出発点となる細胞です。
なぜ肺のスターター細胞が重要か
ヒトの誘導多能性幹細胞(iPSC)は成人組織から再プログラム可能で、多くの臓器へと誘導できます。肺組織をつくるために、これらの細胞は複数の発生段階を経ます。その一つが前部前腸内胚葉で、胚発生では呼吸器系や消化器系の一部に通常発生する層です。適切な化学シグナルが与えられると、そこから肺上皮前駆細胞へと分化し、初期の肺マーカーを示し、のちに気道や肺胞の特殊化した細胞へ成熟し得ます。将来の細胞療法ではこれらの細胞が数十億個必要となるため、研究者は収率を確実に高め、実験室での果てしない試行錯誤なしに異なる患者由来細胞株にプロトコルを適応させる方法を求めています。
細胞分化の仮想モデルをつくる
研究チームは既存の数理モデルを拡張し、前部前腸内胚葉から肺前駆細胞へのこの特定の遷移について、彼らの知る限り初の集団レベルのモデルを構築しました。細胞の表現には二つの方法を考え、単純な版は生存細胞の総数のみを追跡し、より詳細な版は前部前腸細胞と肺前駆細胞を別々に追います。いずれのケースでも、モデルは培養液中のグルコースと乳酸(栄養と廃棄物)も追跡します。システム生物学の手法を用い、細胞の増殖、死、分化の振る舞いを示す多くの候補式を構築し、同定不能性テストを使って、完全なデータがあってもパラメータを特定できないモデルは棄却しました。
モデルで導く賢い実験設計
手元にあるデータに単に当てはめるのではなく、研究者たちはモデルを使ってどのように新しい実験を行うべきかを決めました。シミュレートしたデータを使って、モデルパラメータを正確に推定するにはどの頻度で細胞数や栄養レベルを測定する必要があるかを検討し、統計的精度と頻繁なサンプリングに伴うコストや労力のバランスをとりました。その結果、実用的な計画が導かれました:グルコースと乳酸は毎日測定し、細胞数は1〜2日に一度数える。条件は4つ設け、培養を10日目にどの程度分割(スプリット)するかと、増殖培地を毎日交換するかどうかを変えました。彼らはこれらの実験を実施し、総細胞数とともにフローサイトメトリーで前部前腸細胞の割合と肺前駆細胞へ分化した割合を測定しました。
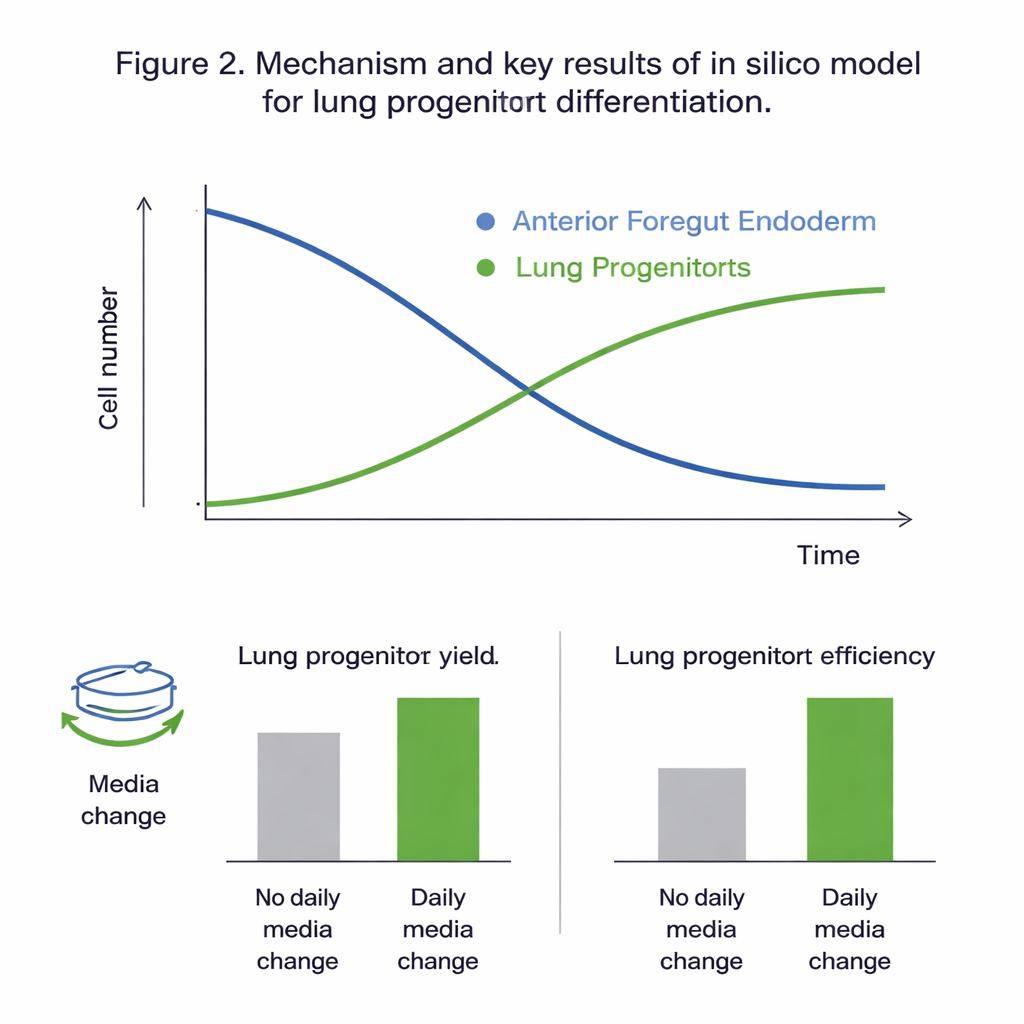
仮想実験が明らかにしたこと
候補モデルすべてを実験データにフィットさせた結果、前部前腸細胞と肺前駆細胞を分けて追う二集団モデルが信頼性高くキャリブレーションでき、観察された振る舞いを最もよく再現することが示されました。統計的検証から、研究で扱った時間窓(プロトコルの11日目から15日目)では、ダイナミクスは主に前部前腸細胞の増殖と分化によって駆動され、肺前駆細胞自身の増殖寄与は小さいことが示唆されました。グローバル感度解析もこの見立てを支持し、前部前腸細胞の成長、死、分化速度とグルコースの影響が結果を左右する主要なレバーであることを浮き彫りにしました。キャリブレーションされたモデルは未使用のデータを実験の自然変動と同等の誤差で再現し、インシリコでの「もしも」のシナリオ検討に十分な精度があることを示しました。
培地交換と細胞スプリットの最適化
信頼できる仮想システムを得たことで、チームは二つの実用的なプロトコール選択が結果にどう影響するかを試しました:10日目の培養をどれだけ希釈するか(スプリット比)と、増殖培地を毎日交換するかどうかです。シミュレーションは、培地を毎日交換すると肺前駆細胞数と投入細胞当たりの収率がほぼ倍増すると予測しました。これは主に栄養枯渇や廃棄物、安定しないシグナル分子の蓄積を防ぐことによります。実験結果もこれらの予測とよく一致しました。またモデルは、10日目により高いスプリット比(細胞を薄く広げる)を使うと、絶対的な細胞数は減るものの「投入細胞当たりの収率」が約25%改善されると示唆しました。いずれの場合も、培養内に占める肺前駆細胞の最終的な割合にはほとんど影響がなく、生産効率に応じて生産可能な細胞数が変わる、という結果でした。
将来の肺治療にとっての意義
専門外の方への要点は、著者たちが幹細胞から肺細胞を育てる重要な一工程のための飛行シミュレーターのようなものを構築したということです。慎重に設計した実験と厳密な数理モデリングを組み合わせることで、培地をどれくらいの頻度で交換するか、どのくらいの密度で細胞を播種するかといった単純なプロトコールの選択が、生成される肺構築細胞の量に大きく影響し得ることを示しましたが、品質自体は変わりません。こうしたインシリコモデリングは将来のプロトコールを合理化し、実験の試行錯誤を減らし、最終的には研究、疾患モデル作成、ひいては再生療法のための肺前駆細胞のより信頼できる大規模生産を支える助けとなります。
引用: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
キーワード: 肺前駆細胞, 誘導多能性幹細胞, インシリコモデリング, 細胞分化, 再生医療