Clear Sky Science · ja
複雑な空間環境における細胞移動ダイナミクスのシミュレーションに基づく推論
混雑した組織内で免疫細胞はどう進路を見つけるか
免疫細胞は感染部位やリンパ節に到達するために、しばしば密集した迷路状の組織を押し分けて進む必要があります。本研究は一見単純に思えるが重要な問いを投げかけます:これらの細胞はこうした散乱した環境をどのように移動するのか、そして雑多な顕微鏡データからその挙動をどのように確実に推定できるのか。精密に設計した実験用“迷路”と高度な計算シミュレーション、最新の機械学習手法を組み合わせることで、著者らは複雑な環境での細胞運動を導くルールを解読する新しい方法を示しています。
免疫細胞のための小さな迷路を作る
環境が移動に与える影響を調べるため、研究者たちは樹状細胞に注目しました。これらは末梢組織からリンパ節へ移動し、ケモカインと呼ばれる化学的な誘引に導かれる免疫の哨兵です。研究チームはマイクロ加工されたチップ、平坦な“ピラー林”を作製しました。これはシリコーンゴム(PDMS)製の規則的に並んだ柱からなり、実際の組織の狭い隙間を模した幅10マイクロメートルの狭い間隔を持ちます。チップの片側には数万個の樹状細胞が配置され、対向側にはケモカインCCL19の供給源を置いて柱群を横切る安定した勾配を作りました。タイムラプス顕微鏡で、各細胞の核を30秒ごとに追跡し、ケモカイン源に向かって移動しようとする様子を記録しました。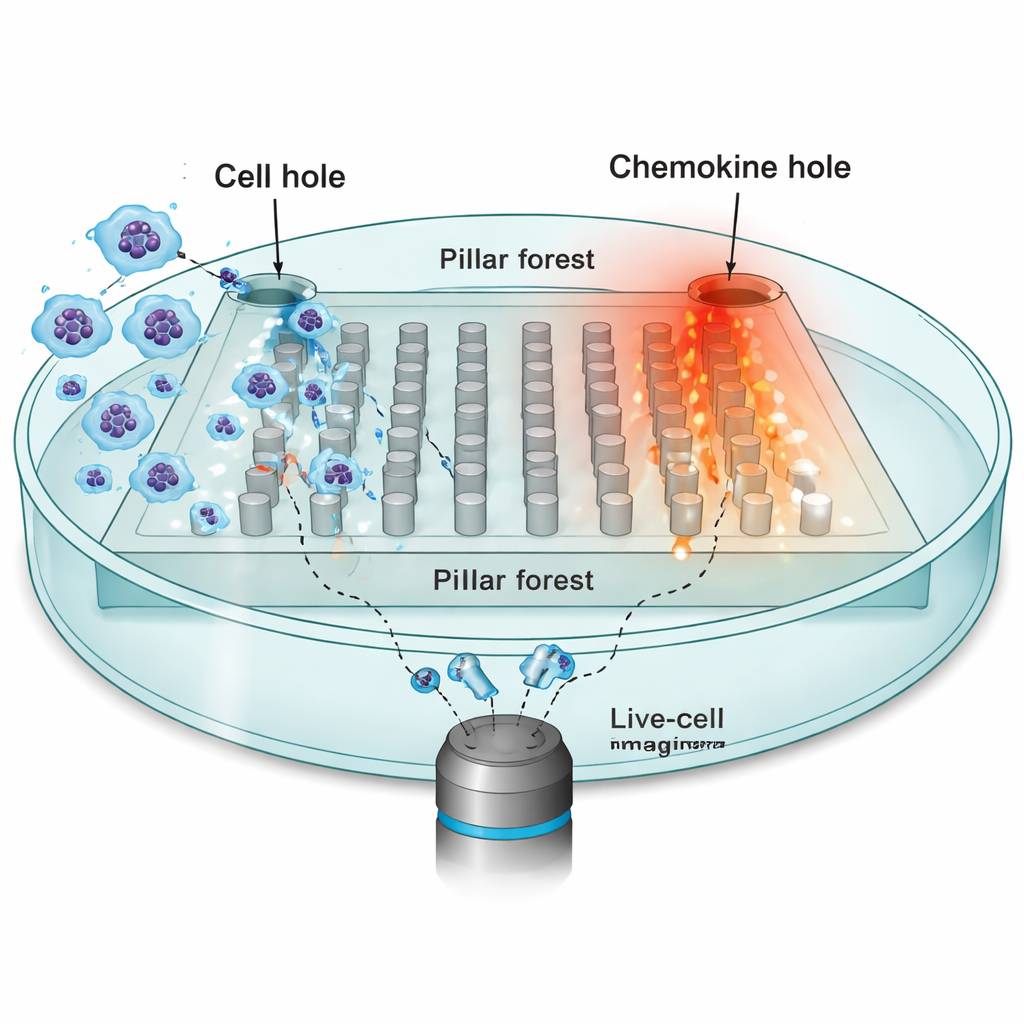
生物現象を仮想実験に変える
この多様性を理解するため、チームはCellular Pottsモデルとして知られる枠組みを用いて、細胞移動の詳細な計算モデルを構築しました。単純な点として細胞を扱う代わりに、この手法は格子上の拡がりを持つパッチとして各細胞を表現し、形状変化、ピラー間のすり抜け、化学信号への応答が可能になります。モデルは4つの主要な要素を含みます:ケモカイン勾配による細胞の引力の強さ(mdir)、現在の運動方向を維持する傾向(mrand)、再配向の頻度(率λで表現)、および実効サイズ(a)。これらのパラメータを調整してシミュレーションを実行することで、モデルは実験で記録されたピラー林中の細胞経路と直接比較できる合成軌跡を生成します。
手作りの測定では不十分な理由
従来、研究者はこうした移動データを、移動距離(変位)、速度、時間経過に伴う方向変化(旋回角度)といったおなじみの統計量で要約してきました。著者らはまずこれらの手作りの要約統計量を用いて近似ベイズ計算(ABC)という手法で、シミュレーションの軌跡が実験データに似るようなパラメータ集合を探索しました。これらの要約は大まかな傾向をとらえる一方で、データ中の細かな構造の多くを見落とすことが分かりました。その結果、特にランダムな持続性や再配向のタイミングを支配するパラメータは十分に絞り込めず、場合によっては偏りが生じました。加えて、ABCは受け入れ可能な適合を得るために何十万ものシミュレーションと何時間もの計算時間を必要としました。
重要な特徴をニューラルネットに学習させる
こうした限界を克服するため、研究はニューラルポスター推定(NPE)と呼ばれる新しい手法群に注目しました。ここでは、ニューラルネットワークを多数のシミュレーションデータとそれに対応する基底パラメータのペアで直接訓練します。ネットワークの一部は細胞軌跡の集合全体から自動的に圧縮された「要約特徴」を学習し、別の部分はそれらの特徴がどのように尤もらしいパラメータ値へと逆に写像されるかを学習します。重要なのは、これらの学習された特徴は人間が解釈しやすいことではなく、正確なパラメータ推定のために明示的に最適化されている点です。著者らはその後、学習された要約をABCの枠組み内で再利用し、ABCの堅牢性とニューラルネットの柔軟性を組み合わせたハイブリッドなパイプラインを作成しました。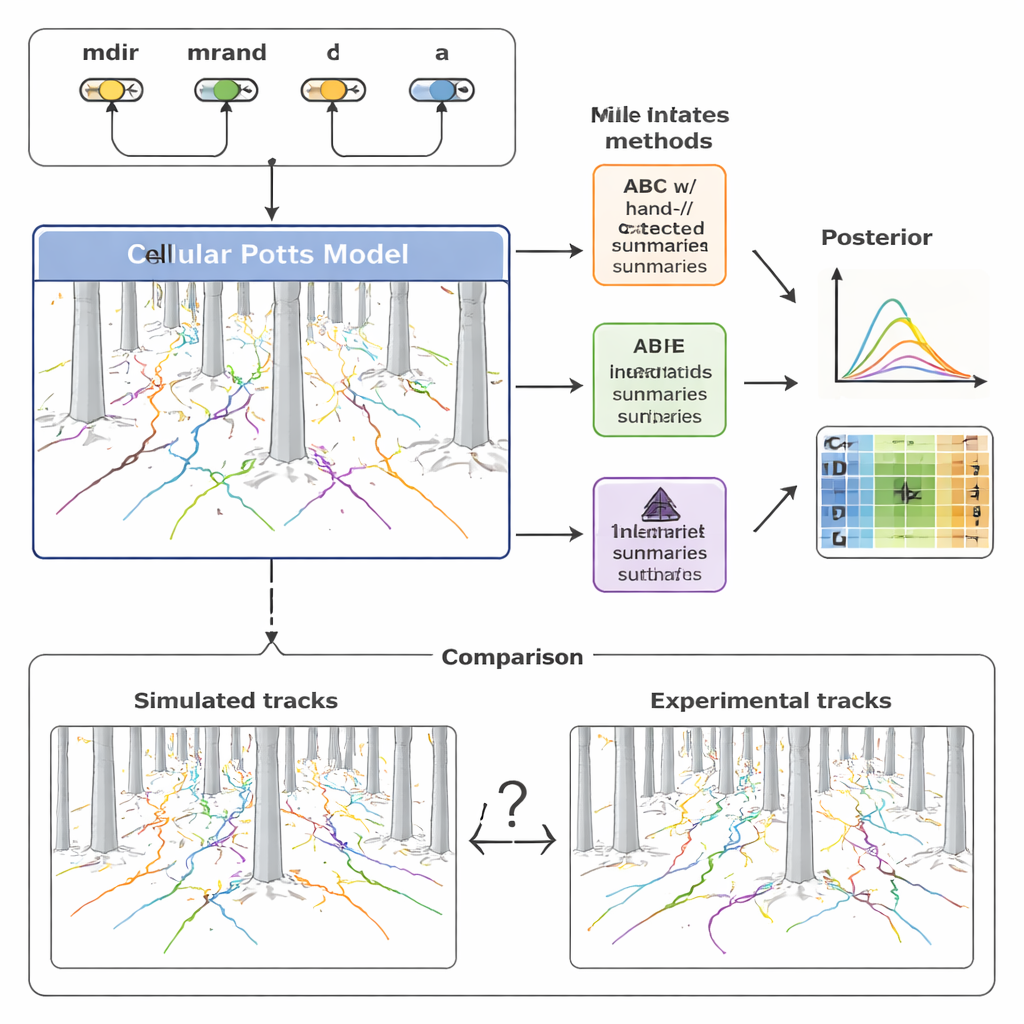
新手法が明らかにする細胞の誘導法
この較正されたモデルを用いて、研究者たちはケモカイン信号と物理的障害物が移動をどのように共同で形作るかを探りました。推定された細胞サイズは、樹状細胞が10マイクロメートルの隙間を通るために実効的に縮み変形することを示唆しており、既知の柔軟性と整合します。シミュレーションは、持続的なランダム運動がケモカイン誘導なしでも細胞の広がりを大きく左右する主要な駆動力であり、強い指向性手がかりと高い持続性が組み合わさるとピラー林が細胞を閉じ込め得ることを示しました。驚くべきことに、モデルは、初期に短時間だけ活性なケモカイン信号の方が、一定の信号よりも多くの細胞を標的に到達させる場合があると予測します。これは、長時間の誘引が障害物内で細胞をぐるぐる回らせ、脱出を妨げる可能性があるためです。
生物学とモデリングにとっての意義
専門外の方への要点は二点です。第一に、組織内の免疫細胞移動は単に化学的な跡をたどるだけではなく、誘導手がかり、細胞固有の運動傾向、周囲の物理的配置の微妙な相互作用から生じるということ。第二に、イメージングデータからこれらのルールを抽出するには、単純で人間が設計した測定量にのみ頼るのではなく、データ中で最も情報量の多いパターンをコンピュータに学習させる必要があるということです。マイクロ工学的実験、形状を解像するシミュレーション、ニューラルネットワークに基づく推論を統合することで、本研究は多様な細胞種が複雑な環境を移動する仕組みを研究するための強力なテンプレートを提供し、免疫監視の理解からより良いがん治療設計まで幅広い応用が期待されます。
引用: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
キーワード: 細胞移動, 樹状細胞, ケモカイン勾配, シミュレーションに基づく推論, マイクロ流体ピラー林