Clear Sky Science · ja
多糖類と大腸粘液バリア:生物物理学的相互作用と機能的影響のレビュー
腸の滑らかな内層が重要な理由
大腸の奥深くには目に見えない粘膜層があり、何兆もの微生物を自分の細胞から一定の距離に保つ薄い防御膜として働いています。本レビューは、食品、海藻、菌類、医療製品などに含まれる複雑な糖鎖である多糖類がこの粘液バリアとどのように相互作用するかを探ります。食事と粘液の間にあるこうした対話を理解することで、特定の食物繊維が腸の健康に有益である理由、ある治療法が大腸炎などの腸疾患からどのように保護するか、そして将来的により賢い薬物送達システムが薬剤を必要な場所に精密に届けられる可能性があることが説明されます。
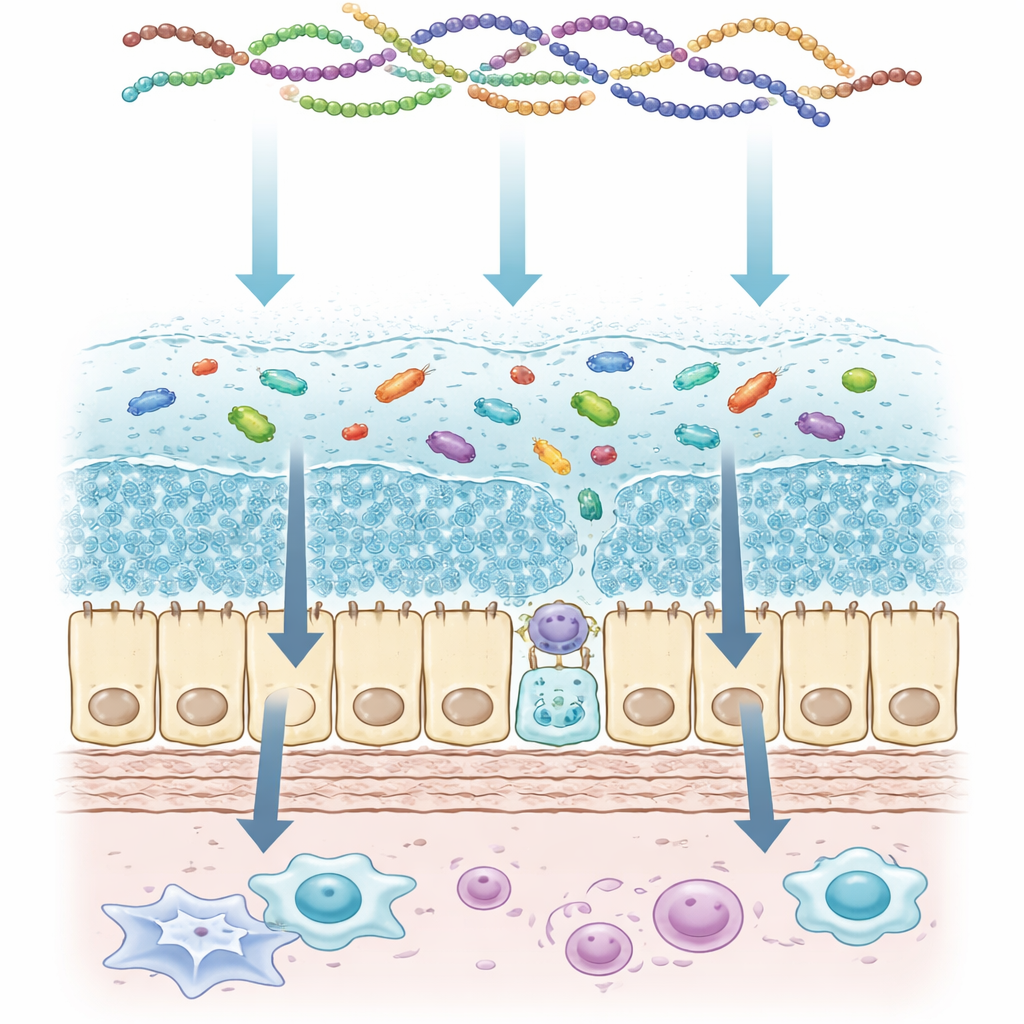
大腸の二重構造の安全毛布
著者らはまず、大腸粘液の構造を二層構造として記述します。腸壁に最も近い内側の層は細菌がほとんどいない密な層で、堅牢な盾のように機能します。その上にある外側の層はより緩い構造で、良好な微生物にとって制御された生息地の役割を果たします。ゴブレット細胞と呼ばれる専門の細胞が継続的に大型の粘液分子を産生・分泌し、これらは腸表面に達すると急速に展開してゲル化します。これらのゲル形成分子は多数の糖鎖で修飾されており、それが粘液の粘度、水分保持能、負電荷を生み出します。この構造が炎症、感染、遺伝的欠陥などで破綻すると、細菌が壁に近づき、免疫のアラームが作動し、慢性的な腸疾患が出現することがあります。
糖の種類で変わる付着の仕方
多糖類は単糖が長くつながった鎖ですが、粘液中での振る舞いはサイズ、分岐、電荷などの細かな特徴に依存します。レジスタントスターチやイヌリンのような中性の鎖は、主に水素結合や物理的な絡み合いを通じて粘液の網目に織り込まれます。ペクチン、アルギン酸、海藻由来のガム類に見られる負に帯電した鎖は、局所のイオン環境や双方の微細な電荷配列に応じて、粘液と弱く結合したり反発したりします。甲殻類や菌類由来のキトサンのような正に帯電した鎖は粘液に強く引き寄せられ、緊密な複合体を形成し得ます。レビューでは、これらの相互作用は単一の力で支配されるのではなく、静電的引力、水素結合、疎水性接触、微妙なファンデルワールス力が混在して、多糖類がゲルにどの程度浸透しどれだけ強く付着するかを決めると説明しています。
チップ、培養皿、切片上のモデル腸壁
これらの複雑な相互作用を解きほぐすために、研究者たちは多種の実験モデルを用います。平面の細胞培養は粘液分泌細胞を加えることで、特定の多糖類が粘液の産生、厚さ、漏れやすさにどう影響するかを調べることができます。幹細胞から成長させた三次元のオルガノイドは自ら粘液を分泌する小さな腸管を作り、マイクロフルイディクスの“腸オンチップ”プラットフォームは実際の流れ、伸展、共生する生菌を加えてより現実的な条件を再現します。ex vivoのセットアップは新たに分離した腸組織を短時間生存させ、自然の粘液層や免疫細胞を保持します。各モデルにはトレードオフがあり、単純な培養皿は扱いやすいが人工的であり、チップやオルガノイドはより現実的だが技術的に難しいです。これらのシステム間で結果を比較することで、多糖類が粘液に及ぼす直接的な物理効果と、微生物や免疫系が媒介する間接的な影響を区別できます。
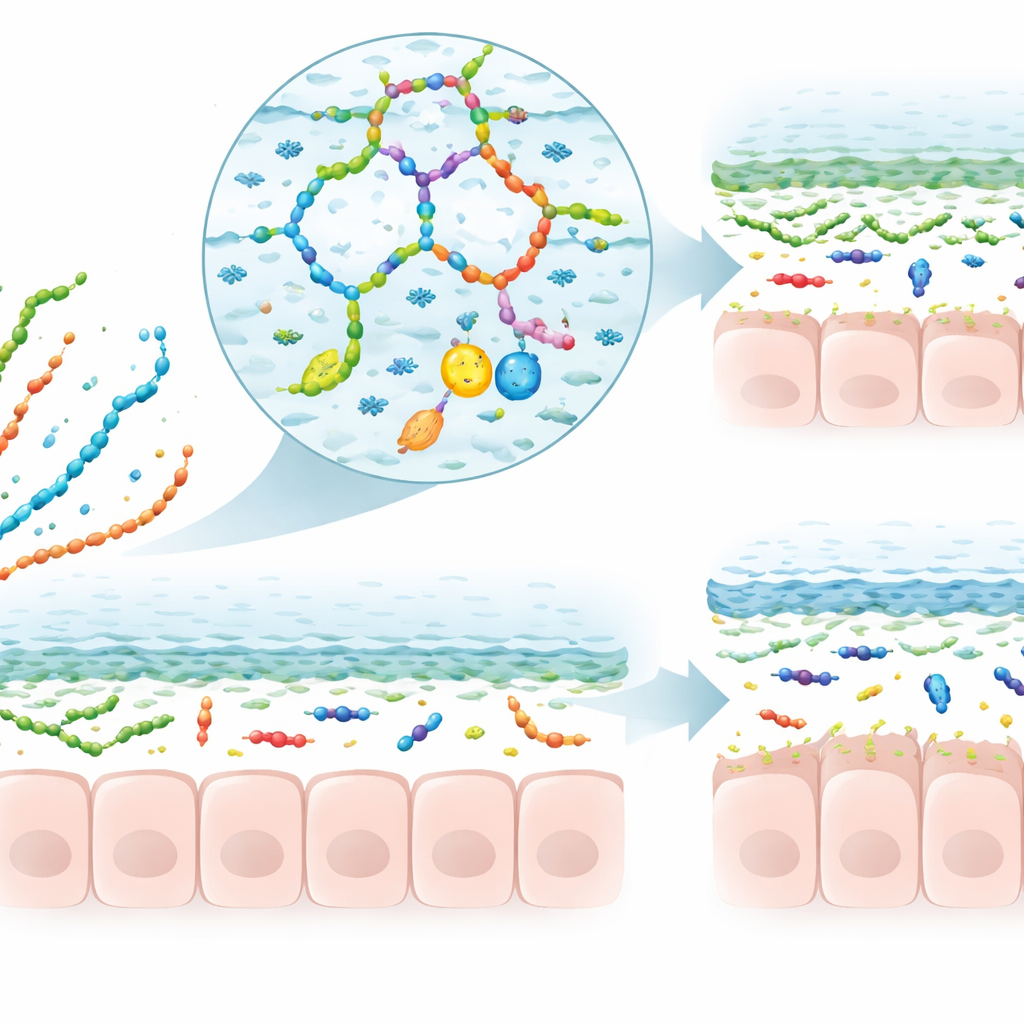
粘液、微生物、免疫応答のかたち作り
次にレビューは、多糖類が粘液と出会ったときに機能的に何が起きるかを検討します。正に帯電した一部の鎖は一時的にゲルを緩めたり再編成したりして、粒子や薬物が通過しやすさに影響を与えることがあります。別のものは粘液と混合ネットワークを形成して層を濃くしたり安定化したりします。多くの食事性多糖類は私たちによって消化されず、腸内細菌によって発酵され、短鎖脂肪酸やその他の小分子に変換されます。これらの発酵産物はゴブレット細胞により多くの粘液を作らせたり、粘液の糖鎖飾りを調節したり、外層に安全に留まる傾向のある微生物コミュニティを支援したりするシグナルを送ります。大腸炎の動物モデルでは、特定の植物や菌類由来多糖類がゴブレット細胞数を増やし、粘液の厚さを回復させ、細菌が腸壁から遠ざかることを促し、しばしば炎症や酸化ストレスの低下を伴います。
粘液と協調する食品・治療の設計
結びとして、著者らは多糖類は意図的に設計または選択することで粘液バリアを支えることができ、偶発的に損なうのではないと主張します。電荷や分子量といった特定の構造的特性を、粘液の厚さ、粘度、貫通性といった測定可能なアウトカムに結びつけることで、バリアを強化する、薬物を大腸へより効果的に運ぶ、あるいは腸内微生物叢を健康促進的な活動へ穏やかに誘導する多糖類の選択指針を提案します。非専門家に向けた中心的なメッセージは、大腸を覆うこの粘性の膜はただの受動的な物質ではなく、食事の化学、常在微生物、免疫防御が出会う能動的な界面であるということです。慎重に設計された多糖類は、その界面を保ちつつ腸のバランスを保つための重要な手段になり得るでしょう。
引用: Cheong, KL., Biney, E., Wang, M. et al. Polysaccharides and the colon mucus barrier: a review of biophysical interactions and functional impacts. npj Sci Food 10, 98 (2026). https://doi.org/10.1038/s41538-026-00750-6
キーワード: 大腸粘液バリア, 食事性多糖類, 腸内微生物叢, 粘膜付着性薬物送達, 炎症性腸疾患