Clear Sky Science · ja
宿主由来のインターロイキン-1αが腫瘍随伴ミエロイド細胞を再プログラムして腫瘍免疫抑制を引き起こす
なぜこの研究ががん患者にとって重要か
免疫療法は一部のがん治療を変革しましたが、多くの乳がんは依然として免疫系を回避します。本論文は、がん細胞自身ではなく正常組織の細胞が作るシグナル分子、インターロイキン‑1α(IL‑1α)というあまり注目されない要因を検討します。著者らは、宿主由来のIL‑1αが免疫細胞を腫瘍の味方に静かに変えてしまい、このシグナルをブロックするとマウスで乳腺腫瘍が縮小または消失することを示しています。このスイッチを理解することは、乳がんに対する免疫療法をより効果的にする治療設計に役立つ可能性があります。
腫瘍の“近隣”に潜む影響因子
がんは孤立して成長するわけではなく、免疫細胞、血管、結合組織といったにぎやかな「近隣」――腫瘍微小環境の中で存在します。その主要な住人の一つがミエロイド細胞、特にマクロファージで、これらは腫瘍を攻撃することもあれば保護することもあります。教科書的にはマクロファージはM1(腫瘍抑制的)とM2(腫瘍支持的)に分けられますが、実際の腫瘍にはその中間的な表現型が多く存在します。著者らは、非がん組織で通常産生される分子であるIL‑1αに着目し、この宿主シグナルが乳腺腫瘍内に侵入するミエロイド細胞を有益な方向へ向かわせるのか、有害な方向へ向かわせるのかを問いかけました。
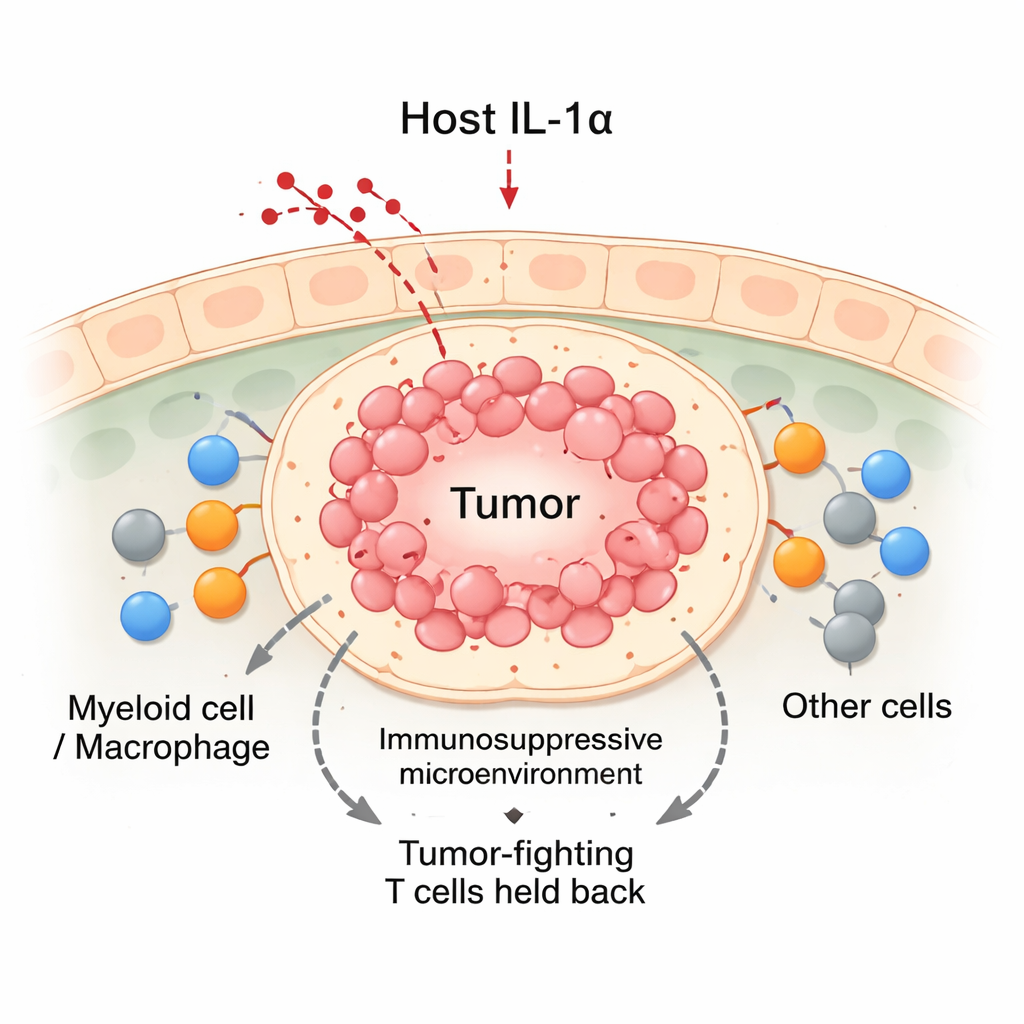
IL‑1αをオフにすると腫瘍に不利に働く
マウスの乳がんモデルを用いて、研究チームは正常マウスとIL‑1αを欠損するように遺伝子改変したマウスを比較しました。乳がん細胞を乳腺に移植すると、正常マウスでは腫瘍は着実に増大しました。対照的にIL‑1α欠損マウスの腫瘍は最初の約2週間は成長したものの、その後しばしば退縮しました。退縮する腫瘍は全体としてより多くの免疫細胞を含み、CD8の“キラー”T細胞やミエロイド細胞の急増が見られました。IL‑1α欠損マウスでは循環血中の白血球は減少していたにもかかわらず、腫瘍部位にははるかに多くの免疫細胞を集積させていました。詳細解析では、IL‑1α欠損腫瘍に浸潤したCD8 T細胞はより活性化され、腫瘍細胞を殺す分子を多く産生し、疲弊の兆候が少ないことが示されました。
IL‑1αが腫瘍随伴ミエロイド細胞をどう再形成するか
IL‑1αが細胞レベルで何をしているかを理解するため、研究者らは単一細胞RNAシーケンシングを用いて腫瘍から得られた何千もの個々の細胞を解析しました。その結果、腫瘍随伴マクロファージのうちごく一部、CX3CR1という受容体でマーキングされるサブセットだけがIL‑1αを産生していることが明らかになりました。正常マウスでは、侵入してきた単球の多くがこれらのCX3CR1陽性マクロファージへ成熟し、免疫抑制的な振る舞いと結び付いていました。IL‑1α欠損マウスではこの成熟経路が妨げられ、その代わりミエロイド細胞はiNOS陽性の炎症性マクロファージに向かいやすくなり、これは抗腫瘍活性と関連します。機能的には、IL‑1α欠損腫瘍由来のミエロイド細胞はT細胞上のPD‑1やCTLA‑4といったブレーキを誘導する能力が低く、T細胞増殖を抑える力も弱くなっていました。
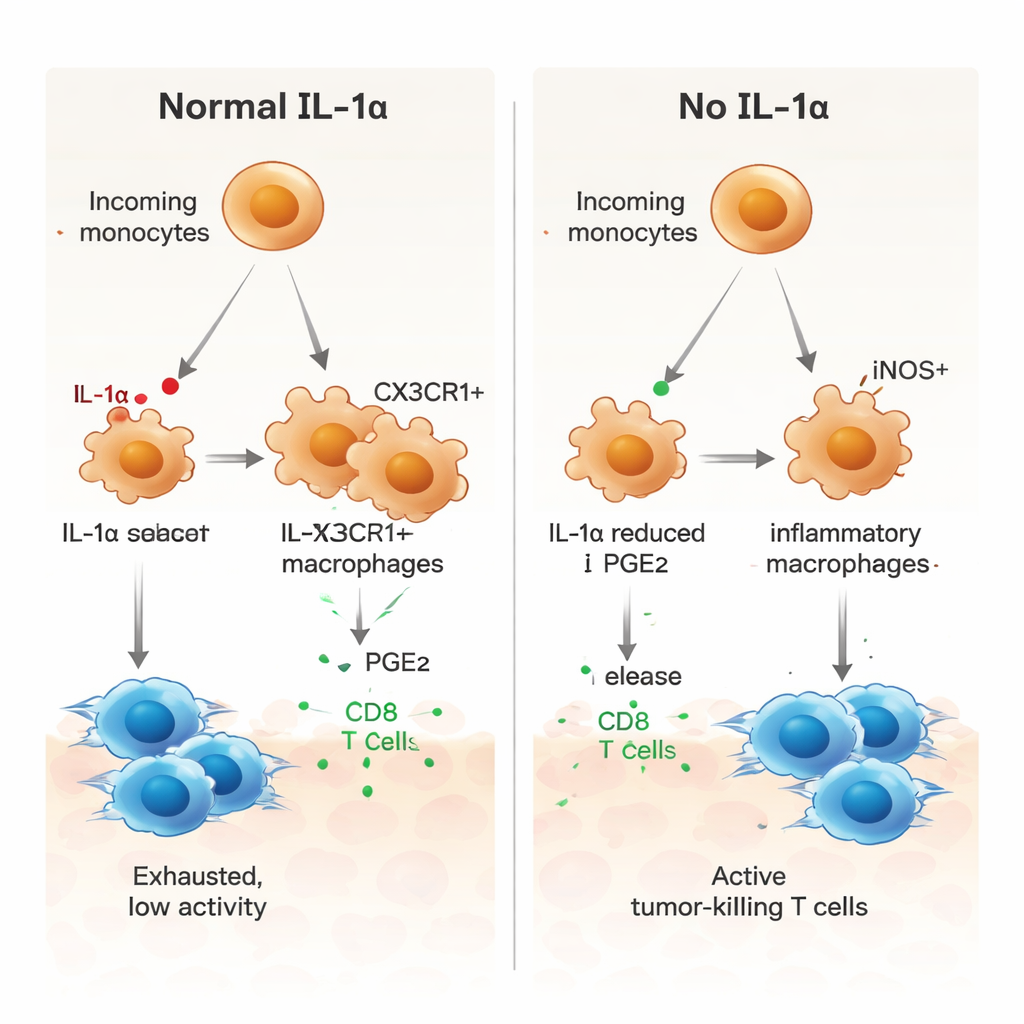
脂質メッセンジャーPGE2の重要な役割
著者らは次に、IL‑1αがどのようにミエロイド細胞を腫瘍支持的な状態へ導くのかを問い、単一細胞データのコミュニケーション解析からいくつかのシグナル経路が示唆されました。その一つが免疫抑制を促進することが知られている脂質メディエーター、プロスタグランジンE2(PGE2)を含む経路です。IL‑1α欠損腫瘍では、マクロファージはマクロファージ増殖因子(M‑CSF)受容体やTGF‑β受容体、PGE2受容体の発現が低く、近傍の間質細胞はPGE2を産生する酵素をあまり作っていませんでした。培養実験では、IL‑1α欠損マウス由来の骨髄由来マクロファージはより炎症性のプロファイルを示し、iNOSが高くCX3CR1が低い状態でした。PGE2を添加するとこの変化は逆転し、より抑制的なパターンが回復しました。一方、正常マクロファージでPGE2を阻害するとそれらは炎症寄りに変わりました。IL‑1αを欠くマクロファージは腫瘍特異的なCD8 T細胞の増殖もより強く刺激し、この効果はPGE2を戻すと減弱しました。
マウスの知見をヒト免疫へ橋渡しする
マウスデータがヒト生物学を反映するかを確認するため、チームはマウスの異なるマクロファージサブセットから得られた遺伝子シグネチャを、さまざまな状態へ誘導された大規模なヒトミエロイド細胞のパネルと比較しました。正常マウスの腫瘍由来マクロファージクラスターは、IL‑10、IL‑4、糖質コルチコイドなどの分子によってM2様の免疫抑制的状態へ押しやられたヒト細胞に似ていました。これに対して、IL‑1α欠損腫瘍の同一クラスターは、より炎症的で抑制的でない条件にあるヒト細胞に一致しました。特に、PGE2シグナルに結び付く遺伝子パターンはIL‑1α依存のマクロファージに濃縮されていましたが、IL‑1αが欠けると消失しており、IL‑1αとPGE2が協働して免疫抑制的なニッチを作るという考えを補強しました。
将来の乳がん治療にとっての意味
平易に言えば、本研究は宿主由来の分子IL‑1αが特定のマクロファージに腫瘍を保護しキラーT細胞の働きを抑えるように“指示”し、部分的にはPGE2シグナルを介してこれを行うことを示唆しています。マウスでIL‑1αを除くと、マクロファージはより炎症性で腫瘍攻撃的な状態へ変わり、CD8 T細胞はより活性化し、移植された乳腺腫瘍はしばしば排除されました。現在の免疫療法は疲弊したT細胞の再活性化を目指しているため、IL‑1αやその下流のPGE2経路を阻害するアプローチと組み合わせれば、腫瘍微小環境を患者の免疫に有利にさらに傾ける可能性があります。ヒトでの安全性と有効性を確認するにはさらなる研究が必要ですが、これらの成果は乳がんを免疫攻撃に対してより脆弱にする新しい標的としてIL‑1αを示しています。
引用: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
キーワード: 乳がん免疫療法, 腫瘍微小環境, マクロファージ, インターロイキン-1α, プロスタグランジンE2