Clear Sky Science · ja
ストレス関連シグナル分子の微生物による制御とその健康・疾病への役割
腸内の小さな住人が私たちのストレスをどのように形作るか
多くの人はストレスを頭の中で起きる現象だと考えがちですが、本稿はストレス応答における最も重要なプレーヤーの一部が腸内に住んでいることを示しています。腸内に棲む微生物は、単に食物の消化を助ける以上の働きをします。圧力や恐怖、痛みに対する体の反応を制御するホルモンを合成・分解・変換し得るのです。この隠れたパートナーシップを理解することは、炎症性腸疾患、うつ病、その他ストレスに関連する病態を和らげる新しい手段を開く可能性があります。
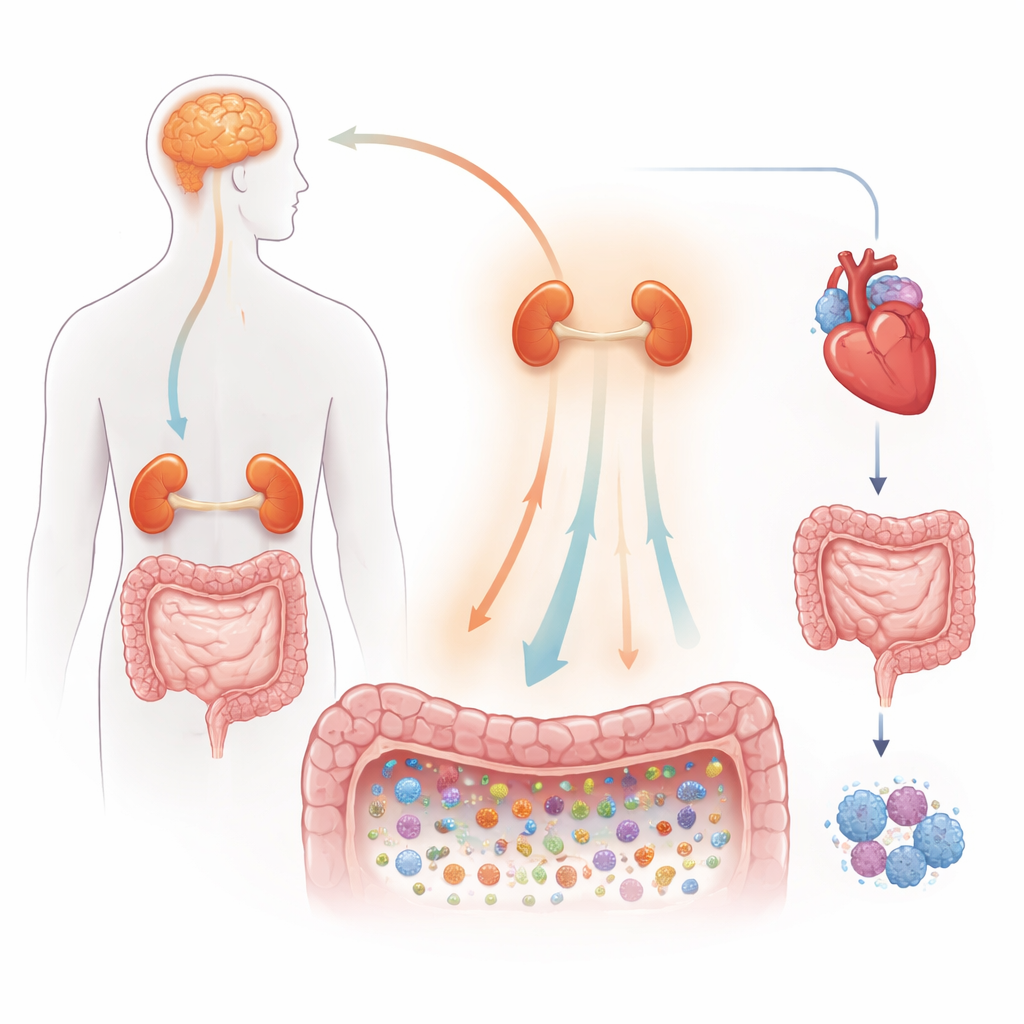
体に備わる警報システム
著者らはまず、ストレス応答が通常どのように機能するかを概説します。挑戦に直面すると、脳は下垂体や副腎を介した指令系を起動し、アドレナリン様のカテコールアミンや糖質コルチコイドと呼ばれるステロイドホルモンなどの化学伝達物質を全身に放出します。これらのシグナルは心拍数を高め、血流を再分配し、腸運動を変え、免疫系を“闘争か逃走か”に合わせて調節します。消化管に直接つながる神経は腸へ信号を素早く伝え、腸のバリアを締めたり緩めたりして、微生物が生きる局所環境を変化させます。こうして腸はストレス生物学とマイクロバイオームが常に交わる重要な交差点となるのです。
ストレス信号を“聞き”、“語る”微生物たち
数十年にわたる研究は、多くの細菌が我々のストレス化学物質を感知し利用できることを明らかにしています。初期の実験では、特定の腸内菌や病原性細菌がノルエピネフリンやエピネフリンなどのカテコールアミンに曝露されると増殖が促進され、より攻撃的になることが示されました。別の研究では、細菌がこれらの分子を取り込み、別の形に変換したり、チロシンのようなアミノ酸から類似化合物を生成したりすることが示されています。同時に、宿主の酵素はしばしば小さな化学基を付加してカテコールアミンを“不活化”しますが、適切な酵素を持つ腸内細菌はこれらの基を切り離して再び活性型を回復させることができます。無菌のマウスでは腸内の多くのストレス伝達物質が不活性型に閉じ込められていますが、特定の細菌を導入すると活性プールが復元され、微生物がこれらのシグナルの利用可能量を直接制御していることが示されます。
内部からのストレスステロイドの再構成
レビューは次にグルココルチコイドに焦点を当てます。これは炎症を抑え、持続的なストレスに対処するために知られるステロイドホルモンです。これらのホルモンは血流から少量が腸に入るか、腸上皮で局所的に作られ、そこで密な細菌群と遭遇します。多くの腸内微生物は、これらのステロイド分子を切り詰め、再配置し、還元するような特殊な酵素を持っています。中には側鎖を切断してアンドロゲンに変換するものがあり、これは血圧やホルモン感受性のがんに影響を与える性ホルモン様の作用を持ちます。ほかの酵素は受容体結合能を弱める化学基を除去したり、強力な形に再生できないようにさらに還元したりします。さらに、硫酸や糖様の付加基を除去して体の“不活化”工程を逆転させ、ステロイドを再び活性循環に戻すものもあります。こうした作用が合わさって、マイクロバイオームはステロイドの強さとバランスを動的に制御する調節つまみとなるのです。
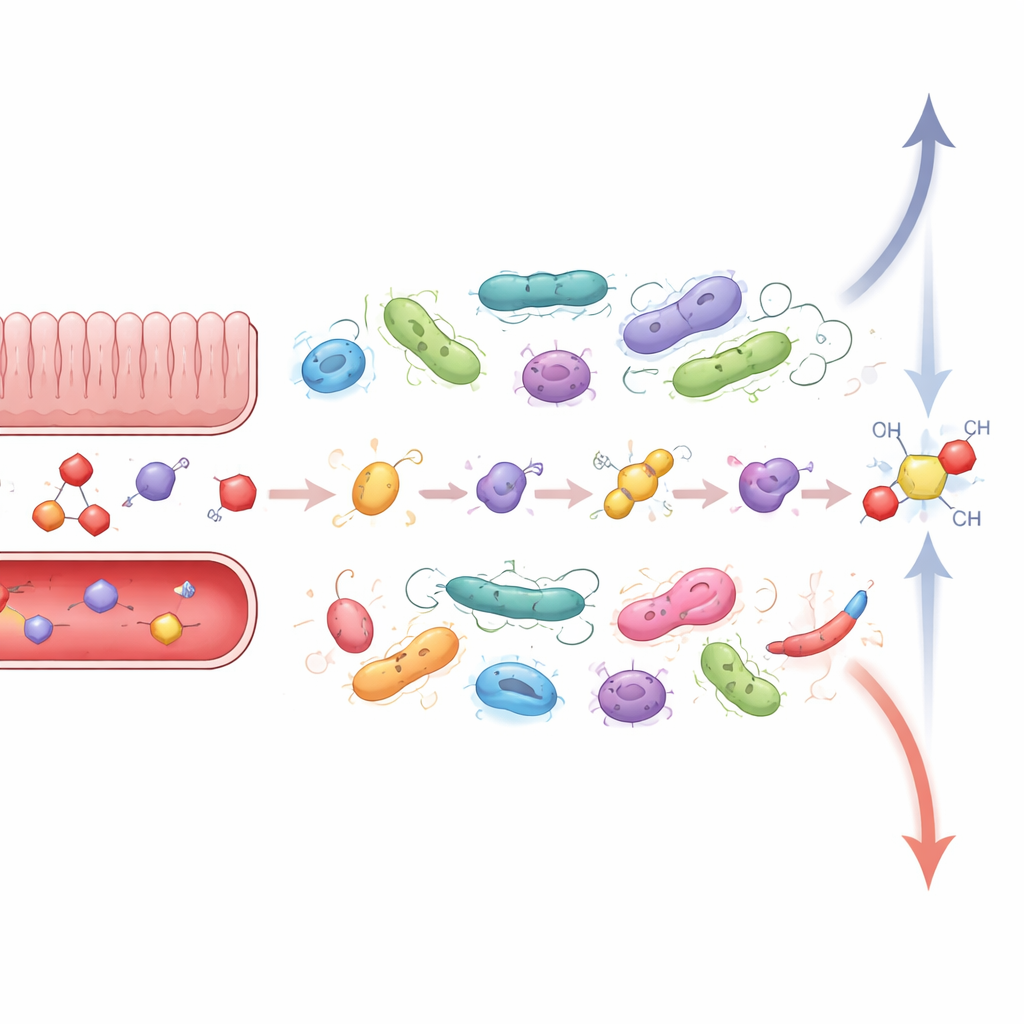
ストレス、炎症、微生物が互いに影響を与え合うとき
これらの親密な化学交換は、ストレスと腸内微生物の両方が既に乱れている疾患で最も重要になります。炎症性腸疾患(IBD)はその代表例です。患者は慢性的な腸の炎症、変化した微生物群集、そして生活ストレスに対する感受性の高まりを示します。ストレスホルモンは腸のバリアを緩め、より多くの微生物やその産物が透過して免疫系を刺激しやすくします。同時に、IBDではコルチゾールや関連ステロイドを再編成できる種の増殖や、通常はバリアを強化し炎症を鎮める短鎖脂肪酸を産生する細菌の喪失が関連しています。動物実験はこれらの微生物変化がホルモンの不均衡と免疫活性を増幅させ、ストレスが腸疾患を悪化させ、腸疾患がストレス感受性を高めるといった悪循環に患者を閉じ込める可能性を示唆しています。
腸–ストレスのループを鎮める新たな手法
微生物はストレス信号と炎症の接点に位置するため、新たな治療の魅力的な標的になります。本文は、イヌリンのような繊維を豊富に含む食事が有益な発酵産物を増やし、腸の炎症を和らげ、IBDモデルにおける一部のストレス関連損傷を軽減することを示す研究を取り上げています。ラクトバチルス属のプロバイオティクス株は腸のバリアを強化し、ストレスによるホルモンの急上昇を抑え、動物の痛み感受性を低下させることが報告されています。短鎖脂肪酸を直接大腸に供給すると、マウスの不安様行動が減り、ヒトでは社会的ストレスに対するコルチゾール応答が抑制されることが示されています。これらの初期の成果は、慎重に設計されたプロバイオティクス、プレバイオティクス、微生物代謝物が腸内でのホルモン処理を変えることでストレス応答をリセットするのに役立つ可能性を示唆しています。
日常の健康にとっての意味
結びとして、著者らは腸内微生物を受動的な傍観者ではなく、我々のストレス生物学における能動的なパートナーと見なすべきだと主張します。ストレス関連のシグナル分子を作り、修飾し、再利用することで、マイクロバイオームは私たちが挑戦にどれほど強く反応するか、どれだけ速く回復するか、そしてストレスが慢性疾患に傾く可能性に影響を与えうるのです。単一の“魔法の”微生物がストレスを治すわけではありませんが、健全な腸内環境を守り育てることがレジリエンスを高める最も強力な手段の一つであることを示唆しています。研究者たちがこれらの微生物–ホルモン相互作用をより詳細にマッピングし、人での検証を進めるにつれて、腸の健康を支える日常的な戦略がストレス、気分、炎症性疾患の管理の中核となる可能性があります。
引用: Sie, C., Tropini, C. Microbial regulation of stress-associated signaling molecules and its role in health and disease. npj Biofilms Microbiomes 12, 65 (2026). https://doi.org/10.1038/s41522-026-00932-w
キーワード: 腸内マイクロバイオーム, ストレスホルモン, マイクロバイオータ–腸–脳軸, 炎症性腸疾患, 微生物内分泌学