Clear Sky Science · ja
標識を使わない光学的代謝イメージングによる生細菌のリアルタイム高解像度代謝解析
リアルタイムで細菌の反応を観察する
細菌は私たちの体の表面や内部の至る所に存在し、静かに健康に影響を与えています。食物の消化を助け、皮膚を守り、時には抗生物質に抵抗する手強い感染症を引き起こすこともあります。本研究は、生きた細菌がストレスや薬剤に反応する様子を、個々の細胞レベルでリアルタイムに、染色や標識を行わずに観察する手法を示します。この能力は、将来的には医師がより速く適切な治療を選ぶ手助けになり、なぜ一部の感染症が治りにくいのかを理解する助けにもなるでしょう。
光が示す細菌の営み
染色や遺伝子タグを加える代わりに、研究者たちは細菌内部の特定の分子がレーザー光で励起されると自然に極めて弱く発光するという性質を利用します。NAD(P)HとFADという二つの分子は、細胞が栄養をエネルギーに変える過程で中心的な役割を果たします。高速で高解像度のレーザー顕微鏡を用いることで、発光の強度とわずかな時間遅れ(寿命)を測定し、細胞の代謝活動の活発さを明らかにできます。この手法は標識不要で非破壊的であるため、同じ生細胞を数秒〜数分にわたって環境変化に伴って追跡できます。 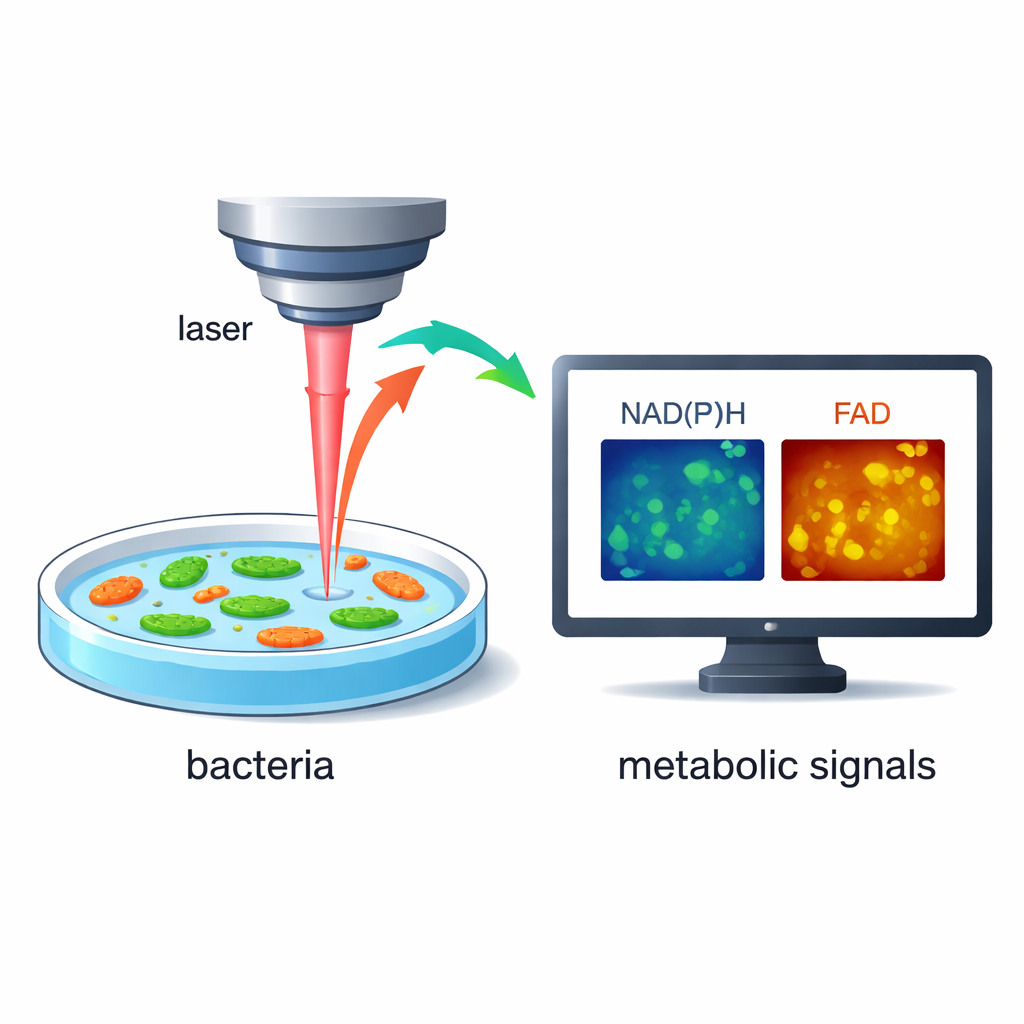
個々の細菌間の差を可視化する
一般的なラボ検査では数百万の細菌をまとめて測定し、平均的な反応しか得られません。本研究のイメージング法は、液体培養中の単一の黄色ブドウ球菌(Staphylococcus aureus)を高密度でも識別し、それぞれを個別に解析できることを示しています。同じ条件で育てた二つのコロニーを比較したところ、FAD由来の主要なシグナルがコロニー間で異なり、各コロニー内でも値のばらつきが見られました。これは、同一フラスコ内の遺伝的に似た細菌でも非常に異なる代謝状態にある場合があり、標準的なバルク検査では見逃されがちな多様性が存在し、それが感染の治療反応に影響を与える可能性があることを示しています。
抗生物質の作用を秒単位で観る
研究チームは次に、数種類の抗菌処理(一般的な抗生物質や家庭用漂白剤を含む)にさらされた個々のS. aureus細胞を追跡しました。高速イメージング設備により、薬液が細胞に触れた瞬間からその後30分間の変化を捉えました。強力な処理では、NAD(P)Hの信号が低下し、FADの信号が上昇することが多く、これはエネルギー生成の停滞と細胞内部のより酸化された状態へのシフトを反映しています。これらの変化の正確なタイミングやパターンは薬剤の種類や用量によって異なりました。例えば、タンパク質合成阻害薬や細胞壁標的薬は一時的な低下と部分的回復をもたらした一方、漂白剤は急激で持続的な変化を引き起こしました。これらの異なる「光の署名」は、細胞がストレスを受けているか死につつあるかだけでなく、どのようにダメージを受けているかも感知できる可能性を示唆します。 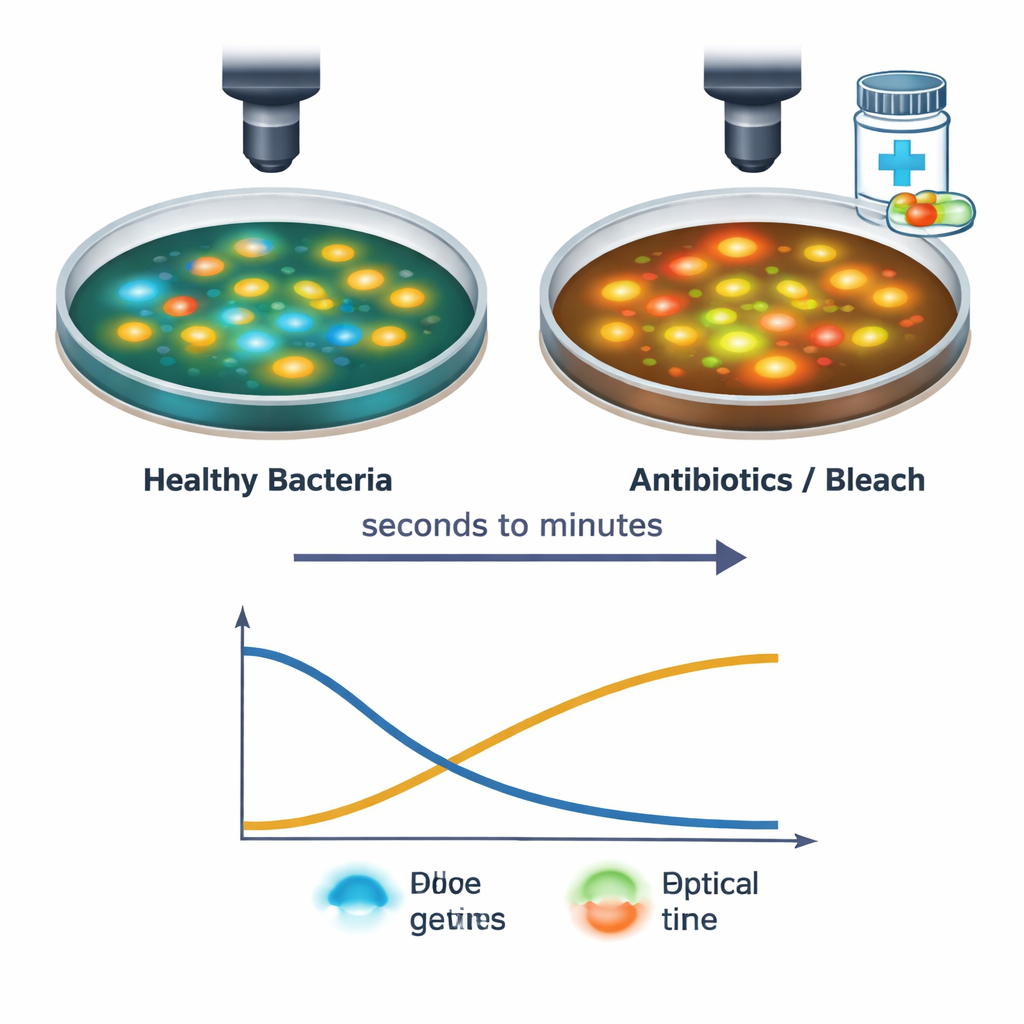
バイオフィルムという隠れた世界をのぞく
自然界で細菌が単独で生きることは稀で、代わりに医療用インプラントから歯に至る表面上に粘性の保護的コミュニティであるバイオフィルムを形成します。こうした高密度の層では、一部の細胞は非常に活発である一方、他は休眠状態にあり、この混在がコミュニティの抗生物質耐性を助けます。研究者たちは大きくスティッチした画像を用いてS. aureusバイオフィルム内の代謝分布をマッピングし、遊走性細胞と比較しました。代謝的に明るく活発なスポットが、より低活性の領域に囲まれて存在することが分かり、複数種にわたりバイオフィルム細菌は遊走性細菌に比べてより酸化寄りの代謝プロファイルを示す傾向がありました。追加の光学シグナルは脂質やタンパク質の存在を示唆しており、バイオフィルムを結びつける接着性物質と一致します。
将来の医療にとっての意義
総じて、標識を用いない光学的代謝イメージングは、細菌がどのように生き、適応し、死んでいくかを迅速に、詳細に、非侵襲的に捉えることができることを示しています。一般読者にとっての要点は、慎重に調整された光だけを用いて細胞を邪魔することなくリアルタイムで細菌のエネルギー利用を「傍受」できるようになったということです。長期的には、この技術により培養が難しい細菌の識別、バイオフィルム内の薬剤耐性細胞の検出、あるいは患者の感染症が異なる抗生物質にどう反応するかの迅速な評価が可能になるかもしれません。これにより、より速く、より個別化された治療の支援や、私たちの日常の健康に影響を与える目に見えない微生物世界の理解が深まることが期待されます。
引用: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
キーワード: 細菌代謝, 光学イメージング, バイオフィルム, 抗生物質反応, マイクロバイオーム