Clear Sky Science · ja
ラクトバチルスをベクターとしたナノボディが、亜臨床壊死性腸炎下のブロイラー生産性を改善し、関連するマイクロバイオームおよびトランスクリプトームの変化を伴う
食卓の鶏肉に直結する、鶏の腸内健康の重要性
現代の鶏舎は綱渡りのような状況にあります:数十億羽を効率的に育てながら、薬剤耐性の原因となりうる抗生物質の使用を削減しなければなりません。ブロイラーにとって最も見えにくい大きな脅威のひとつが、亜臨床壊死性腸炎と呼ばれる腸疾患です。この状態の鳥は外見上はふつうに見えますが、成長が遅く、同じ体重を得るためにより多くの飼料を必要とするため、鶏肉のコストと環境負荷を静かに押し上げます。本研究は、腸内で病原性毒素を無力化するために、善玉菌に小さな抗体断片を持たせるという、高い標的性を持つ新しいプロバイオティクス手法を検討しています。
目立たないが大きなコストを生む腸疾患
壊死性腸炎は、腸内常在菌であるClostridium perfringensが過増殖して強力な毒素を放出することで引き起こされます。重篤な形態では鳥が死亡し明らかな腸損傷を生じますが、より一般的なのは亜臨床型で、NetBやアルファ毒素のような毒素が腸粘膜にわずかな損傷を与えます。これにより鳥は飼料を効率的に消化できず、体重増加が鈍化する一方で外見上の病兆は乏しいままです。世界的に見ると、この目に見えない生産性低下は年間20億米ドル以上の損失を家禽生産者にもたらすと推定されています。歴史的には飼料中の抗生物質で制御されてきましたが、抗菌薬耐性への懸念と「抗生物質未使用」で育てられた鶏を求める消費者の増加により、これら薬剤の受け入れは難しくなり、正確で薬を使わない代替策が急務になっています。
プロバイオティクスを標的毒素阻害剤に変える
研究チームは、プロバイオティクス菌Limosilactobacillus reuteriの二つの株を改変し、非常に小さい抗体断片である「ナノボディ」を分泌させ、NetBまたはアルファ毒素に結合してそれらを中和するという先行研究を基にしています。本研究では、これらの設計プロバイオティクスが、実務的に現実的な軽度の疾病条件に直面したブロイラーの成績を改善できるかを検証しました。43日間の試験で、2000羽以上の鳥を4群に分けました:感染挑戦対照群、一般的な予防用抗生物質(バシトラシンメチレンジサリチレート、BMD)投与群、改変ナノボディ産生株(NE01およびNE06)投与群、そして改変していない親株プロバイオティクス投与群です。全ての鳥はコクシジウム症のワクチンを接種され、その後C. perfringensに曝露されて亜臨床疾患を誘発されました。
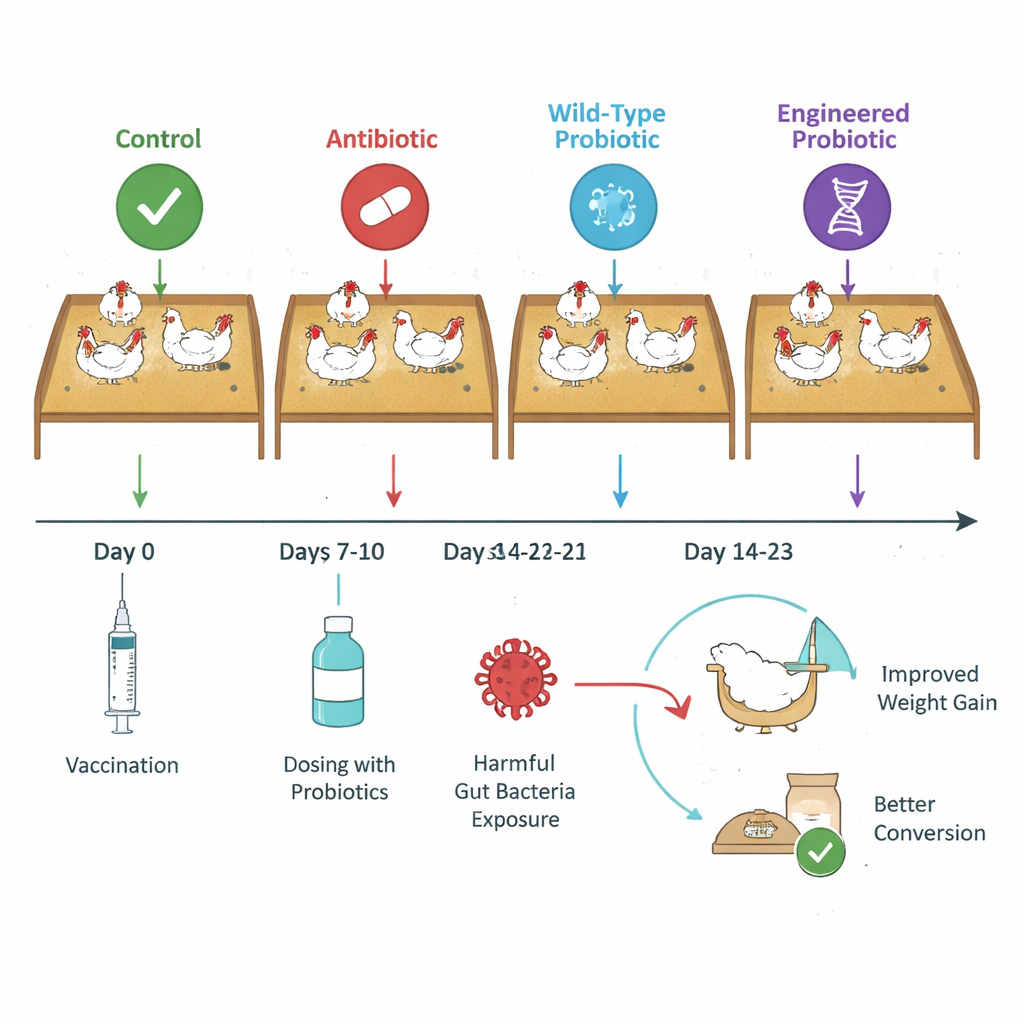
隠れたコストを減らして成長を向上
ナノボディ産生株を投与された鳥は、他の群に比べて一貫して飼料を体重に効率よく換算しました。死亡を調整した飼料変換比は、未処置群と比較して異なる時点で4〜7ポイント(0.04〜0.07単位)改善し、試験終了時には挑戦対照群、抗生物質群、通常のプロバイオティクス群いずれと比べても34〜81グラム重い結果となりました。興味深いことに、目に見える腸病変や糞便および盲腸内容物中のC. perfringens数といった古典的な疾病指標には処置間でわずかな差しか見られませんでした。これは、全ての鳥が類似した低レベルの挑戦を受けていたものの、ナノボディ群はそれに対処する効率が高く、同じ飼料からより多くの肉を生み出していたことを意味します。
落ち着いたマイクロバイオームと静かな免疫応答
成績が向上した理由を理解するため、チームは粗い病理を超えて腸および肝臓のマイクロバイオームと遺伝子発現を調べました。空腸(小腸)内容物のメタトランスクリプトミクス解析は、改変株を投与された鳥でL. reuteriのトランスクリプトとナノボディ遺伝子の発現が検出され、プロバイオティクスが腸内で生存し毒素遮断分子を産生していることを確認しました。総体的な微生物組成は処置よりも鳥の年齢によって主に変化しましたが、ナノボディ群はサンプル間の変動が少なく、より安定で回復力のある腸内コミュニティを示唆しました。機能的には、この群の腸内微生物は発酵やタンパク質合成に関連する遺伝子をより多く発現し、呼吸や硝酸塩利用に結び付く遺伝子をより少なく発現しており、炎症が少ない環境に関連するパターンが見られました。研究者らはまた、動物モデルで抗炎症作用を持つとされる化合物2,3-ブタンジオールを生成する酵素の発現増加も確認しました。
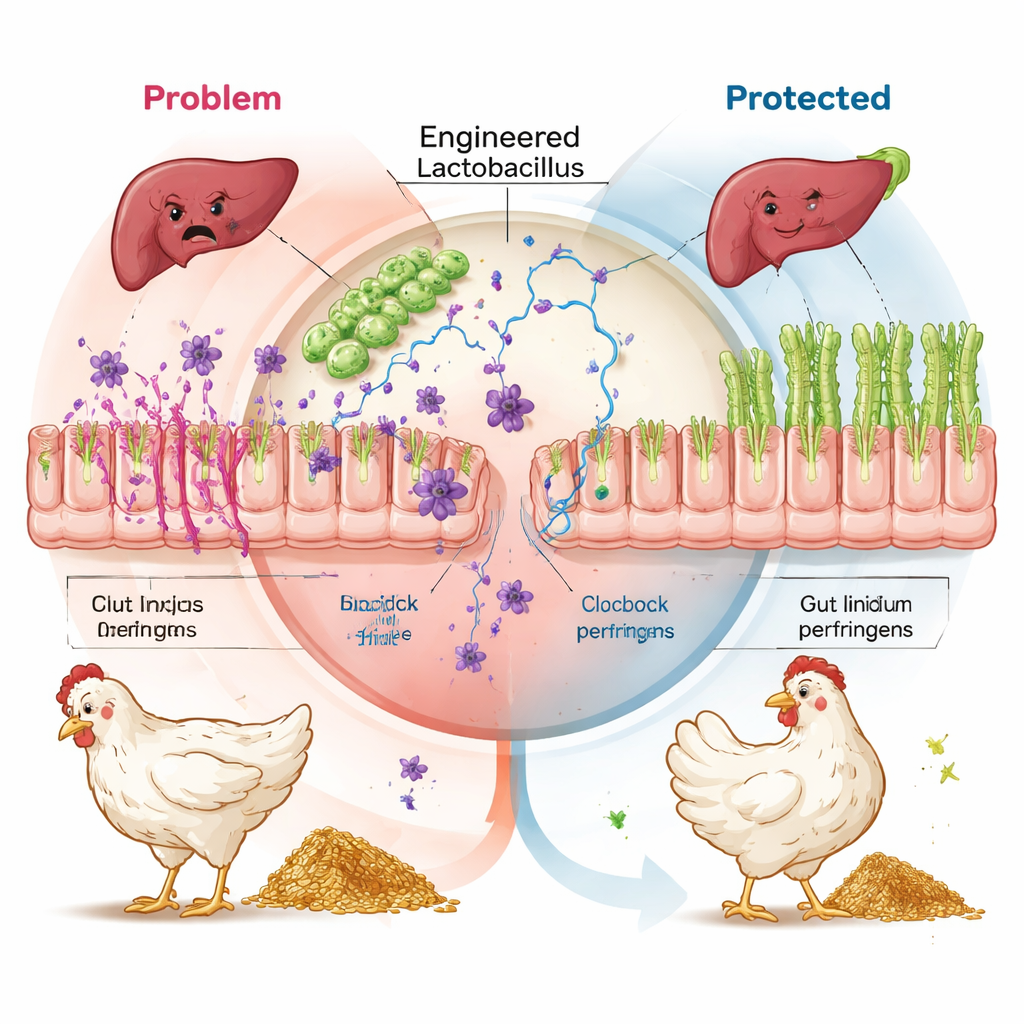
遠隔臓器の保護と効率向上
話は腸にとどまりませんでした。空腸および肝臓の遺伝子発現は、改変プロバイオティクスを与えられた鳥で、挑戦対照群と比べて免疫および酸化ストレス経路の活性化が著しく低く、また多くの場合で抗生物質群や通常のプロバイオティクス群よりも低いことを示しました。肝臓では—細菌毒素による二次的損傷を受けやすい臓器で—ナノボディ群は毒素誘導性障害時に活性化されることで知られるインスリンおよびmTOR経路のシグナルが低下し、一方で抗酸化およびエネルギー産生経路が促進されていました。総合すると、腸表面でNetBおよびアルファ毒素を中和することが、炎症と組織損傷の連鎖を防ぎ、隠れた感染と絶えず戦うことによる大きな代謝コストから鳥を守っていることが示唆されます。
鶏や人体の将来の健康への含意
一般読者にとっての主なメッセージは、すべての「プロバイオティクス」が同じではないということです。役立つ菌に正確に標的化されたナノボディを装備させることで、研究者らは従来の抗生物質に頼らずに、一般的でほとんど目に見えない腸疾患から鶏を保護する生きた治療法を作り出し、抗生物質レジメンや標準的なプロバイオティクスの双方を上回る成果を示しました。鳥は市場体重に達するまでにより少ない飼料で済み、内部ストレスの兆候も少なくなりました。同様の戦略が他の家畜、そして最終的には人間にも拡張できれば、改変プロバイオティクスは有益な微生物を保持しつつ有害な腸毒素を無力化し、抗生物質耐性の拡大を遅らせる強力な手段を提供する可能性があります。
引用: Hall, A.N., Manuja, S., Payling, L.M. et al. Lactobacillus-vectored nanobodies improve broiler productivity under sub-clinical necrotic enteritis with associated microbiome and transcriptome changes. npj Biofilms Microbiomes 12, 52 (2026). https://doi.org/10.1038/s41522-026-00916-w
キーワード: 改変プロバイオティクス, 壊死性腸炎, 家禽の腸内健康, ナノボディ, 抗生物質の代替