Clear Sky Science · ja
CASD1触媒におけるSLC33A1依存および非依存ゴルジ酸性糖質のO-アセチル化の相互作用
健康と疾病を形作る小さな糖の改変
私たちの細胞は複雑な糖鎖で覆われており、それらは分子レベルの身分証明書のように働いて免疫反応や発生、さらにはウイルスの結合様式を導きます。本研究は、末端糖であるシアル酸に小さな化学的「キャップ」であるアセチル基を付加するという、ささやかだが強力な修飾に着目し、細胞内のゴルジ体でこの過程を制御する予想外の二段構成の分子機構を明らかにします。この隠れたシステムを理解することは、いくつかの重篤な神経障害の説明に役立ち、健康や病気における細胞表面の微調整の手がかりを与えます。 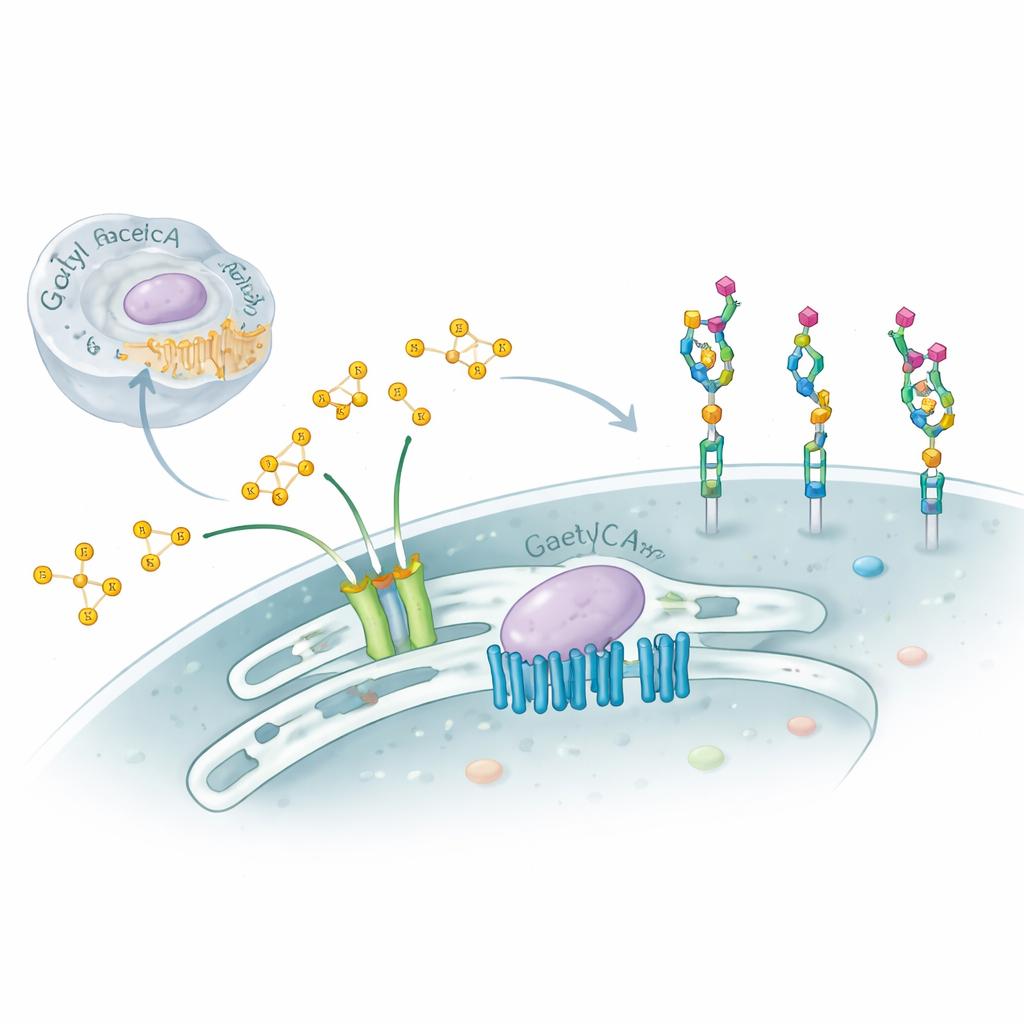
細胞表面にある特別な糖
シアル酸はタンパク質や脂質の多くの細胞表面糖鎖の末端に位置し、特に脳に存在するガングリオシドに豊富です。シアル酸に対して、特定の位置に一つまたは二つのアセチル基を付加するなどのわずかな修飾を加えることで、既存の認識部位を隠したり新たに作り出したりできます。インフルエンザCや一部のコロナウイルスはこうした修飾糖を特異的に認識し、アセチル化されたガングリオシドは神経細胞の生存や死、さらにはがんの増殖に影響を与えることがあります。それにもかかわらず、ゴルジでこれらのアセチル基を付ける細胞内機構の詳細は、長く十分に理解されていませんでした。
輸送体と酵素が手を取り合う
研究者たちはゴルジ付近に存在する二つのタンパク質に注目しました。SLC33A1は膜を越えてアセチルCoA(細胞の主要なアセチル供与体)を輸送する輸送体であり、CASD1はシアル酸へアセチル基を転移する酵素として知られています。ヒトおよびハムスターの細胞株で遺伝子編集を用い、SLC33A1を欠損させて特定のガングリオシドに何が起こるかを観察しました。SLC33A1を欠く細胞は基本的なガングリオシドであるGD3とGD2は依然として作れましたが、がんや神経機能に関連する目印である9-O-アセチル化型は完全に失われました。ヒトのSLC33A1を再導入するとこれらのアセチル化ガングリオシドが回復し、SLC33A1がこの経路におけるアセチルCoAの重要な供給源であることが示されました。 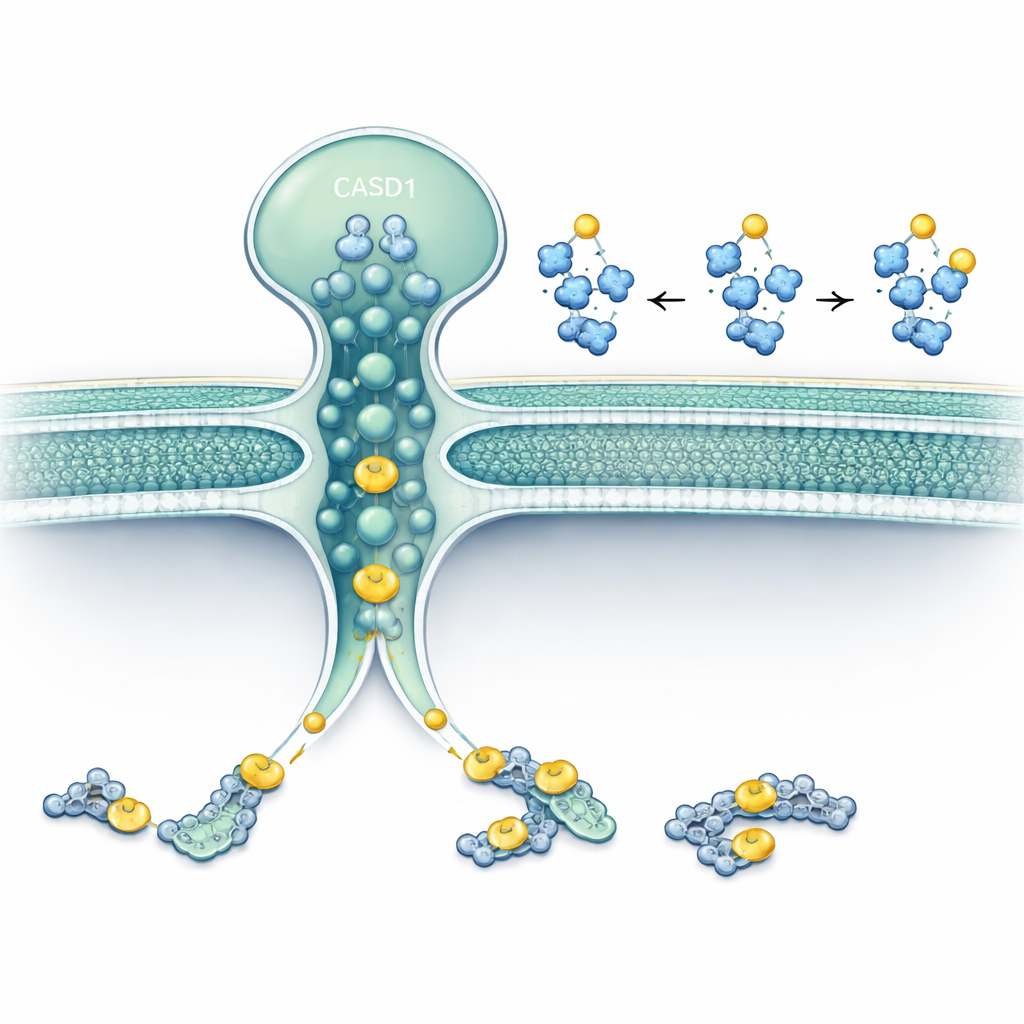
患者変異が示す医学的意義
SLC33A1は重篤な小児疾患(Huppke–Brendel症候群)や家族性痙性対麻痺の一型、遅発性小脳失調など、いくつかのまれな神経疾患に関与してきました。研究チームは患者由来のSLC33A1変異体を四種類、正常な輸送体を欠く細胞に再現し、これらの変異タンパク質がガングリオシドのアセチル化を回復できるかを検証しました。四つとも機能低下を示し、最も重篤な小児発症の変異はほとんどアセチル化を回復できませんでした。最近解かれたSLC33A1の三次元構造を手がかりに、著者らはこれらの変異をタンパク質上に写し、構造やアセチルCoA結合能を損なう可能性を示しました。これらの結果は、ガングリオシドのアセチル化障害が患者に見られる神経症状に寄与していることを強く示唆します。
CASD1に隠された第二の活性部位
さらに研究は予想外の事実を明らかにしました。CASD1は二重の機能を持つ酵素であるように見えるのです。ゴルジ腔内にある既知の領域はSLC33A1が供給するアセチルCoAを使います。しかしSLC33A1を欠損させても、ある条件下では細胞は特定のシアル酸に単一のアセチル基を付けることができ、より複雑な二重アセチル化パターンに必要な二つ目の付加はできませんでした。高度な構造予測と分子シミュレーションを用いて、著者らはCASD1の膜貫通領域がリソソームに存在する既知の膜内アセチルトランスフェラーゼと類似していることを示しました。この領域の重要なアミノ酸残基が細胞質側でアセチルCoAに結合し、そのアセチル基を膜を通して直接シアル酸に渡すと同定されました。これらの残基を変異させると、CASD1は試験管内アッセイおよび生細胞でこの第二の活性を失いました。
二つの経路、一本の緻密に調節された糖コード
これらのデータは「二つの触媒部位」モデルを支持します。一つの経路はSLC33A1がアセチルCoAをゴルジ腔内に運び、CASD1の腔内ドメインがシアル酸にアセチル基を付加して単純な修飾や二重修飾の両方を可能にします。もう一つの経路はCASD1の膜貫通コアに組み込まれており、細胞質のアセチルCoAへ直接アクセスして、SLC33A1が欠けているときでも基本的なレベルのアセチル化を行えます。一般的に言えば、これは一つの酵素が二つの異なるアセチル供給源によって支えられ、細胞表面の糖に微妙な「句読点」を書き込むことを意味します。輸送体や酵素のいずれかの部分が故障すると、これらの印がずれたり欠落したりし、それが特定の神経発達障害や神経変性疾患の説明につながる可能性があり、細胞が外側のアイデンティティを形作る新たな制御層を浮き彫りにします。
引用: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
キーワード: シアル酸, ゴルジでのアセチル化, ガングリオシド, SLC33A1, CASD1