Clear Sky Science · ja
ユビキチン非依存的基質分解中のミドノリン—プロテアソーム複合体の構造動態
細胞が急いでゴミを片付ける仕組み
細胞内ではタンパク質が常に合成され、分解されています。多くのタンパク質はユビキチンという小さな分子で標識されたのち、細胞の主要なリサイクル装置であるプロテアソームに送られます。しかし、核内の一部のタンパク質は非常に迅速に除去されなければならず、標識する時間がありません。本研究は、あまり知られていない補助タンパク質ミドノリンがプロテアソームに直接結合してこれらの緊急ターゲットを排除する仕組みを明らかにし、細胞が遺伝子活性を迅速かつ厳密に制御する手がかりを提供します。
細胞のシュレッダーへの近道
26Sプロテアソームは樽状の複合体で、タンパク質を小片に分解します。従来はユビキチン鎖を読み取って標的を認識することで知られていました。最近の研究により別の経路が明らかになりました:ミドノリンが一部の核内タンパク質、特に遺伝子のスイッチを迅速に入れ替える即時早期遺伝子産物を、ユビキチン標識なしに直接プロテアソームへ案内する“近道”です。応答性の高い転写因子などのこれらのタンパク質は数分以内に出現・消失する必要があります。本論文は高解像度クライオ電子顕微鏡と生化学実験を組み合わせ、ほぼフレームごとにミドノリンがどのようにプロテアソームに取り付き、貨物を分解のために配置するかを描き出しています。
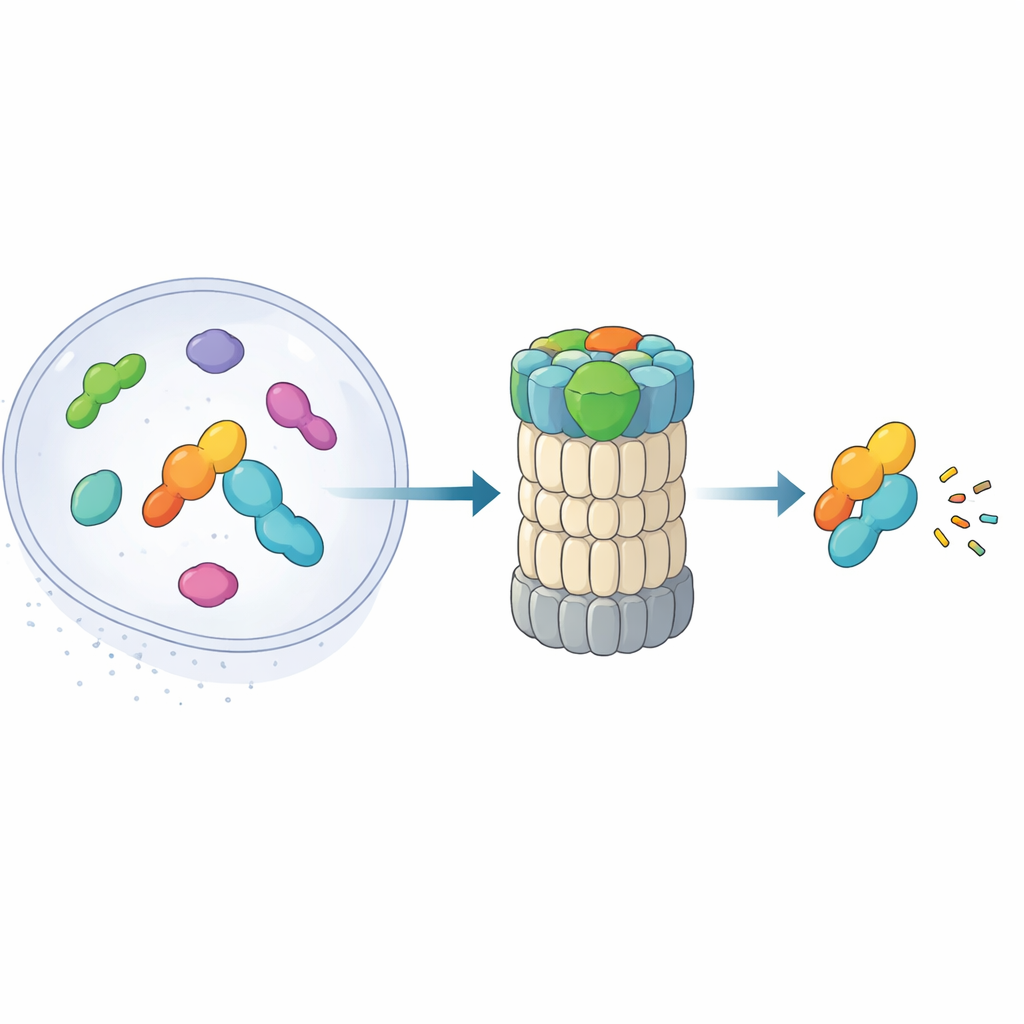
標的を掴み狙いを定める三つのモジュール
ミドノリンは三つの主要モジュールを備えた多機能ツールのように働きます。一端のC末端ヘリックスはプロテアソーム成分RPN1上のドッキング部位に差し込み、ミドノリンをプロテアソームに固定します。中央の「キャッチ」領域は標的タンパク質の特定の鎖状特徴(デグロン)を認識してしっかり捕らえます。反対側にはユビキチン様ドメインが位置します。意外なことに、このドメインは他のシャトルタンパク質で見られるような主なプロテアソーム結合部位ではありません。むしろ著者らは、ユビキチン様ドメインが通常基質からユビキチンを切り離す酵素であるRPN11に寄り添うことを示しています。ここではRPN11は足場のように働き、ミドノリンのユビキチン様部分を受け入れることで、キャッチ領域とその結合貨物をプロテアソームの狭い入口孔の直上に保持するのを助けます。
タンパク質を研削コアへ誘導するしくみ
ミドノリンがドッキングした後は、プロテアソームのエネルギー駆動モーターであるAAA+ ATPアーゼリングが引き継ぎます。このリングは入口孔のすぐ下に位置し、未折りたたみ状態のタンパク質鎖を一段ずつ中核へ引き込みます。クライオEMのスナップショットは、基質を中央通路に沿って掴み渡す際にモーターの6つのサブユニットが採る“らせん階段”様の一連の位置を示しています。著者らはこのサイクルの連続する4段階を捉え、いずれもミドノリン結合物が孔を通して通されている状態でした。さらに一つのサブユニットでマグネシウムイオンの解放が環全体の下方移動と同時に起きる様子も観察されました。これは協調したATP使用とマグネシウムの放出が、切断部位のあるチャンバーへタンパク質を段階的に押し込むラチェット機構を助けることを示唆します。
配置と共発現が重要な理由
研究チームは各ミドノリンモジュールが効率にどう寄与するかを検証しました。アンカリングヘリックス単体はRPN1に結合できますが、プロテアソーム活性を大きく高めることはできません。キャッチ領域を除くと、ミドノリンが付着しても多くのプロテアソームが基質非結合の待機状態に留まりますし、キャッチを恒常的に融合した基質に置き換えても完全な活性は回復しません。これらの結果は、キャッチが単に標的を掴むだけでなく、孔の入り口でタンパク質を精密に向ける役割を果たす必要があることを示します。生化学的データと腫瘍トランスクリプトーム解析からも、ミドノリンはしばしばその基質と共に発現する傾向があることが示されています。共発現するとミドノリンはより良く折りたたまれ安定な複合体を形成し、細胞が遺伝子発現をリセットする必要があるときに迅速にプロテアソームへ届けられる“分解してくれ”パッケージを準備します。
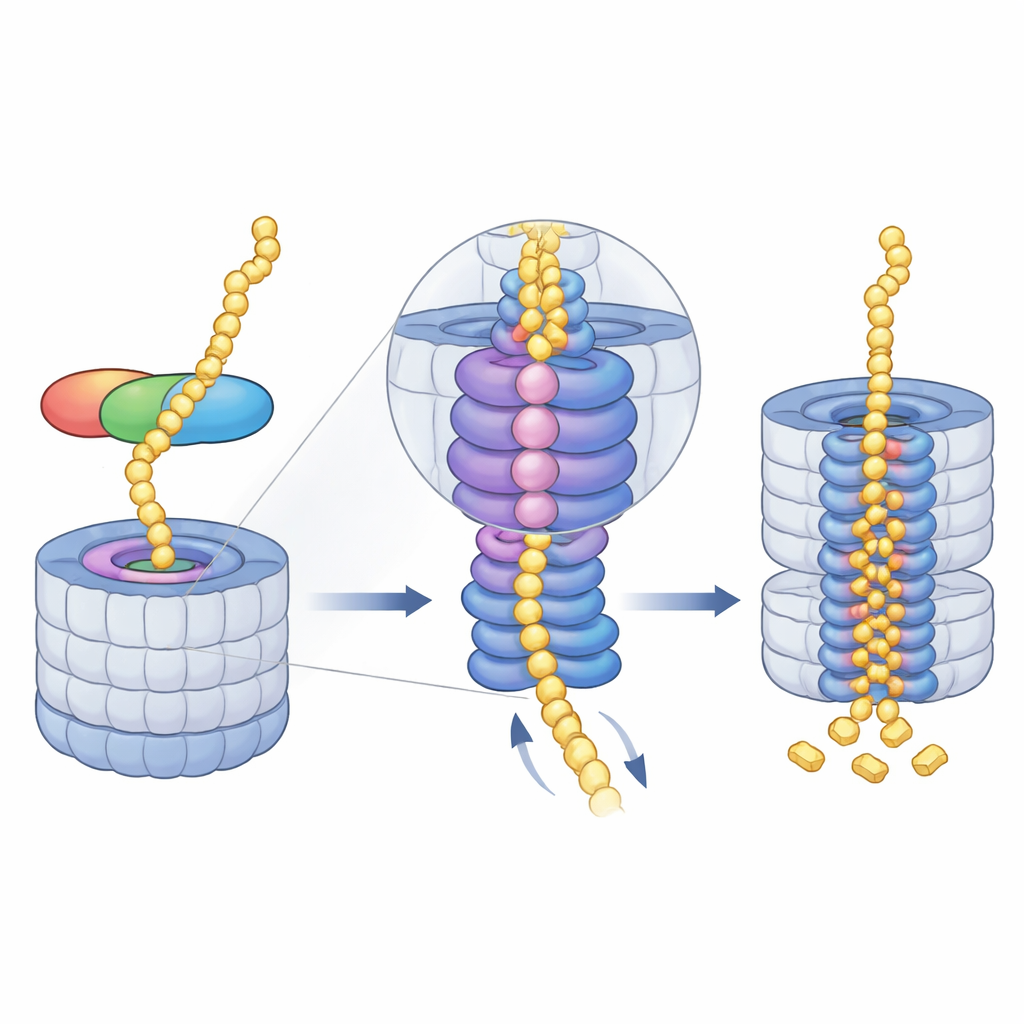
自己分解と将来の医療応用
標的タンパク質が引き込まれ分解された後、ミドノリン自身も免れません。ミドノリンの非構造領域はモーターにスレッドされて同じ分解室に送られ、補助因子が不必要に蓄積しないようにします。このユビキチンを介さないプロテアソーム経路を解明することで、細胞が極めて短時間のスケジュールでタンパク質寿命を管理する仕組みへの理解が深まります。また、ミドノリンを基に疾患原因となる核内タンパク質を直接プロテアソームに結びつけるような分子を設計すれば、特定のがんドライバーを含む“薬で狙いにくい”標的をより迅速かつ選択的に除去できる可能性を示唆しています。
引用: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
キーワード: プロテアソーム, ミドノリン, タンパク質分解, ユビキチン非依存経路, 即時早期遺伝子