Clear Sky Science · ja
転写能が孤立したMSR単位のヘテロクロマチン核形成能力を規定する
DNAに潜む隠れたスイッチ
ゲノムは細胞核内に主に二つの状態で収納されています。遺伝子が働く活性領域と、長い間「遺伝学的ダークマター」と考えられてきた高密度に詰まった領域です。本研究は一見単純な問いを投げかけます:あるDNA領域がまずヘテロクロマチンと呼ばれる密に詰まった遺伝子を抑える物質になることを何が決めるのか?マウスの特定の反復配列を精査することで、著者らはすべての反復配列が同じではないことを明らかにします。特殊な種類の転写を支えられる配列だけが、これらの沈黙したDNA近傍を構築し維持するスイッチを入れられるのです。
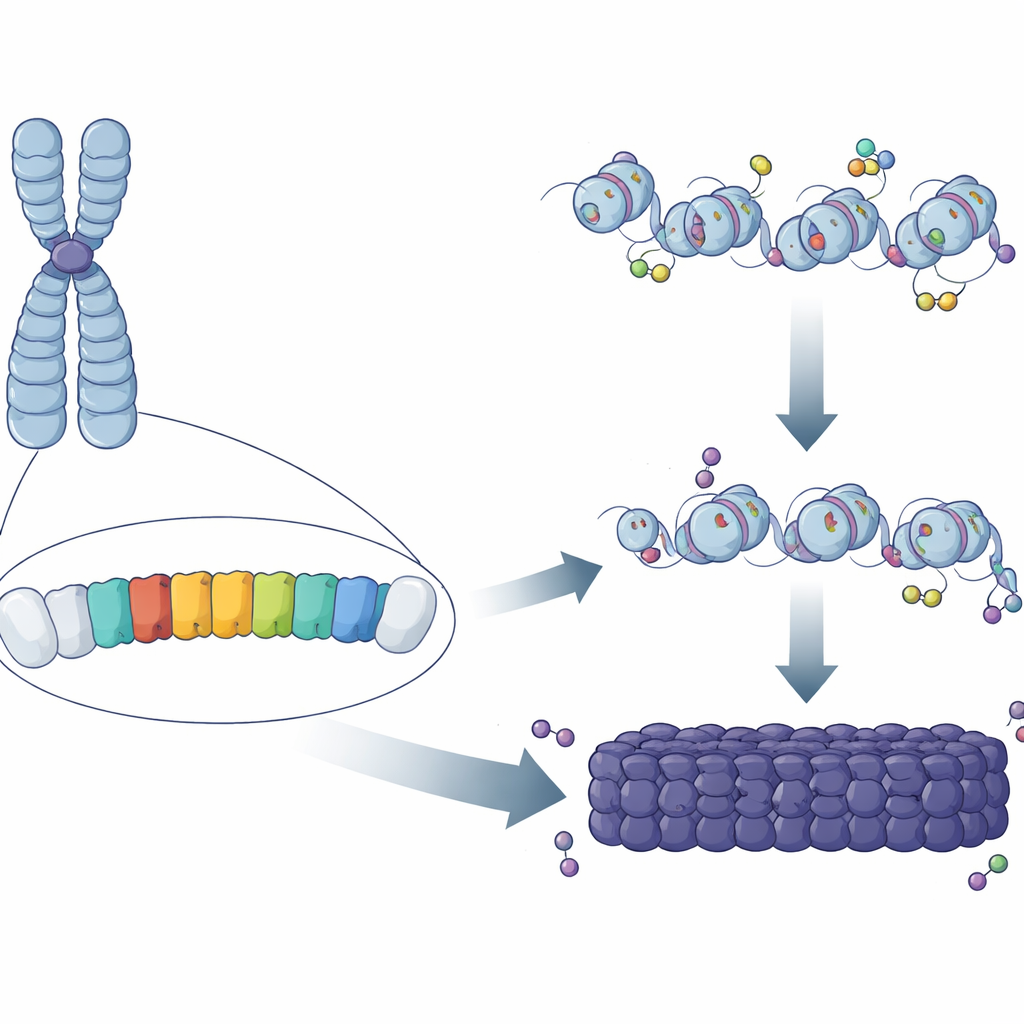
ゲノムの繰り返しパターン
ほぼ半分の哺乳類DNAは反復配列でできており、多くは染色体の中心付近にクラスターしています。マウスではこれらの領域の主要構成要素の一つが「メジャー・サテライト・リピート(MSR)」で、A/Tに富む短い配列が何十万回もコピーされています。古典的な研究は、これらの領域が化学的マークやタンパク質で覆われ、DNAをコンパクトで保護的な状態に固定していることを示しました。しかし、なぜ一部のMSRコピーが完全にヘテロクロマチン化し、ゲノムの別の場所に散在するものはそうならないのかは謎のままでした。著者らは、個々のMSR単位の配列や挙動のわずかな違いが、ヘテロクロマチンのパッチを「核形成(ニュークリエイト)」できるかどうかを決めるのではないかと推論しました。
ゲノム内に試験サイトを構築する
この考えを明快に検証するため、チームはマウス胚性幹細胞を操作して第2染色体の静かな伸長部に人工のランディングパッドを挿入しました—近辺に遺伝子や反復がなく、検出可能な活性がない中立領域です。この中立サイトに、完全なMSR単位、強くスクランブルしたMSR変異体、ウイルス性プロモーターや移動因子の断片などの対照要素を挿入しました。これにより、単位ごとにどの配列がヘテロクロマチンの特徴であるH3K9me3というヒストンの化学的修飾、HP1タンパク質の結合、リンカーヒストンH1の組み込みといった標識を引き付けられるかを調べられるようにしました。これらは総じて局所のクロマチンを厚く安定化させます。
転写準備が整った反復だけが沈黙クロマチンを核形成する
結果は非常に選択的でした。試験サイトに単一の完全なMSR単位を挿入してもクロマチンは変化しませんでした。しかし、完全なMSR配列が三コピー以上連続で並ぶと、周辺領域は強いH3K9me3、HP1、ヒストンH1を伴うヘテロクロマチンの「島」に変わりました。対照的に、同じ長さのスクランブルされたMSR配列や別の反復型(LINE-1の5'非翻訳領域)はそうした変化を引き起こさず、たとえ強い転写を駆動できても同様でした。重要な違いは、多コピーの完全なMSR単位が控えめで双方向的な転写を支持し、短く標準的でないRNA分子を生成してそれらがクロマチンに密接に結びつく点でした。このパターンこそが、高レベルの遺伝子様転写ではなく、ヘテロクロマチンを核形成する能力と相関していました。
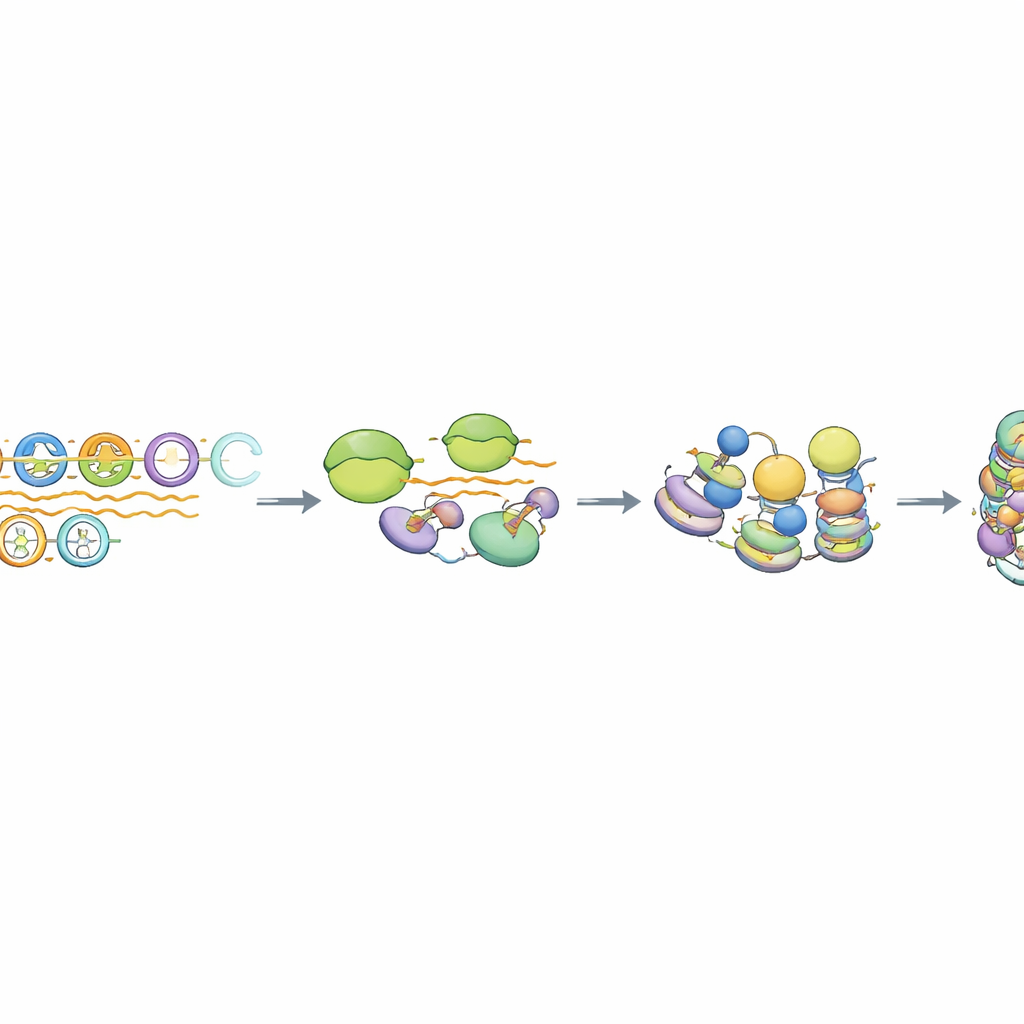
特異な転写とRNA処理
さらに掘り下げると、著者らは通常メッセンジャーRNAを合成する酵素であるRNAポリメラーゼIIがMSR配列に一時的に関与するが、効率的に長い転写を進めないことを見出しました。その結果生じるRNAは保護的な5'キャップや長いポリA尾を欠き、それを生み出したDNAの近傍に留まります。特定の非コードRNAの切断と終結で知られるインテグレーター複合体が、完全なMSR単位に特異的に濃縮していました。インテグレーターの切断活性を低下させるとMSR由来RNAの量は大幅に上昇しましたが、主要な抑制的ヒストンマークは持続し、HP1の結合はわずかに変化しました。ゲノムワイド解析は、最も完全に近い約10–15%のMSRコピーのみがこのように振る舞うことを示し、転写結合によるサイレンシング経路に適合した“能力を持つ”反復のサブセットを浮き彫りにしました。
プロモーターを模したほどけたDNA構造
チームはMSR DNA自体がどのようにしてこの異例の転写を助長するかも調べました。多コピーのMSR配列(単一や二コピーではなく)は、局所的にほどけたDNAやRNA:DNAハイブリッドの明確な兆候を示しました。これらは活性プロモーターやポーズサイトでよく見られる構造的特徴です。これらの構成はトポイソメラーゼを阻害すると増強され、MSR転写の増加とより強いヘテロクロマチン特徴の同時発現を伴いました。著者らは、三コピー以上の連続したMSR単位がプロモーターを模倣する物理的なDNA位相を作り出し、ポリメラーゼや転写因子を誘引して短いRNAを生成させ、それらが特定のタンパク質とともにコンパクトなクロマチン構造を強化すると提案しています。
ゲノムの健康にとっての意義
一般の観察者にとって、この研究は私たちの「ジャンク」DNAの一部が注意深く調整されたスイッチとして機能し、DNAの形状、低レベルの転写、RNA処理の組み合わせを用いてゲノムの保護シェルを構築していることを明らかにします。この制御された非メッセンジャー転写を支えられるMSR単位だけが新たなヘテロクロマチンを点火でき、スクランブルされたものや過度に活性な要素はできません。このDNA/RNAに基づく論理は、細胞がどの領域を沈黙させ、どの領域を遺伝子の宿る場として許すかを識別するしくみ、そして制御の乱れたサテライトRNAががんや発生異常と結びつく理由を説明する助けになります。本質的に、本研究はゲノムの反復的な“背景”が受動的な詰め物ではなく、核の構造と安定性を積極的に設計する存在であることを示しています。
引用: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
キーワード: ヘテロクロマチン, サテライトDNA, 非コードRNA, クロマチン構造, ゲノム安定性