Clear Sky Science · ja
ティモサポニンAIIIはCAR-T細胞の効力を高め、CAR-Tregを障害して再発を防ぐ
免疫のブレーキを弱めてがん治療を強化する
攻撃的な血液がんの患者にとって、CAR-T細胞療法は人生を変える可能性があります。患者自身の免疫細胞を再プログラムして腫瘍細胞を追跡・排除させるからです。しかし、多くの患者はこうした改変細胞の効力が低下して再発します。本研究は植物由来の分子、ティモサポニンAIII(TAIII)を調べ、免疫系の重要なブレーキを選択的に無効化することでCAR-T細胞の活性を長持ちさせ、これらの療法をより耐久性と効果の高いものにする可能性を示しています。
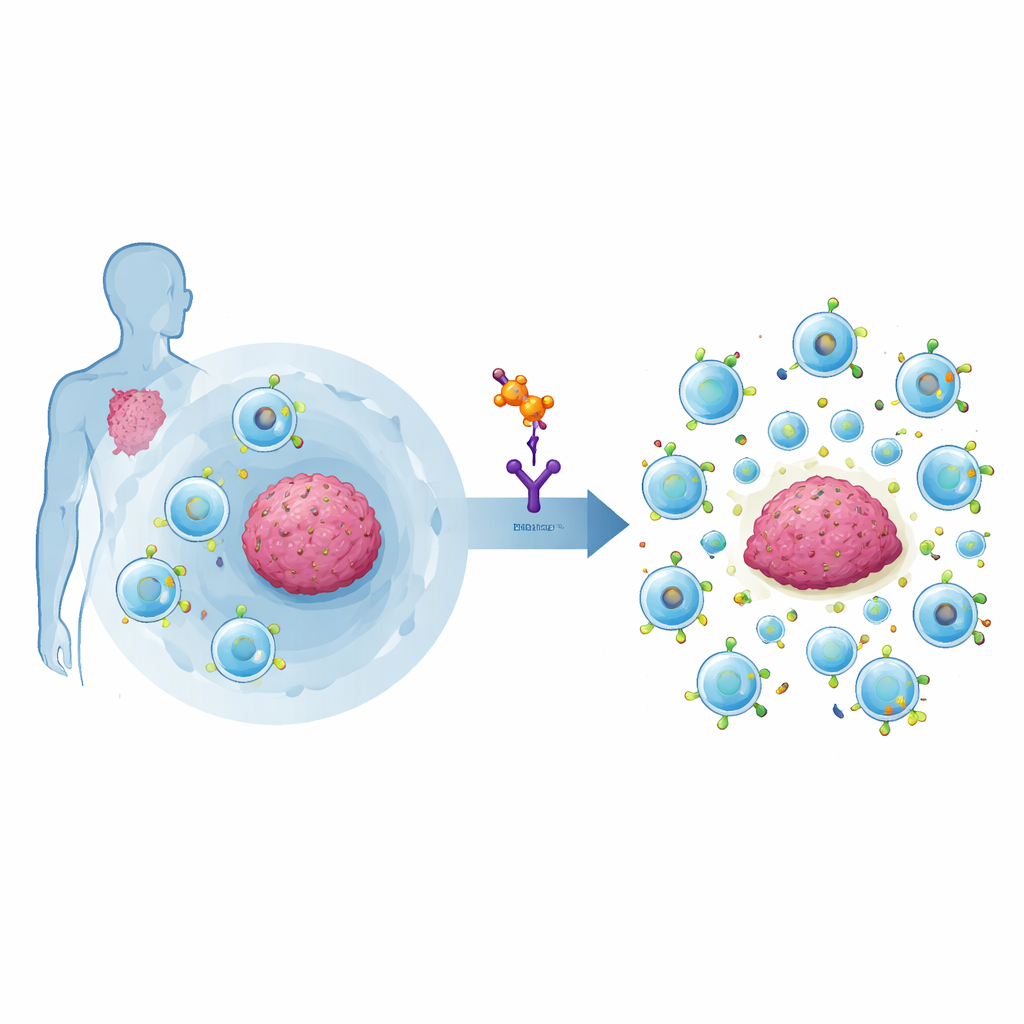
なぜ強力ながん戦士が失速するのか
CAR-T細胞は、悪性B細胞上のCD19などのがん標的を認識する人工的なセンサーを持たせたカスタム免疫細胞です。しかし実際の患者では、長期寛解を得られるのは半数程度にとどまります。主な原因の一つが制御性T細胞(Treg)という特殊な免疫細胞の亜集団です。本来Tregは免疫が健康な組織を攻撃するのを防ぎますが、がんの状況では抗腫瘍応答、特にCAR-T細胞の活動を抑え込んでしまいます。最近の臨床データは、CAR-T製品にTregが多く含まれると治療抵抗性や再発のリスクが高まることを示しました。残念ながら、既存のTreg枯渇薬は往々にして粗い道具であり、有益な免疫細胞まで傷つけてしまいます。
薬用植物に見つけた穏やかな助っ人
研究者らは、Tregの中枢制御スイッチであるタンパク質FoxP3がオフになると免疫活性化が抑えられることを報告するスクリーニング系を構築しました。3000を超える天然物や承認済み化合物を試し、細胞を殺さずにFoxP3の抑制を緩められるものを選び出しました。その候補の一つが際立っていました:ティモサポニンAIII(TAIII)。これは漢方薬材の知母(Anemarrhena asphodeloides)に含まれるステロイド様分子で、局所用抗炎症剤として臨床試験が進んでいます。通常はTregへと分化する条件下で培養したヒトT細胞において、TAIIIはこれらの抑制性細胞の形成と機能を強く低下させ、他のT細胞タイプは概ね保たれました。これはTAIIIが免疫を抑制から攻撃へとそっと傾ける可能性を示唆します。
小分子がCAR-T細胞を解き放つ仕組み
メカニズムを掘り下げるために、研究チームは化学プローブ、タンパク質結合試験、コンピューターモデリングを用い、TAIIIがアデノシンA2A受容体(A2AR)に結合することを突き止めました。A2ARは腫瘍内の高濃度アデノシンに応答するよく知られた免疫の“オフスイッチ”です。TAIIIは主要な結合部位を単に遮断するのではなく、細胞膜中のコレステロール感受性領域に楔(くさび)を打ち込むように入り込み、アロステリック阻害剤として働きます。コレステロール様脂質を置換し、最終的にCREBというタンパク質に至るシグナル伝達を抑えることで、TAIIIはFoxP3の産生を低下させTregプログラムを弱めます。A2ARをT細胞やCAR-T細胞から除去するとTAIIIの効果が失われたことから、この受容体が重要な標的であることが確認されました。
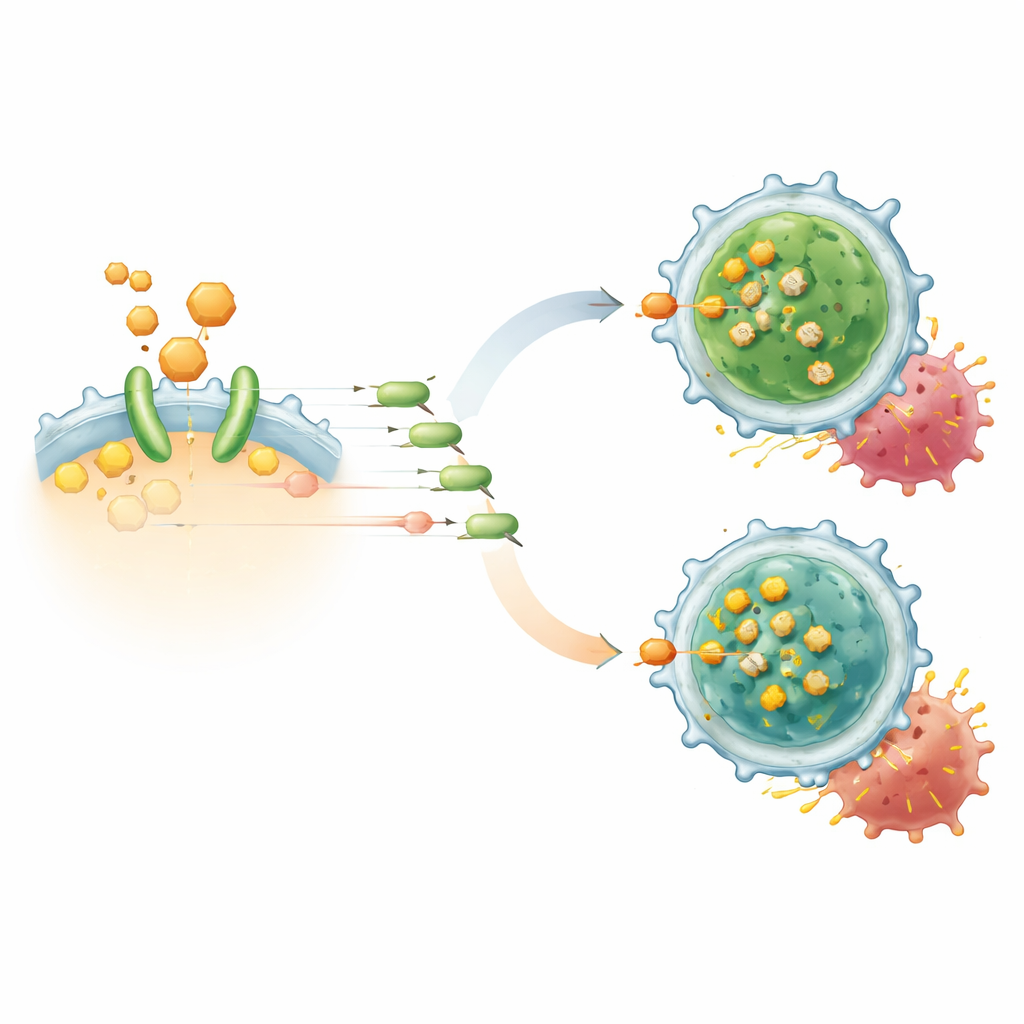
モデル系で得られたより強く長続きするCAR-T応答
培養した共培養実験では、ヒトのCD19 CAR-T細胞にTAIIIを加えるとリンパ腫細胞を殺す能力が高まり、インターフェロン-γやIL-2といった攻撃分子の放出が増加しました。同時に、Treg様の性質を持つCAR-T細胞の割合が縮小し、持続的な保護と関連するセントラルメモリーT細胞が促進されました。単一細胞RNAシーケンシングでは、TAIII処理されたCAR-T集団にFoxP3高発現の制御性細胞が少なく、より活発なキラーT細胞が多いことが明らかになりました。複数の血液がんおよび固形腫瘍のマウスモデルで、TAIIIとCAR-T療法の併用は腫瘍増殖を遅らせ、反応を深め、後期の再発を劇的に減らしました。実験的にCAR-T製品からTregを取り除くとTAIIIはもはや有益性を示さなかったため、その主な作用は全てのT細胞を過剰刺激することではなく、この抑制的な亜集団を解体することにあると強調されます。
CAR-Tを越えて:腫瘍免疫環境の再配線
TAIIIの効果は改変細胞に限られませんでした。免疫機能が保たれたマウスの固形腫瘍では、毎日のTAIII投与により腫瘍内のTreg数が減少し、CD8の“キラー”T細胞の浸潤が増え、抗腫瘍性サイトカインのレベルも上昇しましたが、明らかな毒性や体重減少は見られませんでした。さらに、抗PD-1チェックポイント療法と組み合わせるとTAIIIは腫瘍制御を増強し、有益なメモリー様T細胞を拡大しました。重要なことに、機能的なT細胞を欠く重度免疫不全マウスではTAIIIの効果はほとんど見られず、その抗がん活性はがん細胞を直接毒するのではなく免疫応答を再構築することに依存していることを示しています。
将来のがん医療にとっての意味
一般向けに言えば、著者らは免疫系の内部ブレーキの一つを選択的に緩める方法を見つけた、ということです。燃料ラインを断つこともアクセルを全開にすることもせず、A2A受容体との精密な相互作用を通じて制御性T細胞を調整することで、ティモサポニンAIIIはCAR-T細胞が活性を維持し、より長寿命のメモリー集団を形成し、腫瘍環境によって沈黙させられるのを防ぎます。前臨床試験および患者由来CAR-T細胞での試験では、これがより強力な腫瘍殺傷と再発の減少につながりました。安全性と有効性を人で確認するためには臨床試験が必要ですが、TAIIIは最先端の免疫療法をより長持ちさせ、より広く成功させうる有望な植物由来の付加治療として浮上しています。
引用: Hou, M., Zhang, W., Qi, Z. et al. Timosaponin AIII enhances CAR-T cell potency and prevents relapse through impairing CAR-Tregs. Nat Commun 17, 3045 (2026). https://doi.org/10.1038/s41467-026-70867-5
キーワード: CAR-T細胞療法, 制御性T細胞, アデノシンA2A受容体, ティモサポニンAIII, がん免疫療法