Clear Sky Science · ja
合成アプタマー機械受容体はDNA回路を介して細胞特異的な力の検出と時間制御を可能にする
柔らかな引張りで細胞の声を聴く
私たちの体内では、細胞が周囲に対して常に押したり引いたりしており、その微小な力を用いて増殖、移動、分化のタイミングを決めています。本研究は、特定の細胞種に合わせて調整でき、時間的にオン/オフを切り替えられるDNAベースの装置を用いて、こうした力を傍受する新しい方法を示します。この技術は将来的に、組織の成長を設計したり、腫瘍の挙動を理解したり、生きた細胞にリアルタイムで反応するスマート材料を設計したりするのに役立つ可能性があります。
DNAを微小な機械的スイッチとして使う
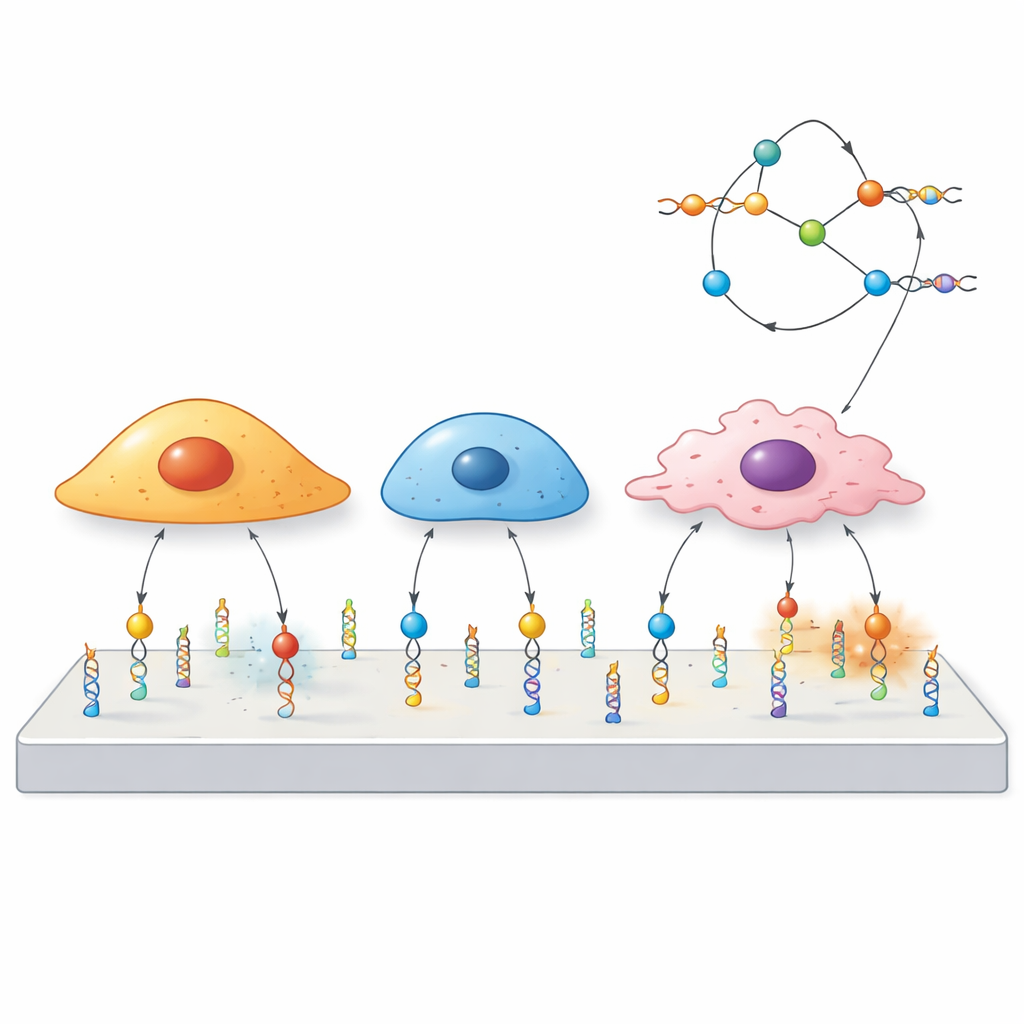
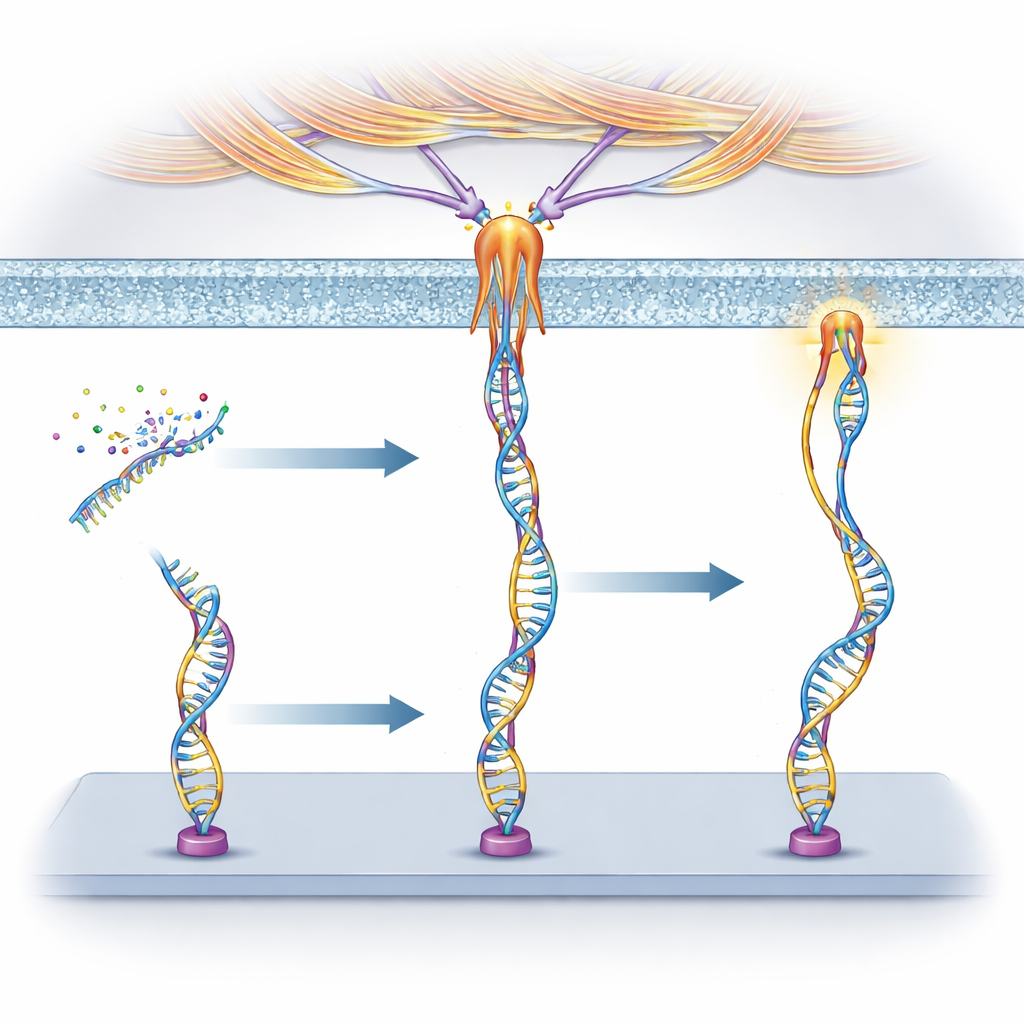
研究者らは遺伝情報を担う分子であるDNAから「メカノプローブ」を構築しました。各プローブは三つの要素で構成されています:標的の細胞表面タンパク質に結合する短いDNA配列(アプタマー)、一定の力で切断するよう調整されたばねのように振る舞う対になったDNAセグメント、そしてそのばねが外れたときに光る蛍光色素です。細胞がアプタマーで捕らえた受容体を十分な力で引くとDNA二重鎖が開いてシグナルがオンになります。アプタマーを変えることで、どの細胞やタンパク質がプローブを作動させられるかを事前に決められます。
細胞表面に潜む力の経路を見つける
既存の力センサーの多くは、細胞が周囲にしがみつくのを助け、多くの細胞種に共通するインテグリンに焦点を当てており、選択性が限られます。本研究ではむしろ、通常は機械的役割で注目されない「非正統的」受容体を標的にしました。がん細胞に多く見られるヌクレオリンというタンパク質に結合するアプタマーAS1411は、標的を特異的に認識できる場合にのみシグナルを出すことを示しました。開くのに弱い力か強い力かを要求するプローブを設計することで、ヌクレオリンはインテグリンと比べて穏やかな力を伝達し、それだけでは細胞の表面での広がり(スプレッディング)を助けないことがわかりました。対照的に、受容体PTK7に結合するアプタマーSgc8は、細胞がほとんど付着していないときでも力を報告し、リング状のパターンを形成して異なる運動源を示唆しました。
力がどこから来るかをたどる
これらのDNAデバイスを何が引いているのかを理解するため、研究者らは異なる細胞プロセスを選択的に遮断する薬剤を用いました。ヌクレオリンの場合、その力は筋収縮を助けるモータータンパク質であるミオシンに強く依存し、細胞が剛性を検知するために用いる特別な接着点であるフォーカルアドヒージョンの部位に現れました。これはヌクレオリンが細胞内のアクチン–ミオシン機構と間接的に結びつき、その収縮力を共有しうることを示唆します。一方PTK7では、細胞が膜を波立たせて液体を取り込むマクロピノサイトーシスを阻害するとシグナルが大幅に減少しました。力は主に小胞化の後半ではなく、アクチン成長に駆動される初期の膜ラフリングから生じており、異なる機械的経路を明らかにしました。
分子レベルの精度で細胞選択性を調整する
各アプタマーが特定の表面受容体を認識するため、同じDNA足場をアプタマーを入れ替えるだけで再プログラムできます。研究チームはPTK7、ムチン-1、EpCAMの三つのターゲット用プローブを用い、各タンパク質の発現が高い細胞株と低い細胞株をパネルで示しました。ある受容体を多く持つ細胞は強いシグナルを出し、受容体が少ない細胞は同じ皿の中に混ざっていてもほとんど反応しませんでした。興味深いことに、同じ受容体を共有する細胞同士でも力の空間分布は異なり得て、受容体を介した力の流れは単に受容体の存在だけでなく各細胞種の内部配線にも依存することを強調しました。
細胞が引ける時間をプログラムする
アプタマーがDNAで作られているという利点を生かし、研究者らはプローブをアプタマーの結合能を制御するDNA反応ネットワークに接続しました。相補的な「ブロッカー」鎖は一時的にアプタマーを隠し、「アクチベータ」鎖はストランド交換反応を通じて後からブロッカーを除去して力感受性を回復します。また、RNase Hという酵素で切断され得るRNAベースのブロッカーを設計し、さらにその切断を酵素と競合するデコイ分子で遅らせました。このようにしてメカノセンシングを時間的プログラムに変換し、組み込みの遅延後や選んだ時間窓内でのみ細胞がシグナルを生成できるようにしました。
今後の生体材料にとっての意義
日常的な言葉で言えば、本研究はDNAを特定の細胞に対して、特定の力の下で、かつ選んだ時間にだけ開くスマートな機械的ロックに変えました。ヌクレオリンやPTK7のような一見目立たない受容体が細胞内で非常に異なる経路を通じて機械情報を運べることを示したことで、細胞が環境を「感じる」方法の図式が広がりました。全システムが核酸から構築されているため、DNA回路やナノデバイスの急速に成長するツールボックスに直接組み込めます。これにより、細胞が押したり引いたりする瞬間を検知するだけでなく、精密にタイミングされた生化学的応答で反応する材料や人工組織の基盤が築かれ、治癒や成長、がん治療の高度にプログラム可能な指導につながる可能性があります。
引用: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
キーワード: 機械的シグナル伝達, DNAアプタマー, 細胞力学, 合成生物学, DNA反応ネットワーク