Clear Sky Science · ja
階層型ビジョントランスフォーマーで増強したナノ流体散乱顕微鏡によるラベルフリーで数kDaの生体分子の質量とサイズの特性評価
最小の分子を可視化する
ホルモンや免疫シグナルなど、体内で重要な役割を果たす多くのメッセンジャーは非常に小さく、蛍光ラベルで標識しなければ強力な顕微鏡でもほとんど見えません。だがそのラベルは分子の挙動を変えてしまう可能性があり、創薬や基礎生物学には重大な欠点です。本研究は、ナノ流体チップと高度な人工知能を組み合わせることで、インスリン程度のサイズの個々の分子をラベルなしで秤量・寸法評価する手法を提示します。これにより、重要な生体分子をその自然状態で一つずつ観察する道が開かれます。
小さなチャネルを試験管として使う
この手法の中核はナノ流体散乱顕微鏡で、爪先ほどの大きさのチップに極めて狭いチャネルを刻んだものを使います。これらのチャネルは幅が数十ナノメートルしかなく、人の髪の毛より何千倍も細いです。バッファーに溶けた分子は表面に貼りつくのではなく、これらのチャネル内を自由にドリフトします。チップに可視光を照射すると、チャネル壁と通過する分子の双方が光を散乱します。チャネルの断面が分子よりはるかに大きいため、散乱光が干渉して分子の光学的なシグネチャーを大きく増幅します。空のチャネルの画像を分子がいるときの画像から差し引くことで、研究者はその通過の映画のような記録(キモグラフ)を得られ、質量と拡散速度の両方に関する情報を得られます。
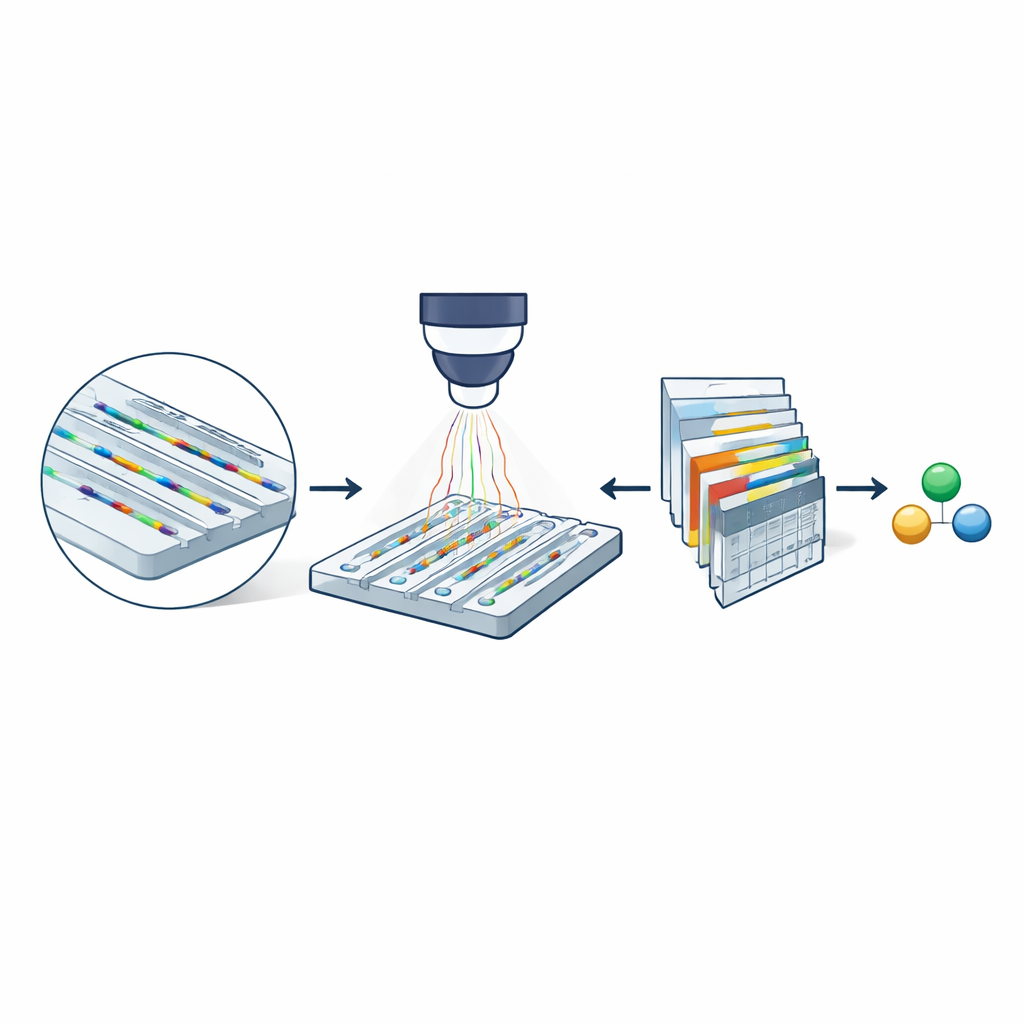
より小さいチャネルが重要な理由
この光学的増幅があっても、従来の手法ではおよそ60キロダルトン以上の分子、すなわち典型的な大型タンパク質しか特性評価できませんでした。より小さい種の信号はノイズに埋もれてしまうからです。研究チームは、ナノチャネルの断面積を縮めることで感度が劇的に向上することを示します:チャネル面積が小さくなるほど分子からの光学コントラストは増加します。牛血清アルブミンを用いて二つのチャネルサイズを比較した実験では、狭いチャネルでは経路がはっきり見える一方、広いチャネルではほとんど失われていることが示されました。この単純な幾何学的変更は、理論的には微弱な信号をノイズから確実に抽出できれば、さらに小さな生体分子も検出可能になることを示唆しています。
ノイズだらけの“映画”をAIに読ませる
この領域に到達するため、研究者らは階層型ビジョントランスフォーマーと呼ばれる専用の深層学習モデルを開発しました。各分子の正確な軌跡をピクセル単位で再構築しようとする代わりに、このモデルはキモグラフをマルチスケールで走査し、二つの出力を生成します:ある地点と時間に分子がいる確率を示す確率マップと、分子量および水力学的サイズの推定を符号化した特性マップです。確率マップで特性推定に重み付けすることで、モデルは主にノイズで占められる領域を無視できます。学習は実験的に測定した背景ノイズの上に重ねた模擬軌跡のみで行われ、目にほとんど見えない実際のシグナルがどのように見えるかをシステムが学べるようにしています。
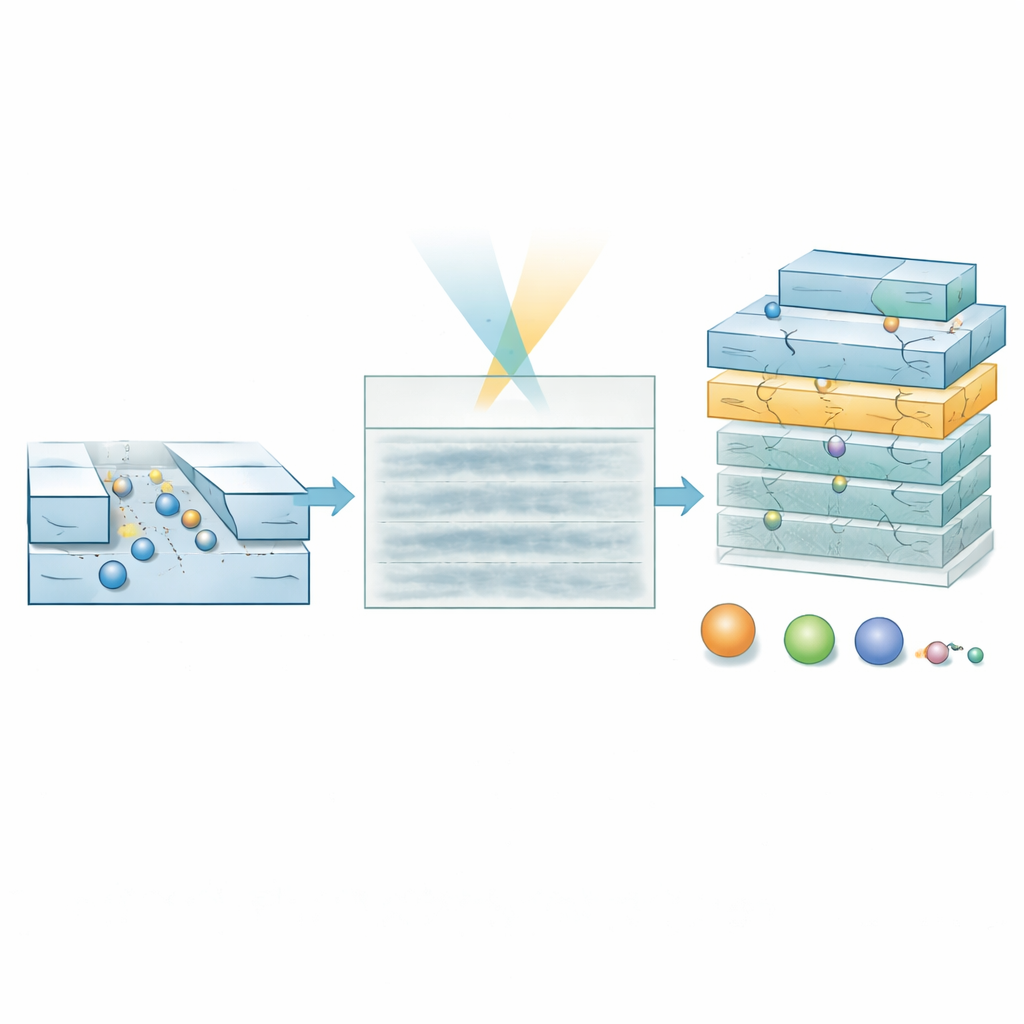
DNAとホルモン分子での検証
著者らはまず標準的なDNA「ラダー」を用いて手法を検証しました。これは既知の長さと質量の二本鎖断片の混合物で、比較的広いチャネル内で通常の検出限界を下回る断片をすべて意図的に含んでいます。生の動画では明確なDNAの軌跡は見えません。それでもAIモデルは分子の通過位置を正しく浮かび上がらせる確率マップを生成し、低信頼度のデータを除外すると予測質量は期待値と一致しました。また、この手法は、剛直で棒状のDNA断片がその全長よりも拡散に与える形状の影響から、より小さい有効サイズを報告する点も正しく捉えました。最も負荷の高い試験では、幅わずか約1.5 nm、質量約5.8 kDaのペプチドホルモンであるインスリンを超小チャネルで調べました。ここでもキモグラフは特徴がないように見えますが、モデルは文献値と良好に一致する質量とサイズの密集したクラスタを抽出し、バッファーのみの対照とは明瞭に分離しました。
限界への挑戦
この戦略がどこまで到達できるかを評価するため、チームはモデルの精度をクレーマー=ラオ下限(Cramér–Rao lower bound)と比較しました。これはデータのノイズに基づいて任意の不偏推定量が達成し得る最良の精度を定義する統計的限界です。大規模なシミュレーション群を用いて、分子の軌跡に寄与するフレーム数が約一万フレームを超えると、モデルの質量とサイズの推定は理論的最適値に近づくことを示しました。これは6 kDa程度の粒子でも成り立ちます。異なる濃度のインスリン実験でも同様の傾向が再現され、より長い有効軌跡がより精密な測定をもたらすことが示されました。制限要因は主に、微小で高速に拡散する分子が視野内に留まる時間の長さです。著者らは将来的にチャネル内で分子を穏やかにトラップする、あるいはブートストラップのようにデータを再利用する戦略で観察可能時間をさらに延ばすことを提案しています。
生物学と医学への意義
日常的な視点では、この研究は蛍光タグで触れたり表面に貼りつけたりすることなく、体内で最も小さく重要な分子のいくつかを個別に秤量・寸法評価できるようになったことを示しています。ナノ加工されたチャネルと、ノイズだらけの光散乱ムービーを読み取るために作られたAIを組み合わせることで、このラベルフリー顕微鏡法の質量検出限界はおよそ10倍程度改善されました。これにより、サイトカインやケモカイン、インスリンのような小さなシグナル伝達タンパク質やペプチドホルモンの単一分子レベルでの研究、さらには極めて感度良く小さな生体ナノ粒子や薬物輸送担体の特性評価が可能になります。技術が成熟すれば、創薬、診断、分子間相互作用が生命を形作る最小スケールでどのように働くかを探る基礎研究において強力なツールとなるでしょう。
引用: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
キーワード: ラベルフリー単一分子顕微鏡, ナノ流体散乱, ビジョントランスフォーマー, 小さな生体分子, インスリン検出