Clear Sky Science · ja
病原性Tau変異はオートファジー─リソソーム機能障害を引き起こし、前頭側頭型認知症モデルでのTau分解を制限する
脳の“清掃隊”が追いつかなくなるとき
なぜ一部の人は高齢になる何十年も前に記憶や行動に深刻な障害をきたすのか。本研究はその疑問に、1つの脳タンパク質であるTauと、それを制御する小さな細胞内「リサイクルセンター」に着目して取り組んでいる。生きたヒト神経細胞を超高解像度顕微鏡で観察することで、病的なTau変異がどのように細胞の廃棄処理機構を詰まらせるか、そして小分子でその機構を活性化すると混乱を解消できる可能性があることを示している。これらの知見は、特定の形式の認知症に対する新たな治療戦略を示唆するかもしれない。
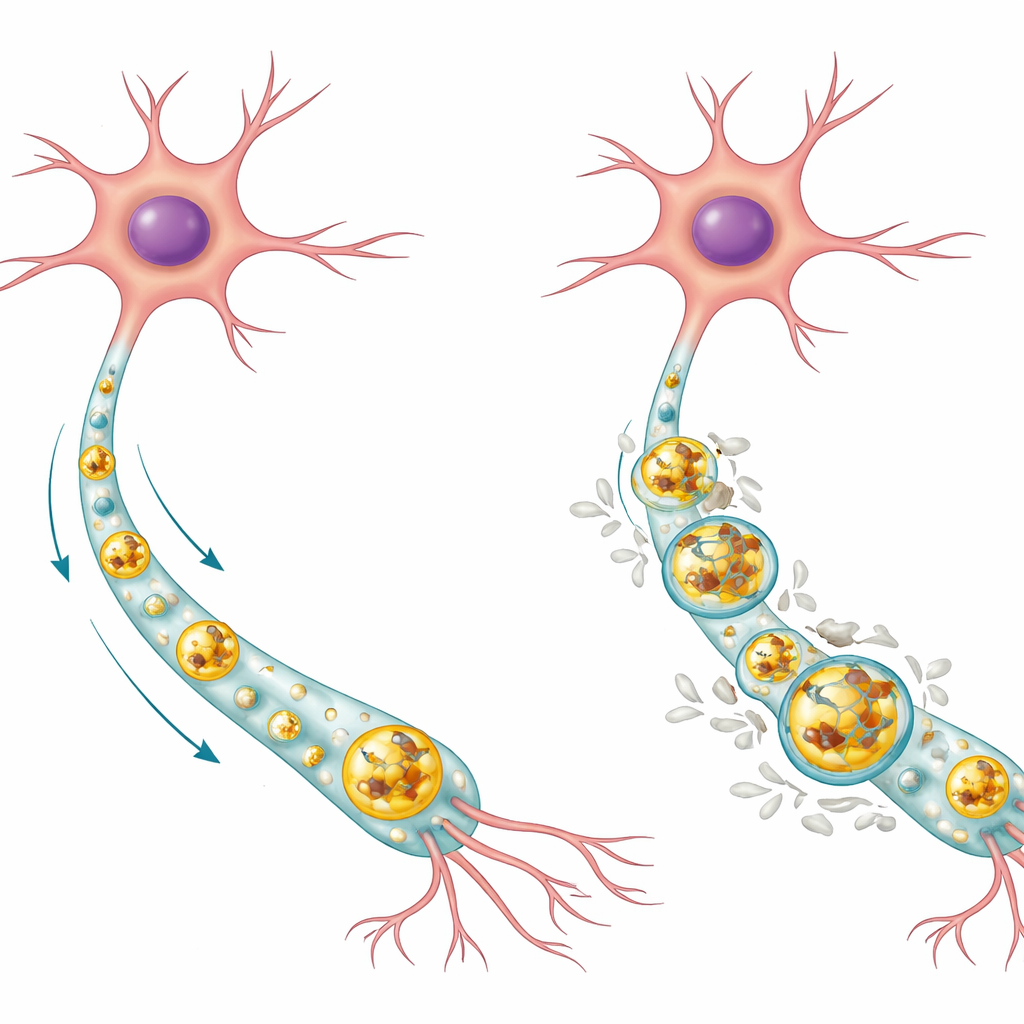
脳細胞は通常どう「ゴミ出し」するか
ニューロンは長寿命で単に分裂して損傷物質を希釈できないため、内部の清掃システムに強く依存している。主要な経路の一つがオートファジー─リソソーム経路である。この過程では不要なタンパク質や古くなった構成要素がオートファゴソームと呼ばれる膜嚢に包まれ、それが酵素を含むリソソームと融合して内部の荷物が分解・再利用される。健康なヒトニューロンでは、著者らは正常なTauタンパク質がリソソームの酸性中心に蓄積しそこで分解されやすい一方、疾患に関連する化学修飾型のリン酸化Tauはリソソームの外膜により多く存在する傾向があることを見いだした。健常細胞の多くのリソソームはTauをほとんど含んでおらず、この系が通常Tau量を低く良好に制御していることを示唆している。
遺伝性認知症で何が狂うのか
研究チームはMAPT遺伝子のp.R406Wという変異に着目した。これは遺伝性の前頭側頭型認知症を引き起こし、アルツハイマー様の記憶障害を模倣することがある。幹細胞技術を用いて患者の皮膚細胞を誘導多能性幹細胞にリプログラムし、さらに変異を持つものと遺伝子編集で正常に戻したものの大量のヒトニューロンに分化させた。変異ニューロンでは総Tau量とリン酸化Tauが著しく増加していたが、それはTauの産生が増えたためではなく、除去が効率的でないためだった。超高解像度イメージングにより、変異細胞のほぼ全てのリソソームがTauで満たされ、特にリン酸化Tauがリソソーム膜を覆っていることが示された。この蓄積は、細胞の主要なタンパク質廃棄経路が詰まっていることを示していた。
詰まったリサイクルセンターとのろい交通
リサイクル機構を詳しく見ると、変異ニューロンのリソソームは数が増え、より大きくなり、細胞体からより遠くに位置する傾向があった。蛍光色素を用いた生細胞イメージングでは、これらのリソソームはより遅く移動し、神経突起に沿っての移動距離が短かったが、微小管のトラック自体は正常に見えた。変異ニューロンにはまたオートファゴソームや荷物結合アダプタータンパク質p62が増え、脂質滴も増加しており、材料が廃棄対象としてタグ付けされているものの完全に分解されていないことを示していた。pH感受性レポーターを用いると、変異細胞ではオートファゴソームがリソソームと適切に融合できないことが多く、「未完了」のリサイクル小胞が堆積し、Tauだけでなく他の荷物に対しても広範な清掃障害が生じていることが明らかになった。
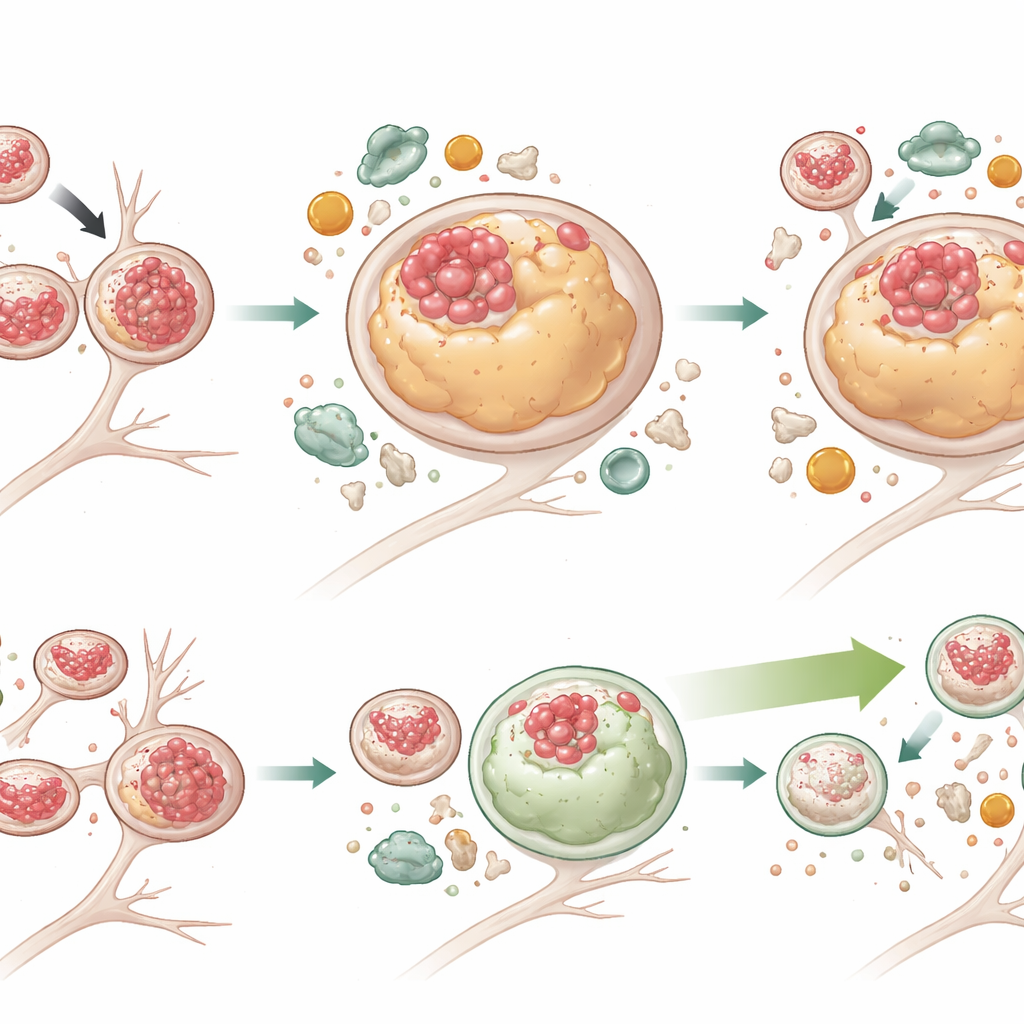
交通渋滞は直らなくても清掃を強化する
オートファジーを強化すればこれらの問題を克服できるかを試すため、研究者らはG2‑567という小分子でニューロンを処理した。これは以前にオートファジー─リソソーム系を刺激することが示されていた。2週間の処理後、変異ニューロンでは総Tauおよびリン酸化Tauの両方が大幅に低下し、多くのリソソームが再びTauのない状態に戻った。リソソームも正常に近い大きさに縮小した。オートファジー活性のマーカーは増加し、分解の滞りを示すp62は変異細胞で減少し、荷物の分解がより効果的になったことが示された。興味深いことに、G2‑567は全ての欠陥を是正したわけではない。変異ニューロンのリソソームは依然として細胞体から遠くに位置しがちで移動は鈍く、リソソーム輸送に関係するアダプタータンパク質(JIP3)は高値のままだった。これは、リソソームの移動機能と分解機能が部分的に切り離せること、そして分解能を高めるだけで有害なTauの蓄積を減らすのに十分かもしれないことを示唆している。
将来の認知症治療への意味
非専門家向けにまとめると、この前頭側頭型認知症の遺伝モデルでは問題は単にTauが異常化することだけではなく、ニューロンのリサイクルシステムが追いつかないことにある。p.R406W Tau変異はオートファジー─リソソーム経路のいくつかの段階を直接乱し、特にリン酸化型Tauがリソソームの内外に蓄積し、ほかの未分解物質とも共にたまる。細胞の清掃機構を薬理的に刺激して働きを強めることで、研究者らはTau量を下げリソソームの大きさを正常化できたが、輸送の欠陥は残ったままだった。これらの知見は、安全にオートファジーやリソソーム機能を高める薬剤が、Tau関連認知症やより一般的なアルツハイマー病のような状態でタンパク質バランスを回復する助けになる可能性を支持するものである。
引用: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
キーワード: Tauタンパク質, オートファジー, リソソーム機能障害, 前頭側頭型認知症, 神経変性