Clear Sky Science · ja
NS4B 正同族全域の相互作用アトラスはオルソフラビウイルス複製における UFMylation の保存的役割を同定する
このウイルス研究が重要な理由
デング熱、ジカ、ウエストナイルのようなウイルスは新しい地域へ広がり、発熱から脳感染や先天性欠損までさまざまな病態を引き起こします。それでも、広範囲に効き信頼できる治療法はまだ不足しています。本研究は、これらのウイルスと UFMylation と呼ばれるあまり知られていない細胞内のタグ付けシステムとの間にある隠れた協力関係が、病原体の増殖にどう寄与するかを探ります。多数の関連ウイルスにわたってこの関係をマッピングすることで、将来の抗ウイルス薬開発に利用できる共有の弱点を明らかにしています。
重要なウイルスの内通者を追う
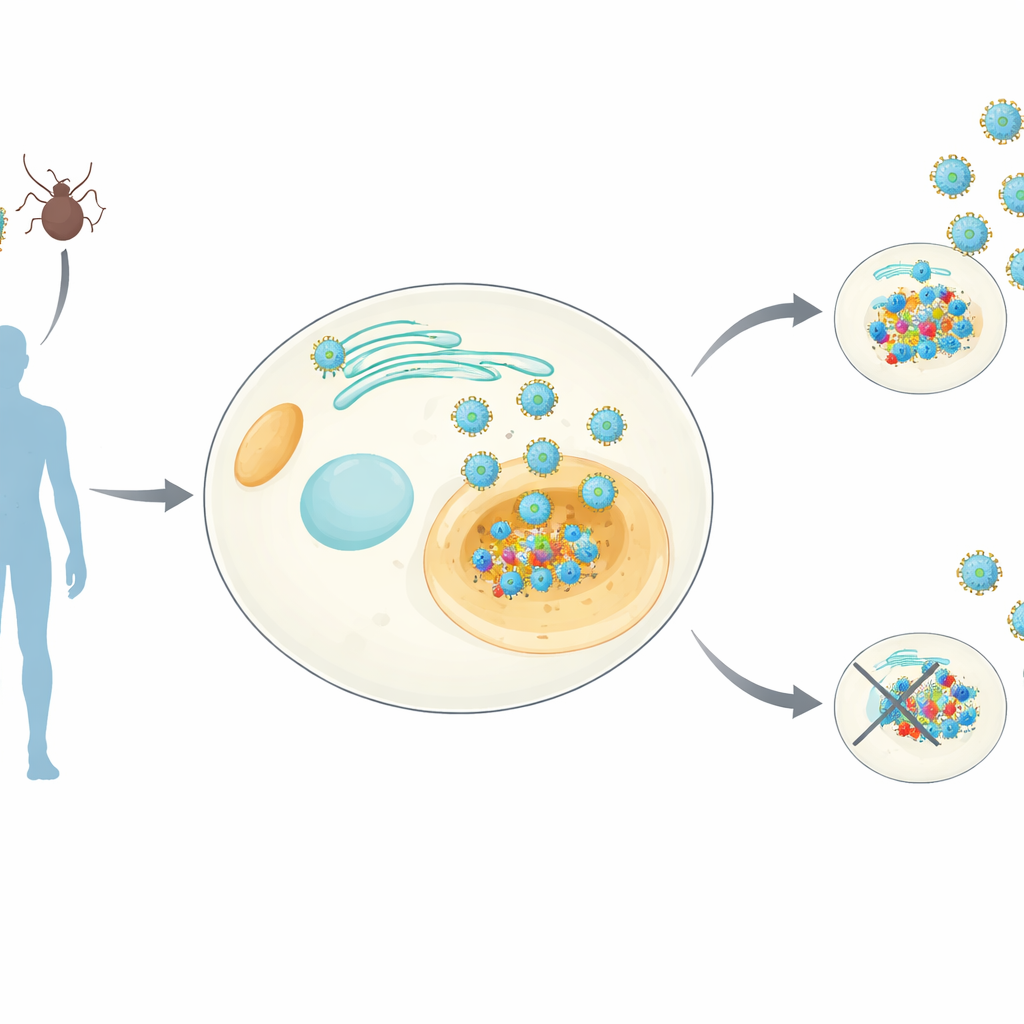
オルソフラビウイルス群—デング熱、ジカ、黄熱などを含むグループ—は、細胞内膜に埋まる小さなタンパク質 NS4B を持ちます。NS4B はウイルス複製に必須であることが知られていますが、その正確な役割は不明瞭でした。研究者らは人由来の細胞株を作製し、8 種類の異なるオルソフラビウイルス由来の NS4B を安定的に発現させました。次に、高感度の質量分析法を用いて NS4B と結合するヒトタンパク質を引き出し、並行して NS4B 発現が細胞内のタンパク質構成に与える影響を測定しました。これにより、共通およびウイルス特異的な宿主標的を示す属全体の「相互作用アトラス」—研究者らが NS4Bome と呼ぶもの—が得られました。
共通の手口と種ごとの工夫
アトラスは NS4B と相互作用する 538 のヒトタンパク質と、NS4B 存在時に量が変動する 500 を超えるタンパク質を明らかにしました。これらの多くはミトコンドリアのエネルギー産生、内部膜の形作り、新しく合成されたタンパク質や脂質の輸送を管理する経路に集中していました。いくつかの相互作用は大部分のウイルスに共通しており、すべてのオルソフラビウイルスが使う進化的に保存されたトリックを示唆しています。一方で、特定の種や株にのみ見られる相互作用もあり、これがあるウイルスが蚊を好む理由や、出血熱ではなく脳疾患を引き起こす理由を説明する可能性があります。この系統的な全体像は、これまでの断片的な研究群を纏め上げ、これらのウイルスが細胞をどのように書き換えるかの一貫した地図に変えます。
意外な協力者:UFMylation システム
NS4B が結びつく多くのパートナーの中で、際立っていたのは UFMylation 経路の開始酵素である UBA5 でした。UFMylation は小さなタンパク質タグ UFM1 を選択的標的に付加し、タンパク質品質管理やストレス応答などのプロセスに影響を与える細胞システムです。RNA干渉や CRISPR による遺伝子ノックアウトを用いて、研究チームは UBA5 を欠く、あるいは UFMylation を実行できない細胞がジカおよびいくつかの関連ウイルスの複製を大幅に低下させることを示しました。正常な UBA5 を再導入するとウイルス増殖は回復しましたが、UFMylation を駆動できない変異型は回復させず、タグ付け活性自体が感染に不可欠であることを証明しました。
タグ付けはウイルス工場をどう支えるか
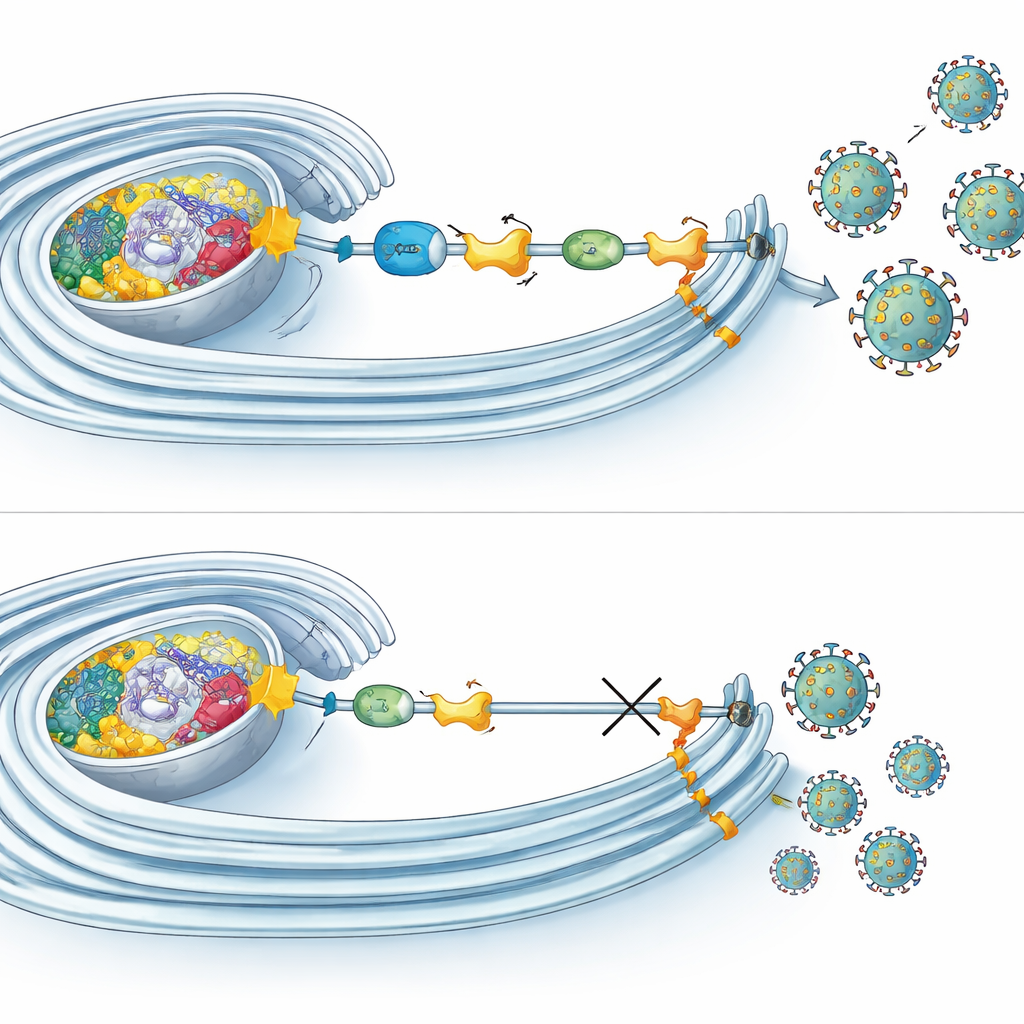
顕微鏡観察と生化学的実験により、複数の UFMylation 成分がウイルス RNA が改変膜内で複製される場所に集合することが示されました。そこでそれらは NS4B に加え、複製装置を構築する他のウイルスタンパク質とも結合していました。興味深いことに、UFMylation を阻害してもウイルスの侵入、RNA 産生、タンパク質合成は止まりませんでした。代わりに、主にサイクルの後半段階、例えば感染性粒子の組み立てや放出が著しく損なわれました。同時に、UFMylation はミトコンドリアの呼吸にも影響を与えることがわかりました:経路が無効化されると酸素消費が減少しミトコンドリアの形状が変化しました。対照的にジカ感染の初期ではミトコンドリア呼吸が亢進し、ウイルスは必要な時に細胞のエネルギー産出を高めるために UFMylation を利用している可能性が示唆されます。
細胞と小さな魚で薬を試す
次に著者らは、UBA5 の活性部位を阻害する小分子化合物 DKM 2‑93 に注目しました。培養ヒト細胞では、この阻害剤は細胞に大きな損傷を与えない用量でジカウイルスの産生を約 10 分の 1 に減少させ、いくつかの細胞型で活性を示しました。この戦略が生体内で機能するかを評価するため、発達中の脳での病態を模倣するジカ感染のゼブラフィッシュモデルを用いました。初期脳発生期に感染した胚を DKM 2‑93 で処理するとウイルス RNA レベルが有意に低下し、重度の奇形を示す個体の割合が減少し、生体内での実質的な抗ウイルス効果が示されました。
今後の治療にとっての意味
多くのオルソフラビウイルス由来の NS4B がヒトタンパク質とどのように相互作用するかの包括的な地図を構築することで、本研究はこれらのウイルスが感染性粒子を産生するために依存する保存的な補助経路として UFMylation を浮き彫りにしました。同じ宿主システムがデング熱、ジカ、ウエストナイルなどを支えているように見えるため、UFMylation を選択的に抑える薬剤は個別のウイルスを狙うのではなく広域スペクトルの抗ウイルス作用をもたらす可能性があります。どのタンパク質が実際にタグ付けされるかを正確に理解し、安全性を確保するためのさらなる研究は必要ですが、本発見は将来的に複数の蚊媒・ダニ媒疾患の流行を単一の治療法で抑える助けとなり得る有望な宿主標的を示しています。
引用: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
キーワード: ジカウイルス, デング熱, 宿主–ウイルス相互作用, UFMylation, 広域スペクトル抗ウイルス薬