Clear Sky Science · ja
線条体のコリン作動性介在ニューロンの同期活性化は局所的なセロトニン放出を誘導する
この脳化学の発見が重要な理由
習慣、動機づけ、強迫的行動はいずれも線条体と呼ばれる小さくも重要な脳領域に依存しています。ドーパミンとセロトニンという二つのよく知られた神経伝達物質がこの領域の調節を担っており、多くの精神薬はそれらのバランスを調整することを目指します。本研究は、これまで隠れていた別の情報伝達経路を明らかにしました。アセチルコリンを放出する特別な種類の神経細胞が、セロトニン線維に直接作用してセロトニン放出を増強できることが示されたのですが、それは線条体の特定部位に限られていました。この新たな連結は、強迫性障害(OCD)やパーキンソン病のような疾患で、複数の脳化学物質が同時に絡み合って変化する理由を説明する手がかりになるかもしれません。
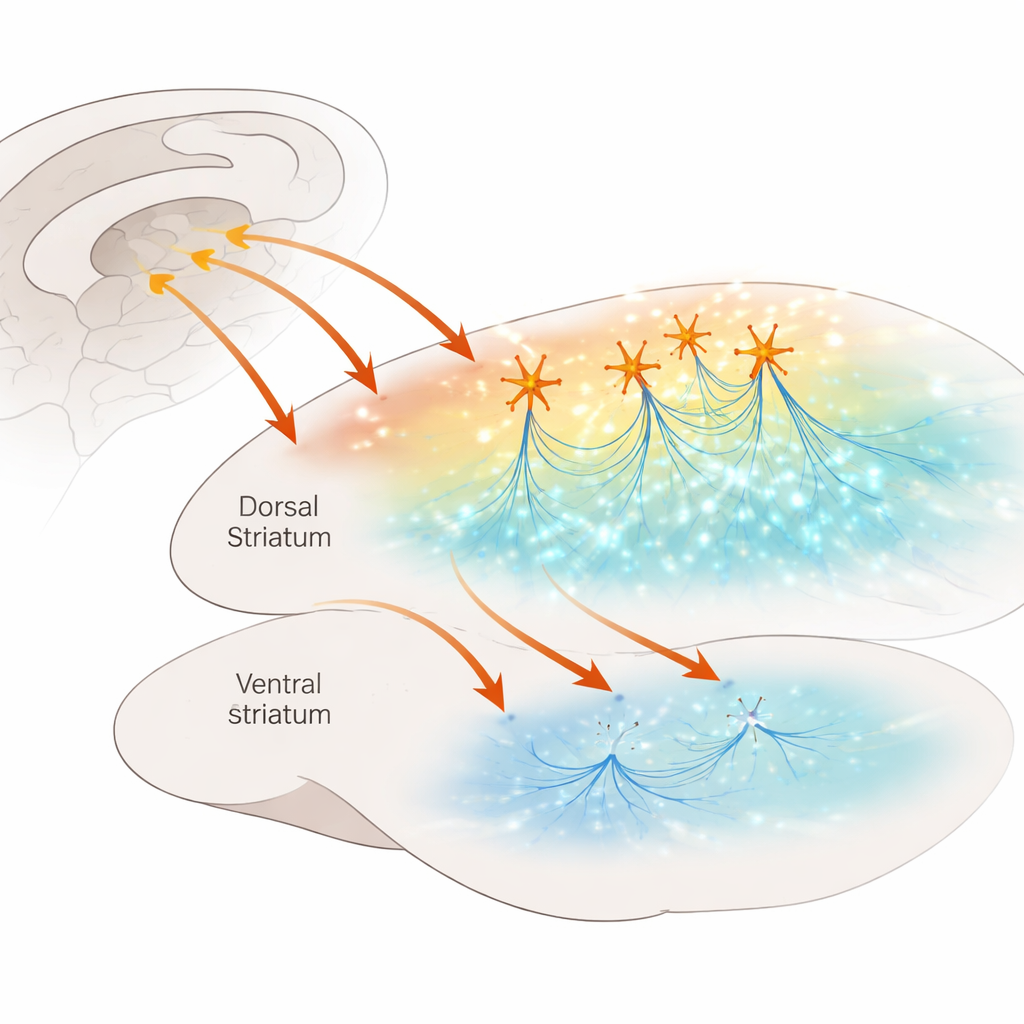
脳内の多忙な交差点
背側線条体は意思決定のハブとして働き、目標指向の行動と自動的な習慣との切り替えを助けます。皮質からの豊富な入力を受け、ドーパミンやセロトニンといった神経調節物質に囲まれて信号処理が微調整されます。このハブにはまばらながら強力なコリン作動性介在ニューロンの集団が存在し、アセチルコリンを放出して小さなメトロノームのように規則的に発火します。以前の研究は、これらの細胞が同期して発火すると、ドーパミン線維上のニコチン性アセチルコリン受容体に作用してドーパミン放出を強く増強できることを示していました。セロトニンについて同様の近道が存在するかは分かっていませんでしたが、セロトニンは気分や学習、OCDやうつ病の治療に使われる薬の効果にとって中心的です。
リアルタイムでセロトニンの活動を観察する
この問いに取り組むため、研究者たちはセロトニンの存在で蛍光センサーが明るく光るマウスを用いました。彼らはこのセンサーを運ぶウイルスを線条体に注入し、薄切りの脳スライスを作製して、二光子顕微鏡で組織を刺激しながらセロトニン信号を観察しました。背側線条体内での電気刺激は、ゆっくり減衰する明瞭なセロトニンセンサーの発光を引き起こしました。研究チームがニコチン性アセチルコリン受容体を遮断する薬を適用すると、これらの発光は小さくなり空間的にもより局所化しました。これは、アセチルコリンがこれらの受容体を介してセロトニン放出を増し、それを広い領域に拡げるのに寄与していることを示します。驚くべきことに、近接する領域でセロトニン配線がさらに密な腹側線条体で同じ実験を行っても、こうしたニコチン性の寄与は見られず、この相互作用が領域特異的であることが明らかになりました。
光で標的的にセロトニンを引き起こす
コリン作動性介在ニューロンからのアセチルコリンだけでセロトニン放出を駆動できるかを調べるために、著者らは光遺伝学に頼りました。彼らはこれらの介在ニューロンが短い青または黄の光に応答するように遺伝子改変し、同期的に活性化しながらセロトニンセンサーを監視しました。1ミリ秒ほどの短い光照射だけで、背側線条体において強力なセロトニンシグナルが誘発され、時間経過は電気刺激で誘発される応答のニコチン感受性成分と類似していました。ニコチン受容体を遮断すると、このシグナルはほぼ完全に消失しました。これはスライス内の他の化学的入力や受容体が薬理学的に沈黙させられている場合でも同様でした。この精密な刺激と受容体遮断の組合せにより、アセチルコリンが他の細胞型やドーパミン軸索を介する間接経路に依存するのではなく、セロトニン線維上のニコチン受容体に直接作用して局所的なセロトニン放出を引き起こすことが示されました。
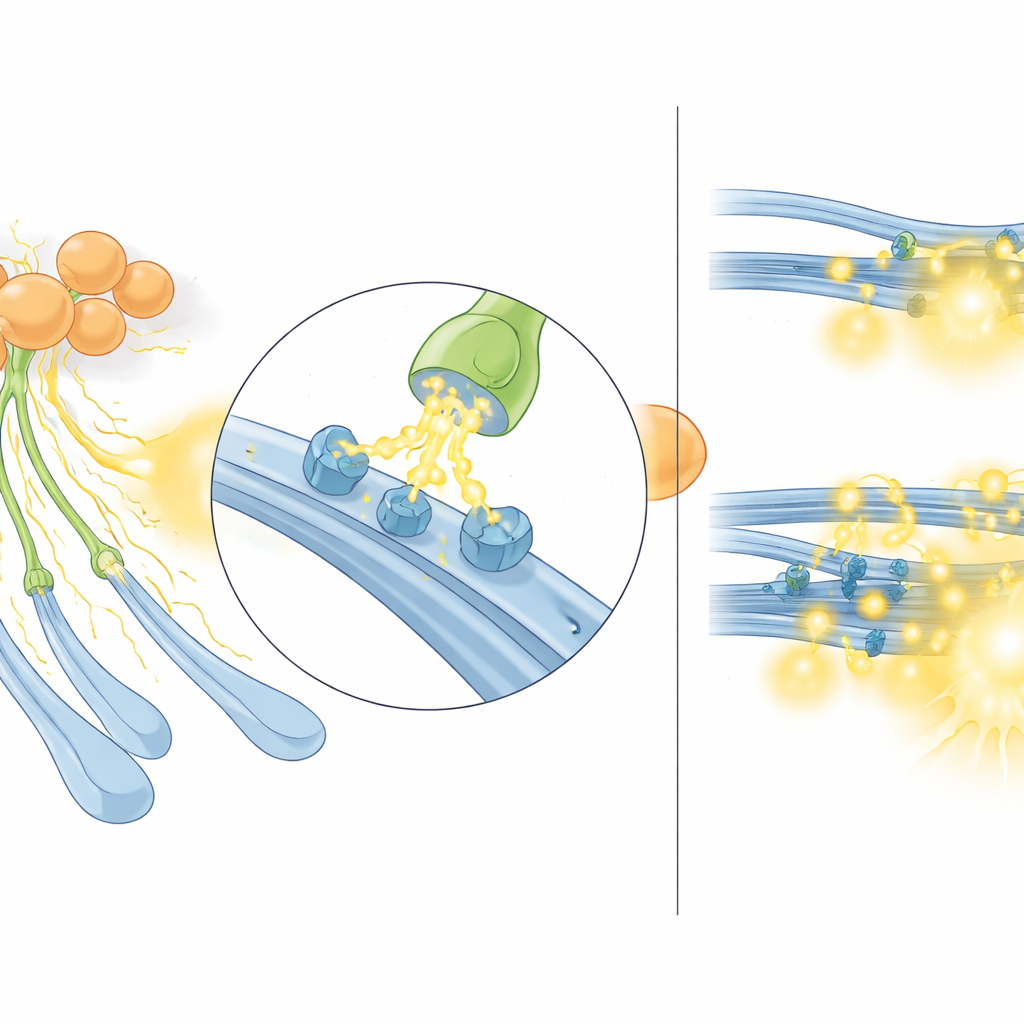
システムが過剰に働くとき
次に研究チームは、アセチルコリンシグナルが異常に強い病態関連の状態で何が起きるかを問いました。彼らは過剰なグルーミングなどOCDに類似した行動を示し、コリン作動性介在ニューロンの活動増加とアセチルコリン放出の増大が示されている確立されたモデルであるSapap3ノックアウトマウスを用いました。これらのマウスでは、背側線条体への電気刺激が正常マウスよりも大きなセロトニンセンサー信号を生じました。重要なことに、この差はニコチン受容体を遮断すると消失し、つまりセロトニン放出のアセチルコリン依存部分だけが増強されていることを意味しました。ドーパミンでも同様のパターンが見られました。言い換えれば、この過コリン作動性状態では、コリン作動性介在ニューロンがモノアミン放出のニコチン成分を不均衡に増幅し、結果としてアセチルコリンがセロトニン線維を主要な出力経路として“ハイジャック”するかのように振る舞います。
脳疾患への広い示唆
これらの発見は、背側線条体におけるアセチルコリンとセロトニンの間の微細に調整された、領域的に限局した対話を明らかにします。健常な脳では、行動的に重要な出来事によって駆動されるようなコリン作動性介在ニューロンの同期バーストが、セロトニン信号を一時的に拡大・強化し、行動がどのように学習されたり抑制されたりするかを形作る可能性があります。Sapap3ノックアウトマウスやおそらくOCDやパーキンソン病のような状態でアセチルコリンが持続的に高まっている病態では、この同じ機構が過剰になり、セロトニンやドーパミンのシグナリングパターンの異常に寄与しているかもしれません。この隠れた連結を理解することは、複数の神経調節物質が正常行動と疾患の双方でどのように相互作用するかを再考させる新しい視点を提供し、将来的には各化学物質を個別に扱うのではなく、その共同ダイナミクスをより正確に標的にした治療法につながる可能性があります。
引用: Matityahu, L., Hobel, Z.B., Berkowitz, N. et al. Synchronous activation of striatal cholinergic interneurons induces local serotonin release. Nat Commun 17, 2278 (2026). https://doi.org/10.1038/s41467-026-70359-6
キーワード: 線条体セロトニン, コリン作動性介在ニューロン, ニコチン性アセチルコリン受容体, 強迫性障害, 基底核