Clear Sky Science · ja
アミノアシルリン酸塩が駆動するクリック反応とアシルトランスファー反応の経路選択
日常の化学でタイミングが重要な理由
細胞内では重要な分子がまるでレシピの手順のように非常に正確な順序で合成・修飾されます。そのタイミングがタンパク質のスイッチオン・オフや立体変化を決定します。化学者は酵素や光・pHといった外部トリガーに頼らず、水中で単純な非生体系分子を用いてこのような組み込まれた時間制御を模倣したいと考えています。本論文はまさにそれを実現する人工の反応系を示します:小さなペプチドの構造と「クリックケミストリー」に由来する一般的な結合形成反応を利用して、どの化学段階が先行し、どれが順番を待つかを決めています。
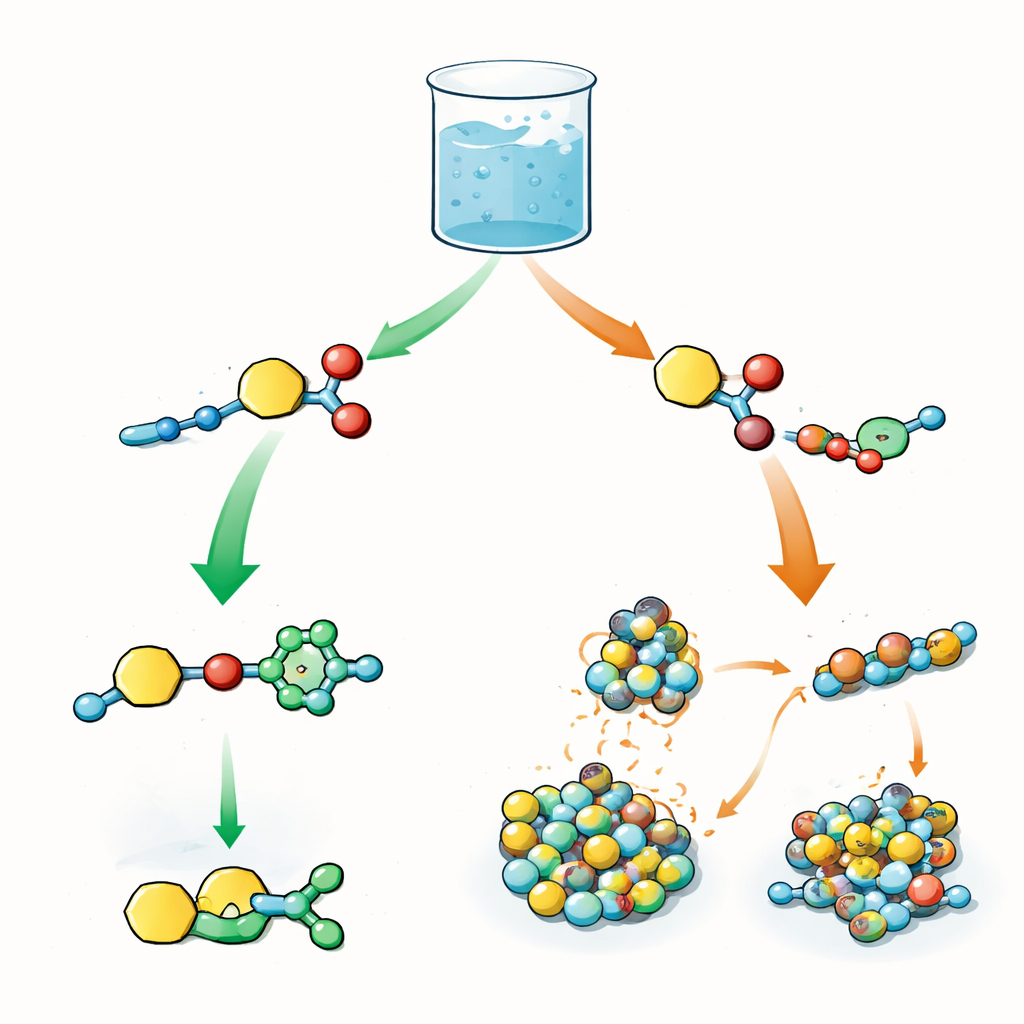
一つのフラスコ内の二つの競合反応
著者らは二つの反応性を持つ中心的なビルディングブロックを設計します:一つはアシル基(タンパク質修飾に頻用される小さな化学フラグメント)を受け渡せる性質、もう一つは銅触媒を用いるアジド–アルキンの環化付加反応(CuAAC)というクリック反応を受けうる性質です。同一の容器内で、この中間体はアジドと、アシル基を奪う求核剤として働く短いペプチドと混合されます。生物では活性化、転移、さらなる修飾といった一連の順序がタンパク質の挙動を制御します。ここでの問いも同様です:双方の反応が同時に可能なとき、系はまずクリック反応を選ぶのか、アシルトランスファーを先行させるのか、それとも両者の混合を生むのか?
遅い酸素、速い硫黄
研究チームはまずチロシンを含むペプチド(側鎖が酸素基を持つアミノ酸)を調べます。弱塩基性条件下ではクリック反応が先行します:アルキンとアジドが素早く結合する一方で、チロシンへのアシルトランスファーは遅く、中間体はほとんど検出されません。複数のクリック由来生成物が共存し、段階間に明確な時間差はほとんど見られません。研究者がシステイン(側鎖が硫黄基を持つアミノ酸)に切り替えると状況は逆転します。システインは迅速にチオエステル(硫黄結合したアシル生成物)を形成し、高収率で生成物が現れ、クリック生成物が出るのはずっと後になります。この変化は、硫黄が反応性が高いだけでなく銅イオンにも強く結合して触媒を拘束し、クリック経路を一時的に「一時停止」させることに起因します。
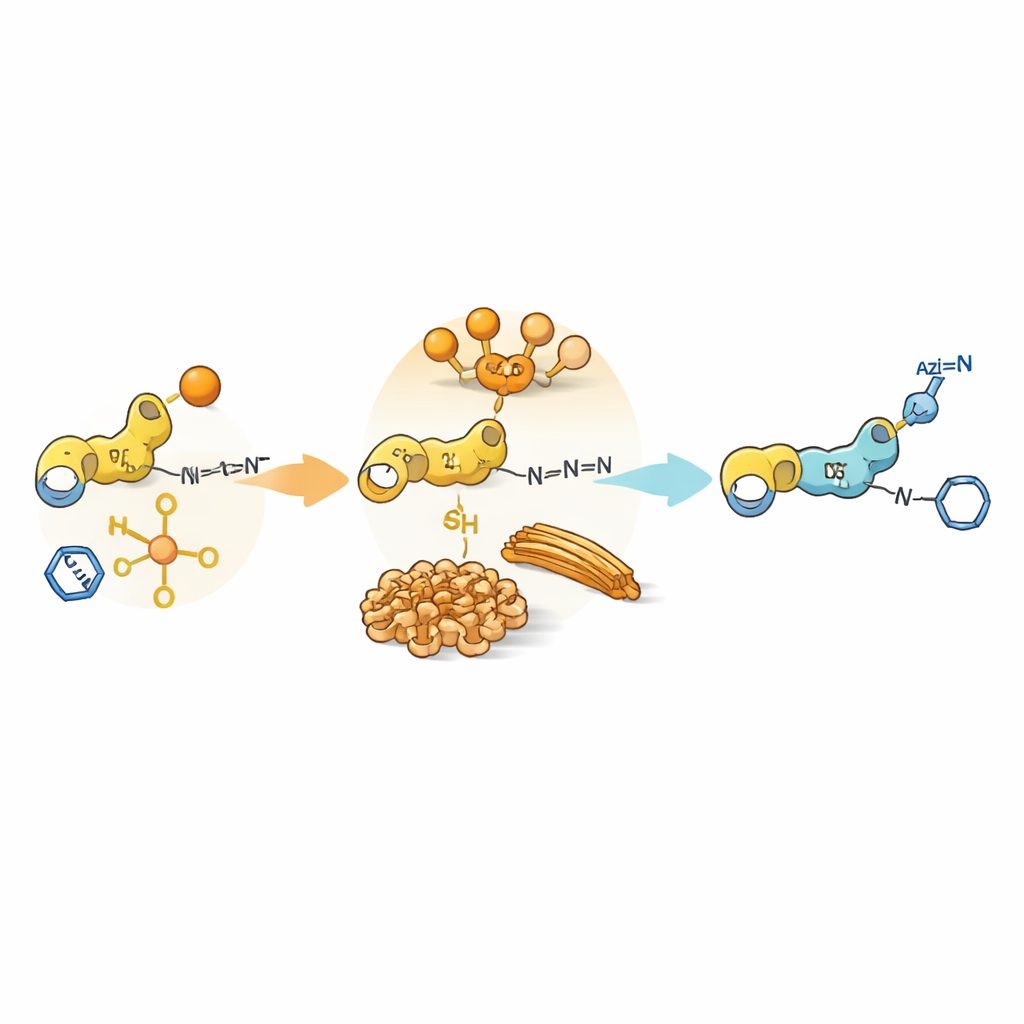
自己集合が化学的ゲートになる
単純な反応性を超えて、ペプチド自身が水中で大きな構造に凝集し、ソフトゲルや繊維を形成することがあります。これらの集合体は一部の反応成分を濃縮し、他を排除する小さな領域を作ります。特定の芳香族基を持つチロシンやシステイン含有ジペプチドでは、中間体が繊維状や密な粒子へと自己集合します。こうした詰まった領域内では、求核剤とアシル供与体が隣接しているためアシルトランスファーが有利になります。一方でアジドと銅触媒は主に周辺の溶液に残ります。その結果、自由溶液中では本来速いクリック反応が、反応点に到達する必要があるために遅延します。この触媒の居場所と基質の位置との「相不一致」が、アシル化中間体の寿命を伸ばし、クリック化学の開始を遅らせます。
カスケードと選択をプログラムする
組み込みのスケジューリングをどこまで制御できるかを試すため、著者らはより複雑な状況を設計します。一例では一つのペプチドがシステインとチロシンの両方を含み、二種類の異なるアシルトランスファー部位を提供します。反応は三段階のカスケードとして進行します:まずシステイン上にチオエステルが形成され、次に二つ目のアシル基がチロシンへ移動し、それらの後にのみクリック生成物が現れます。別の実験系では、一本鎖の柔軟な脂肪族アジドと剛直で芳香族なアジドの二つが同じ反応中心を競います。驚くべきことに系は一貫して脂肪族アジドを好み、アジドの形状や電子的性質がどの生成物が支配的になるかに偏りを与え得ることを示します。これらはいずれもアシルトランスファーの時間制御がペプチドによって担われている状況です。
将来のスマート材料にとっての意義
平易に言えば、この研究は複数の潜在的に競合する反応を同じ単純な水系混合物に詰め込み、それらを酵素やポンプ、外部スイッチを使わずに所定の順序で発火させる方法を示しています。ペプチドに酸素か硫黄かを持たせるか、自己集合の傾向を調整するか、アジドの性質を変えるかによって、著者らは小さな化学ネットワークに内部時計を組み込みます。初期の可逆的なアシルトランスファーは短命の中間体を作り、頑健でほぼ不可逆的なクリック段階がいつどのように起こるかを形作ります。こうしたプログラムされた配列は、生命が行う精密な時間制御化学のように、経時的に自身の経路を「決定する」スマート材料や合成反応ネットワークの基盤となり得ます。
引用: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
キーワード: クリックケミストリー, アシルトランスファー, 超分子集合, 反応ネットワーク, ペプチド化学