Clear Sky Science · ja
単一細胞マルチオミクスが明らかにした、肺線維症を駆動する血管内皮の機械感受性PIEZO1‑IL‑33軸
なぜ硬くなった肺が問題なのか
肺線維症は、かつて弾力のあった肺胞が徐々に硬い瘢痕組織に置き換わり、呼吸が常に大変に感じられるようになる深刻な肺疾患です。現在の治療は病状の進行を遅らせることはできても、完全に止めたり逆転させたりすることはできません。本研究は一見すると単純だが重要な問いを投げかけます:肺の血管を内側から覆う細胞は、周囲の組織が異常に硬くなったことをどのように感知し、その感覚がどのようにしてさらなる瘢痕形成につながるのか?研究者らはこの連鎖を単一細胞と個々の遺伝子レベルまでたどることで、血管に存在する薬剤で狙える可能性のある機械的“スイッチ”を明らかにしました。
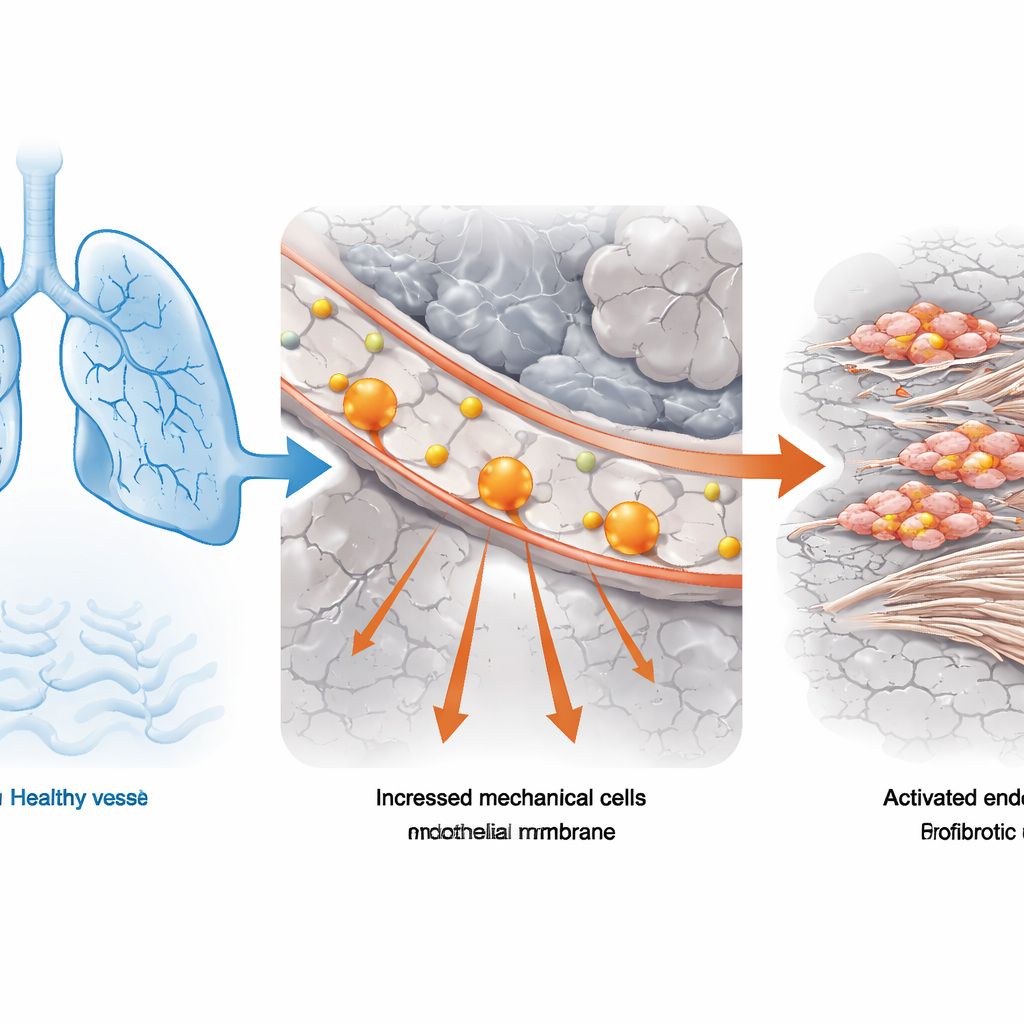
肺機能検査から単一細胞解析へ
チームはまず特発性肺線維症患者(この病気の最も一般的な型)と健常な肺を持つドナーの肺組織を用いました。呼気量などの標準的な肺機能測定と、数千の個々の細胞でどの遺伝子が活性化しているかを読み取る強力な単一細胞RNAシーケンシングを組み合わせました。臨床のバルクデータを単一細胞プロファイルに結びつける計算ツールを使うことで、重度に機能が障害された肺と最も強く関連する細胞種を特定しました。血管内皮細胞――血管の内膜を形成する細胞――が、肺活量が正常の半分未満の患者で特に豊富に見られました。これらの内皮細胞では「機械的ストレス」に関連する遺伝子プログラムが一貫して亢進しており、異常な物理的力が病態の一部であることを示唆していました。
隠れた駆動因子としての機械的ストレス
このストレス感知と病気の関連が一般的かどうかを確かめるために、研究者らは2種類のマウス肺線維化モデルに取り組みました:化学療法薬ブレオマイシンによるものと、長期のシリカ粉塵曝露による職業性のものです。これらの実験的肺で単一細胞解析を行うと、やはり内皮細胞が強い機械的ストレスのシグネチャーを示していました。両モデルとも周囲の肺組織が肥厚し硬くなるにつれて、血管内皮は不適応な状態に切り替わるように見えました。ヒト試料と動物モデルの一致は、炎症や免疫反応だけでなく、肺の歪んだ物理的力が線維化の発生と進行に中心的な役割を果たしているという考えを強めました。
重要な役割を持つ圧力センサー
さらに掘り下げると、研究者らは伸展などの物理的刺激を生化学的シグナルに変換する「機械受容体」タンパク質を、ストレスを受けた内皮細胞で上方制御されているものとして探索しました。チャネル型のタンパク質PIEZO1が繰り返し有力な候補として浮上しました。線維化を持つマウスとヒトの血管内皮では、PIEZO1のレベルが健常対照より著しく高かったのです。内皮でのみPIEZO1を欠損させたマウスを作製すると、これらの個体はブレオマイシン誘発の肺線維化に対してより強い抵抗性を示しました:コラーゲン蓄積が少なく、瘢痕を形成する活性化細胞が減り、線維化の化学的マーカーも低下しました。ペプチド阻害剤でPIEZO1を薬理学的に遮断すると瘢痕が軽減され、逆に活性化させると線維化が悪化しましたが――内皮細胞に受容体が存在しない場合は例外でした。これらの実験は、血管内皮におけるPIEZO1が単なる傍観者ではなく、疾患の必要な駆動因子であることを示しています。
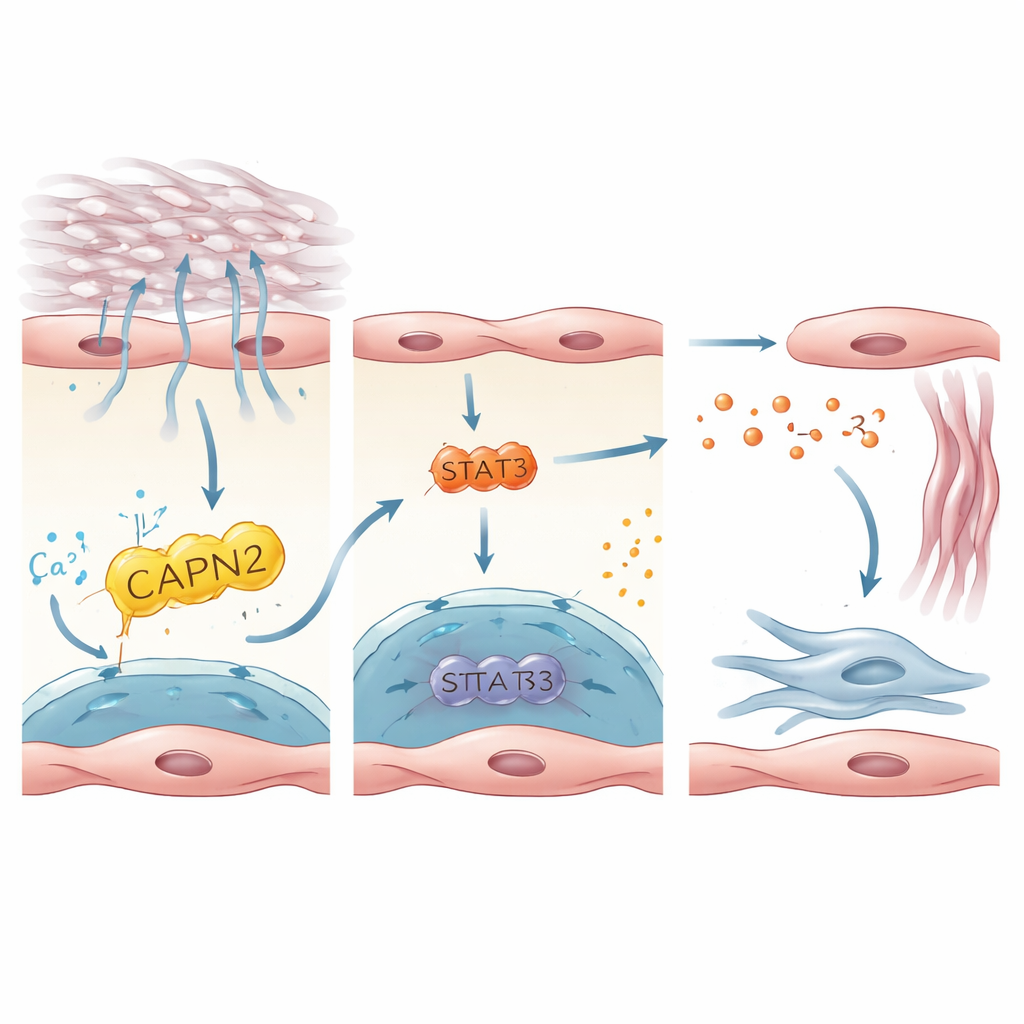
瘢痕形成細胞を目覚めさせるシグナル連鎖
研究は次に、内皮細胞内でのPIEZO1活性化がどのように線維芽細胞(瘢痕組織を敷設する細胞)を目覚めさせる信号へと変換されるかを追跡しました。ヒトとマウスのデータセットを統合することで、ストレスや損傷を受けた細胞から放出される小さなタンパク質であるインターロイキン‑33(IL‑33)が主要なメッセンジャーとして特定されました。IL‑33はPIEZO1陽性の内皮細胞で強く発現しており、線維化を持つ患者とマウスの肺で上昇していました。硬い基質上で培養したり、硬い肺に対して呼吸で伸展される状況を模したヒト内皮細胞では、PIEZO1の活性化がIL‑33産生を促進しました。これは下流の酵素CAPN2と転写因子STAT3に依存しており、両者が協調してIL‑33遺伝子の活性を調整していました。マウスでは内皮細胞特異的にIL‑33を欠損させると線維化から保護され、一方で内皮細胞にIL‑33を過剰発現させるとPIEZO1欠損の保護効果が消失しました。これらの結果は直線的な軸を描きます:機械的ストレス → PIEZO1 → CAPN2/STAT3 → IL‑33 → 線維芽細胞活性化と瘢痕形成。
将来の治療法にとっての意味合い
非専門家向けの要点は、肺線維症は暴走する免疫細胞だけによって駆動されるのではなく、血管における“触覚”の欠陥も病態に関与しているということです。内皮細胞は周囲が過度に硬くなったことを感知し、PIEZO1スイッチを入れ、それに応答してIL‑33という危険信号を放出し、近傍の線維芽細胞に瘢痕の形成を続けるよう促します。機械的力から遺伝子発現へと至るこの連鎖を解剖することにより、PIEZO1自体、CAPN2‑STAT3の中継、IL‑33といった複数の有望な治療標的が浮かび上がりました。これらの経路を人に対して安全に調節するためにはさらなる研究が必要ですが、この機械感受性の内皮軸は、長年効果的な治療が得られなかった疾患に対する新しく物理的に根ざした切り口を提供します。
引用: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
キーワード: 肺線維症, 血管内皮細胞, 機械的シグナル伝達, PIEZO1, IL‑33