Clear Sky Science · ja
Plasmodiumのチューブリンの適応は異なる微小管構造、力学特性、薬剤感受性を決定する
マラリアの“骨格”が重要な理由
マラリア寄生虫は人の赤血球内で生き延びますが、同時に蚊やさまざまな組織を通り抜ける必要があります。そのために寄生虫は微小管と呼ばれる微小な管からなる内部の足場に依存しています。本研究は単純だが強力な問いを投げかけます:基本的な構成要素が私たちの細胞のものと非常によく似ているのに、なぜ寄生虫の微小管はそれほど特殊で頑丈なのか?答えは寄生虫が形を保つ仕組みだけでなく、我々の細胞に害を与えずに寄生虫の骨格を標的とする薬剤を設計する方法を示しています。 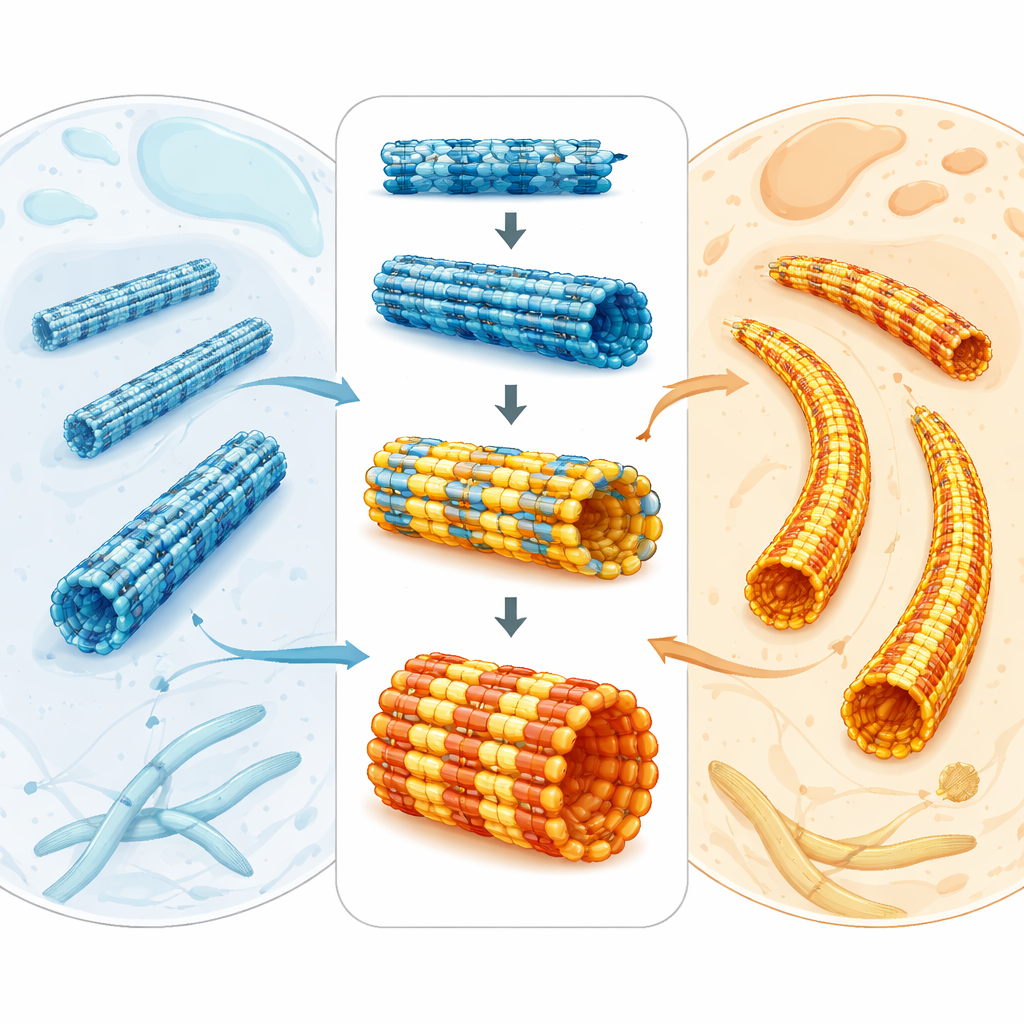
致命的な寄生虫の形を作る小さな管
微小管は細胞分裂、運動、形態維持を助ける中空のタンパク質管です。これらはチューブリンという対をなすタンパク質単位から構築されます。動物、植物、寄生虫を通じてチューブリンは驚くほど類似しており、それが異なる生物で微小管が見た目や振る舞いを大きく変える理由を説明しにくくしています。マラリア原虫Plasmodium falciparumでは、微小管は多様な配列を形成します:一部は動的で細胞分裂に関与し、他は寄生虫の外膜の下で長く剛直な支持構造を成します。これらの構造は寄生虫の成長と伝播に不可欠なため、特に現在の治療法に対する耐性が上昇する中で、有望な抗マラリア薬の標的となります。
寄生虫チューブリンを原子レベルで観る
研究者らはP. falciparumから直接チューブリンを精製し、高解像度のクライオ電子顕微鏡でそれがどのように微小管を組み立てるかを観察しました。これらの構造をよく研究された哺乳類脳由来の微小管と比較しました。一見すると寄生虫のチューブリンはヒト版とほぼ同一に見え、全体の折りたたみも同じです。しかし慎重な比較により、エネルギーを運ぶ分子(GTPやGDP)が結合する重要なポケットや特定の薬剤が作用する箇所の周囲に、小さな配列変化のクラスターが見つかりました。これらの微妙な変化は、隣接するヘリックスやループの位置を変え、とくにチューブリン二量体の表面で他のタンパク質や薬剤が結合する部位の形を変えます。本質的な設計図は保存されている一方で、局所的な調整が重要部位の形状を微妙に書き換えていることが示唆されます。
横方向の結合が強いことでより頑丈な管
微小管はポリマーです:多くのチューブリン二量体が端から端へ積み重なって原始フィラメントを作り、いくつかの原始フィラメントが並んで管の壁を形成します。チームは寄生虫の微小管では各原始フィラメントに沿った縦方向の接触は脳由来の微小管と非常によく似ていることを見出しました。差が現れるのは隣接する原始フィラメント間の横方向(ラテラル)接触です。接触面積は実際には寄生虫のほうがやや小さいにもかかわらず、シミュレーションはこれらの横方向結合が集合的に強く、格子(ラティス)をより剛直にしていることを示しました。微小管壁のパッチをコンピュータでモデル化すると、寄生虫のチューブリンは脳のチューブリンより曲がりやねじれが少ないことが示されました。実際の微小管末端の電子トモグラフィーは、寄生虫の微小管が短く、開いた原始フィラメントの広がりが小さい末端を持つことを確認しており、これはより頑丈な管の特徴です。 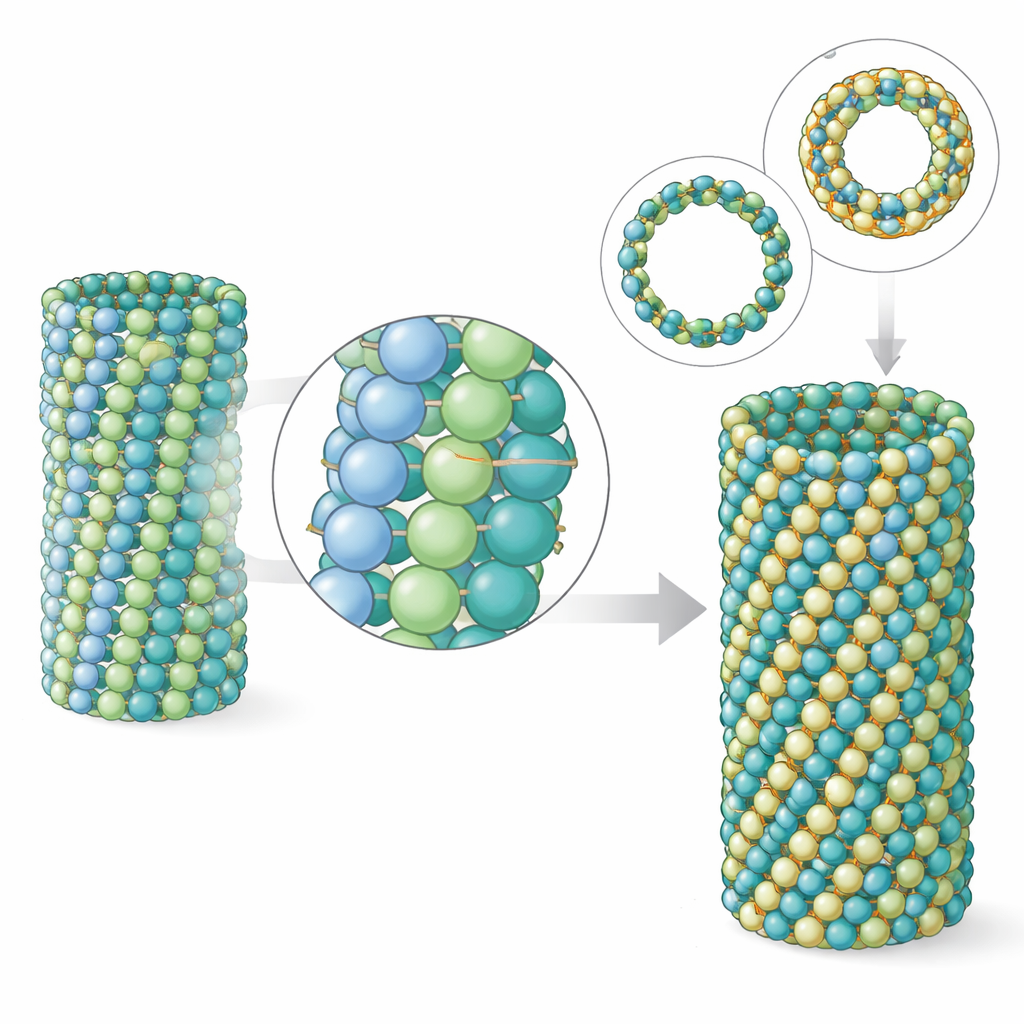
寄生虫の活動に合った異例の管径
P. falciparumのもう一つの顕著な特徴は、ある生活環でその微小管が標準的な13本ではなく、周囲により多くの構成要素を含むことがある点です—しばしば15本あるいは17本の原始フィラメントが見られます。研究チームは組み立て時に使用するヌクレオチドを変えることで、この挙動を試験管内で再現しました。成長状態を安定化するGTP様分子を用いると、寄生虫チューブリンは自然に15原始フィラメントの微小管を好みました。著者らはこれらの太い管の構造を解き、格子をわずかに傾けることで余分な原始フィラメントを収めつつ、ほぼ完全な円筒形を保っていることを示しました。実験室で作った15原始フィラメントの管を寄生虫細胞内で観察されるものと比較すると、形状と寸法の一致は非常に近く、補助タンパク質の群れではなくチューブリン自体の内在的特性だけで寄生虫特有の構造が生み出されることを示唆しています。
将来の寄生虫特異的薬剤への手がかり
本研究の結論は、進化が寄生虫のチューブリンを小さく散在する配列変化によって調整し、それが集合的に微小管の力学特性、構造、薬剤感受性を変えているということです。これらの微調整により寄生虫の微小管はより剛直になり、その過酷な生活史に適した非標準の管径を形成できる一方で、基本的なチューブリンの設計は認識可能なままです。医療にとって重要なのは、がん薬パクリタキセルのように薬剤結合ポケットの一部は寄生虫と宿主でほぼ同一に見えるため、選択的な抗マラリア薬の良い標的とはなりにくい点です。一方で、除草剤に類似した化合物オリザリンが結合すると考えられる部位などは、配列の変化と微妙な構造的変位を示しており、そこが寄生虫の微小管がヒトより脆弱な理由を説明し得ます。これらの微妙な違いを地図化することは、我々の細胞にはほとんど影響を与えずにマラリア寄生虫の骨格を攪乱する将来の薬剤設計のための設計図を提供します。
引用: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
キーワード: マラリア寄生虫, 微小管, チューブリン構造, 薬剤標的化, クライオ電子顕微鏡法