Clear Sky Science · ja
tRNA依存的なチロシン利用を標的化すると肝細胞癌の代謝的脆弱性が明らかになる
一般的な構成要素をがん細胞から奪う
肝臓がん細胞は、ほかの急速に増殖する細胞と同様に、タンパク質の小さな構成単位であるアミノ酸を安定的に必要とします。本研究は、最も一般的な肝臓がんである肝細胞癌が予想外の弱点を持つことを明らかにしました。すなわち、エネルギー産生と生存の両方にチロシンというアミノ酸を強く依存しているという点です。研究者らはチロシンの利用を選択的に制限することで、腫瘍増殖を抑え、がん細胞のエネルギー産生装置を損ない、治療に利用できる可能性のある細胞死を誘導できることを示しました。
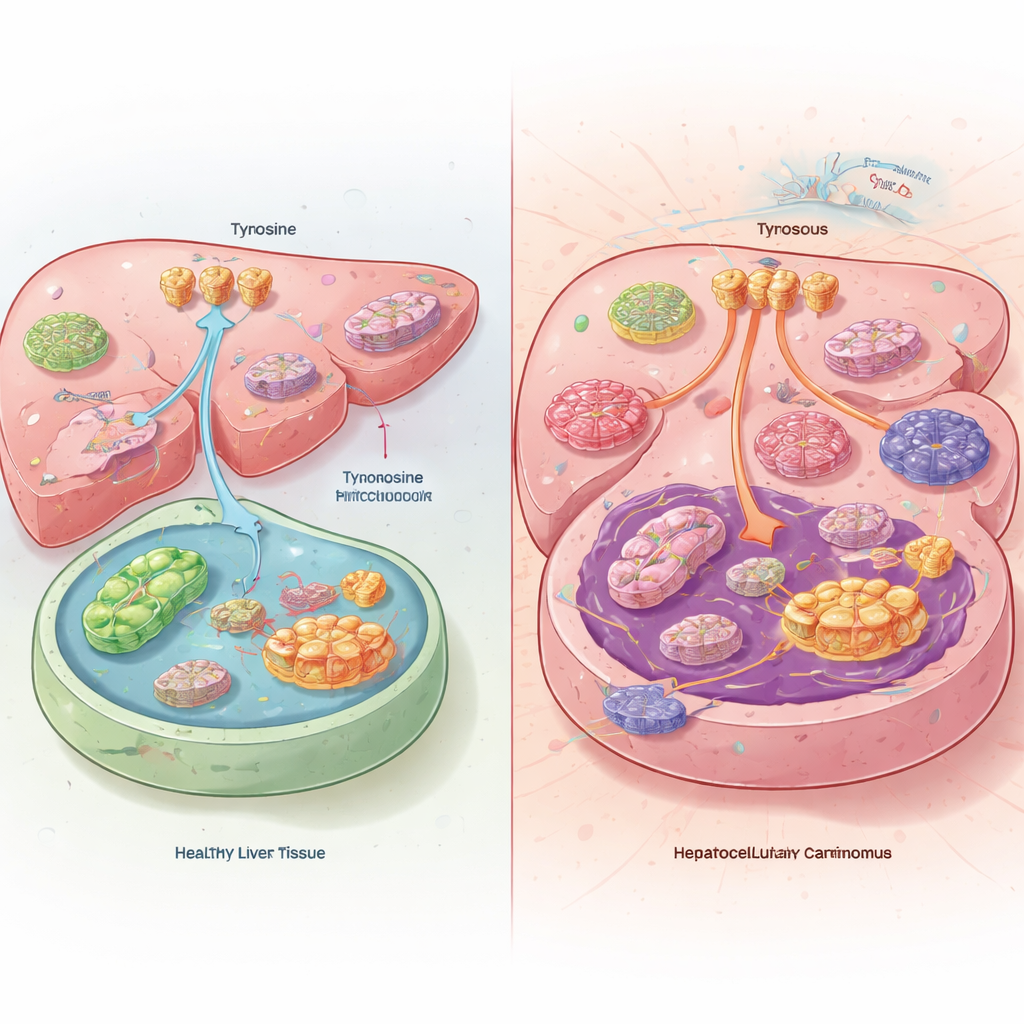
肝腫瘍に隠された不均衡
研究チームが患者およびマウスの肝腫瘍と正常肝組織を比較したところ、興味深い結果が出ました。がん細胞内のチロシン濃度は実際には低い一方で、腫瘍は血流からより多くのチロシンを取り込み、分解は少なくしていました。つまり、チロシンを燃料として消費するのではなく、タンパク質合成へと振り向けていたのです。腫瘍はこの仕組みを、細胞表面のチロシントランスポーターの活性を高め、肝臓で通常チロシンを分解する酵素の発現を下げることで実現していました。チロシンを含まない食事を与えたマウスでは腫瘍が小さくなり寿命が延び、逆に食事でチロシンを多く与えると腫瘍はより速く成長しました。
がんがタンパク質合成をどのように書き換えるか
研究者らはこのチロシン飢餓の原因を、強力ながん促進遺伝子であるMYCにたどりました。肝腫瘍ではMYCがYARS1というタンパク質をオンにし、YARS1は特定のトランスファーRNA(tRNA-TyrGUA)にチロシンを付加します。リボソームがチロシンを多く含むタンパク質を合成するには、この充填されたtRNAが必要です。本研究は、肝がんがYARS1とそれに対応するtRNAの両方を増強し、チロシンをタンパク質合成へ優先的に供給する回路を確保していることを示しました。この回路を断つ――チロシン濃度を下げる、YARS1やtRNA-TyrGUAをノックダウンする、またはチロシンの付加を阻害する――ことで、培養やマウスのモデルにおいて肝がん細胞の適応力は大幅に低下し、高いタンパク質生産需要に結びつく代謝的脆弱性が露呈しました。
エネルギー産生装置と脂質バランスの機能不全
全ゲノム規模のRNA、タンパク質合成、代謝物の計測を組み合わせて、研究チームはチロシン制限に特に敏感な二つの標的を特定しました。一つはNDUFB8で、ミトコンドリア複合体Iの構成要素であり細胞のエネルギー産生機構の核となります。もう一つはSCD1で、飽和脂肪を細胞膜や脂滴に安全に蓄えるための単価不飽和脂肪に変換するのを助けます。翻訳向けのチロシンが制限されると、NDUFB8とSCD1の産生は低下した一方で、それらのRNAレベルは大きく変わらなかったため、転写ではなく翻訳が影響を受けている明確な証拠となりました。その結果、複合体Iの組み立て不全、細胞呼吸の低下、過剰な活性酸素の発生、そして脂肪が単価不飽和から酸化されやすい多価不飽和へと傾く変化が起こりました。
鉄依存的な細胞死へがん細胞を追い込む
ミトコンドリア損傷と不安定な脂質の組み合わせは、脂質過酸化により駆動される鉄依存的な細胞死であるフェロプトーシスへ肝がん細胞を押しやりました。腫瘍はGPX4などの自然なフェロプトーシス阻害因子を増やして反撃しようとしましたが、大規模なCRISPR遺伝子編集スクリーンは、これらの保護因子を無効化するとチロシン制限がさらに致命的になることを示しました。細胞やマウスのモデルでは、チロシン制限戦略をGPX4またはBCL2を阻害する薬剤、あるいはソラフェニブやベネトクラクスのような既存の肝がん薬と組み合わせることで、腫瘍制御が強化され、腫瘍負荷が小さくなり生存が延長しました。
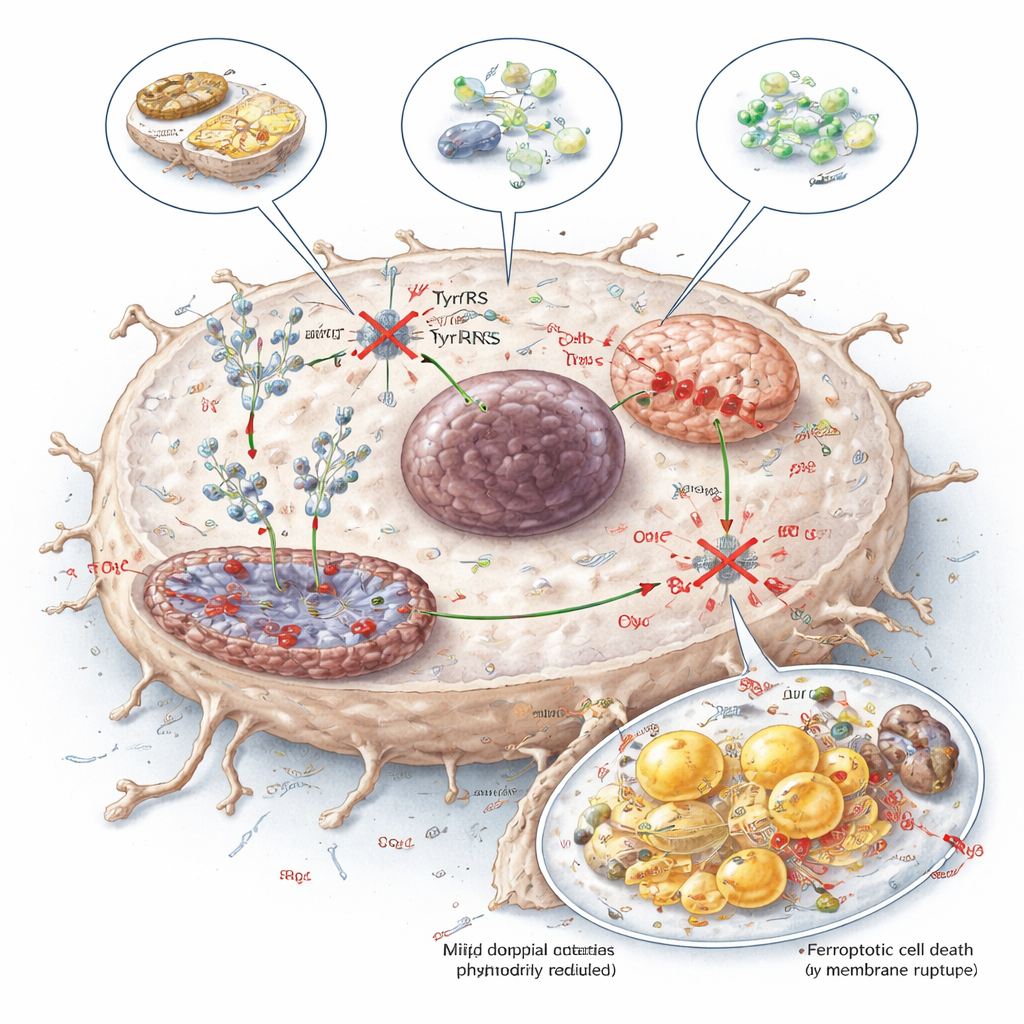
代謝的弱点を治療へと変える
この弱点を実際に利用する方法を探るため、研究者らは三つのアプローチを試しました:チロシン制限食、チロシンを酵素的に分解する酵素(TAL)、およびYARS1への結合を競合する小分子チロシノールです。いずれもタンパク質合成へのチロシン供給を減らし、NDUFB8とSCD1レベルを低下させ、ミトコンドリア機能を損ない、肝腫瘍でのフェロプトーシスを増加させました。一方でマウスの正常組織に対する影響は管理可能な範囲でした。一般向けに言えば、肝がんはチロシンを単なる栄養素としてではなく、そのタンパク質生産機構にとって精密な燃料として依存しているように見えます。食事、酵素、または薬剤によってこの依存を標的化することは、腫瘍を弱らせ既存治療の効果を高める有望な新しい方法を提供します。
引用: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
キーワード: 肝臓がん, アミノ酸代謝, チロシン, ミトコンドリア, フェロプトーシス