Clear Sky Science · ja
RNA G-四重鎖を例に示す変異特異的RNA構造と小分子相互作用の体系的同定
将来の医薬でRNAの小さな変化が重要な理由
私たちの多くは、個々人を特徴づける小さなDNAの違いを受け継いでいます。これらの微細な変化は、細胞内のRNA分子の折りたたみをわずかに変えることがあります。本研究は、そうした遺伝的な微調整がRNAを標的とする実験的な薬剤の結びつきをどのように変えるかを可視化する方法を示します。これは、特にがんや遺伝病において、同じ薬が人によって大きく異なる挙動を示し得るため重要です。
薬がRNAに触れる場所を新しく可視化する手法
多くの創薬者は現在、タンパク質だけでなくRNAも治療標的として注目しています。小分子は特定のRNA構造に結合して遺伝子の読み取りに影響を与え得ますが、従来の手法はほとんどが単一の「参照」RNA配列上でしか機能しませんでした。実際の患者に見られる無数の1塩基変異をほぼ無視してきたのです。著者らは、BIVID-MaPと呼ばれるハイスループット手法を開発し、数千のRNAバリアントを同時に検査して、それぞれのバリアントに対する小分子の結合部位を1塩基分解能で特定できるようにしました。 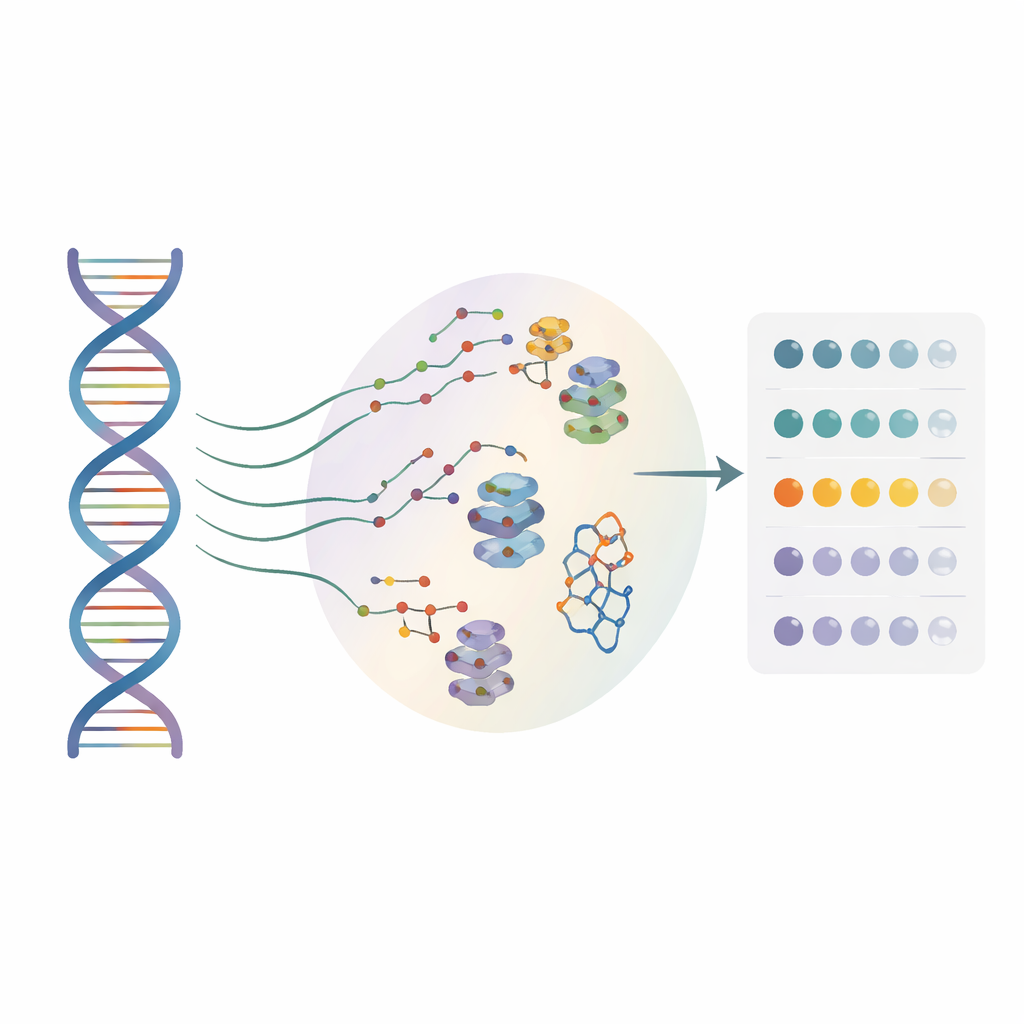
化学的マークを読み取れるシグナルに変換する
BIVID-MaPは主に三つの手順で機能します。まず、研究チームはRNAに結合する小分子に反応性タグを付加します。このタグ付き化合物が、グアニンに富む配列からできる緻密なG-四重鎖のような好ましいRNA構造に嵌まると、タグが近傍のRNA塩基と永久的な化学結合を形成します。次に、特殊な酵素が修飾されたRNAをDNAに転写しますが、これらの化学的マークに遭遇すると単一の塩基を「飛ばす」傾向があり、コピーに小さな欠失が生じます。最後に、ディープシーケンシングで数百万分子にわたるこれらの欠失の署名を読み取ります。周囲の配列のほとんどが保存されているため、欠失は混合プール中の特定の遺伝的変異に正確に割り当てられます。
制御されたテストケースで手法を実証する
BIVID-MaPが実際に変異特異的な結合を検出することを確認するため、研究者らは通常G-四重鎖を形成するCD44遺伝子のRNA断片を調べました。単一のG→A変化がこの構造を崩します。両方のバージョンを含む混合物では、ベンベリン(berberine)系のプローブに暴露した際、折りたたまれた領域付近で強い欠失シグナルを示したのは正常な形を保つ方のみであり、独立したアッセイもそこでの結合がより強いことを検証しました。同様の形を作れない変異体は欠失がはるかに少なく、結合も弱かったのです。他の一般的なマッピング技術はこの違いを見逃すか、混乱するバックグラウンドを生じさせることがあり、新手法の感度と特異性の向上が示されました。
多くの遺伝子にわたるがん関連変異の走査
研究チームはその後スケールアップしました。彼らは283のがん関連遺伝子からの5′非翻訳領域(5′ UTR)を収めたRNAライブラリを構築し、それぞれに腫瘍で報告された実際の体細胞変異を組み合わせました。G-四重鎖様構造を認識するプローブを用いることで、BIVID-MaPは小分子結合を強めるか弱める多数の変異を明らかにしました。DAXXやING2のような遺伝子では、グアニンに富む配列の単一塩基の変化が結合を著しく変え、G-四重鎖形成の独立した生物物理的検査や質量分析による直接結合測定とも一致しました。場合によっては、明らかなGトラクトの外側にある変異でさえ、近傍塩基の対合しやすさを微妙に変えることで結合をシフトさせ、予測される全体的な折りたたみを大きく変えずに構造の「アンサンブル」を再形成していました。 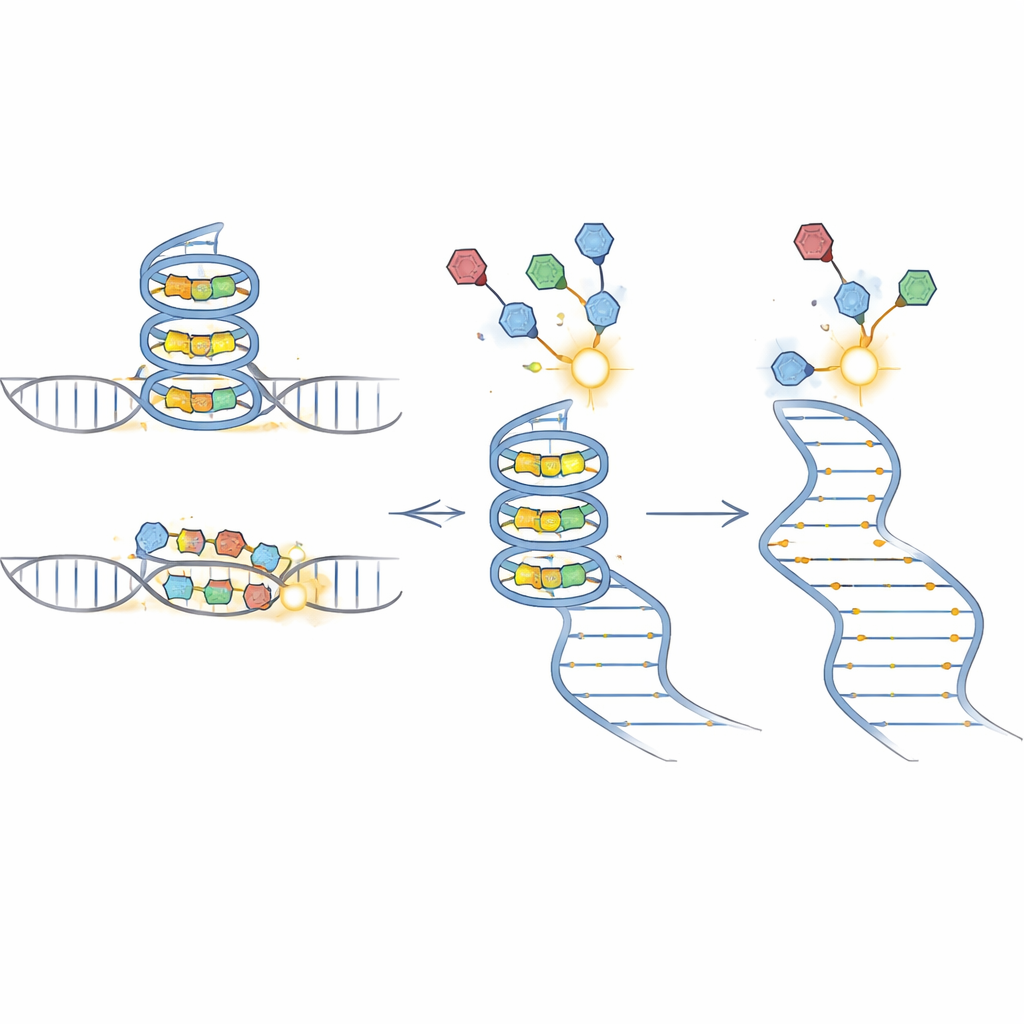
コンピュータ予測が見逃すものを見える化する
重要なのは、既存のRNA構造やG-四重鎖予測ツールがBIVID-MaPで明らかになった変化の多くを予測できなかったことです。計算スコアをほとんど変えないように見える変異が、実際には結合に大きな差をもたらす場合がありました。ある変異はG-四重鎖標的化化合物のファミリー全体に影響を与えるように見え、別の変異は薬剤特異的な影響を示しました。これは、1塩基変異が配列だけからは推測しにくい方法でRNAの折りたたみと薬剤との接触の景観を調整し得ることを示しています。
個別化されたRNA薬剤にとっての意義
著者らは、BIVID-MaPが個々の遺伝的差異がRNA構造と小分子薬との相互作用をどのように再形成するかをマッピングする強力な手段を提供すると結論づけています。局所的な化学修飾を正確な欠失署名に変換することで、この手法は何千もの変異を並列に調査し、薬剤結合を意味ある形で変える変異を浮き彫りにできます。長期的には、こうしたマップが多様な患者に対してより効果的で安全なRNA標的薬の設計を導き、これまで隠れていた新たな薬物標的となり得るRNA構造を明らかにする可能性があります。
引用: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
キーワード: RNAを標的とする薬, G-四重鎖, 遺伝的変異, 小分子の結合, がん変異