Clear Sky Science · ja
合成細胞における大規模収縮のためのFtsZリングの空間配置最適化
なぜ小さなリングが合成細胞構築で重要なのか
成長して自律的に二つに分かれる、単純な人工細胞を作ることを想像してみてください。そのためには、せっけんの泡のように柔らかい膜を、限られた生体部品だけで制御してつまむ方法を学ぶ必要があります。本研究は、細菌性タンパク質が脂質の巨大な泡上で大きく安定したリングを形成するよう手助けすることで、これらのモデル「細胞」がほぼ分裂に近いまで収縮できることを示します。どのようなタンパク質の構造が、細胞全体のスケールで膜を曲げ変形させるのに必要かを明らかにしています。
自然の分裂ツールキットを借りる
多くの細菌はFtsZというタンパク質を使って分裂します。FtsZは、私たちの細胞で内部骨格を作るチューブリンの遠縁で、フィラメントを組み立てて細胞の中央にリングを形成し、分裂位置を標します。生細菌では、多数の補助タンパク質がこのリングを内膜に付着させ、中央に位置づけ、細胞壁を再構成する酵素と結びつけます。これまでの試みでは、細胞大の小胞内でこの機構を再現してリング形成や局所的なへこみを引き起こすことはできても、巨大な小胞を滑らかに連続的に収縮させてほぼ二つの半分へと形作るような進行性の収縮は達成されていませんでした。
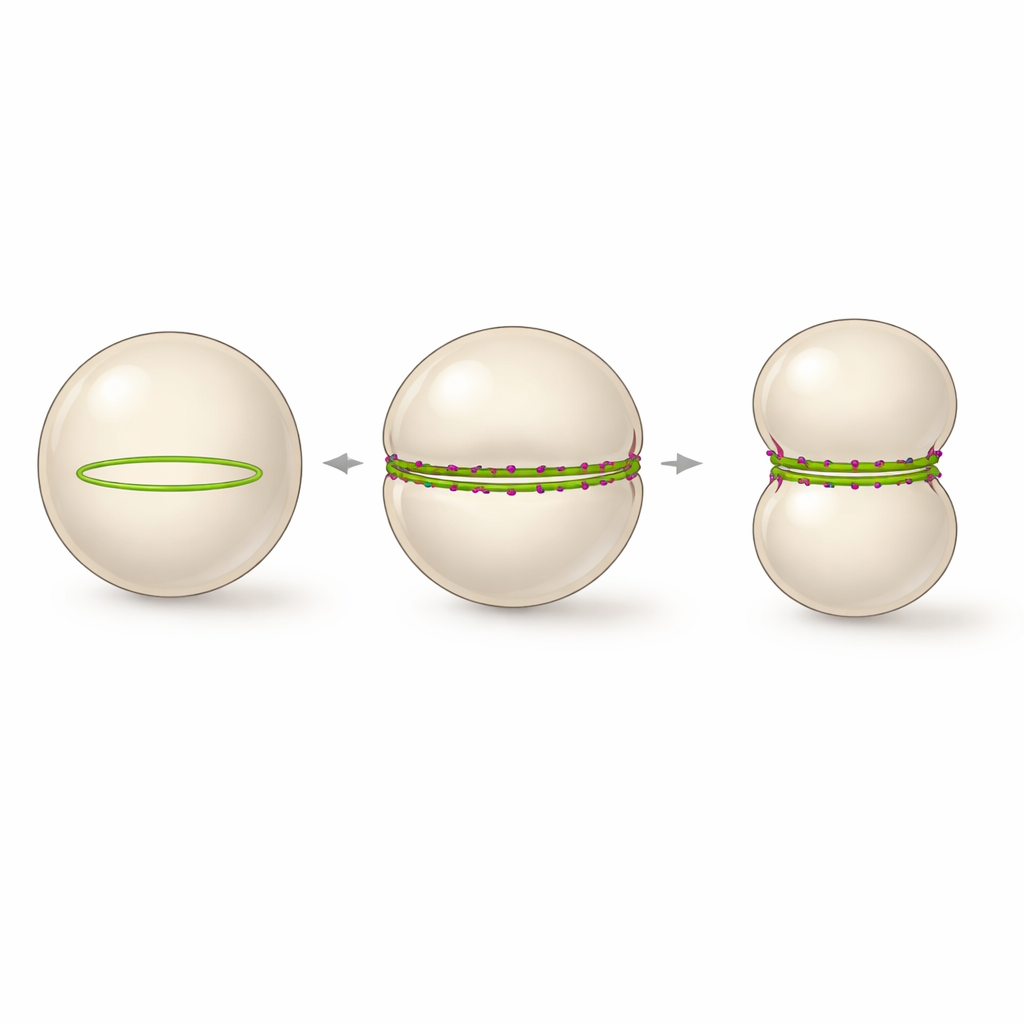
分裂膜に対するミニマリストのアプローチ
著者らは、このシステムを二つの要素だけにまで削ぎ落とせるかを問いました:膜に直接付着できる改変型FtsZと、別の分裂タンパク質FtsN由来の短い正電荷を帯びた末端片です。彼らはこれらを巨大一重膜小胞(合成細胞に似た空洞の脂質球)内に封入し、タンパク質の動態を調整するためにエネルギー分子GTPと作用の遅いGTP模倣体を供給しました。FtsN末端がない場合、FtsZは多数の小さなリングやパッチを形成して局所的なくぼみしか生じませんでした。FtsN断片(cytoFtsNと呼ばれる)を過剰に加えると、それらの小さなリングは再編成され、赤道付近を取り巻く単一の大きなリングとなり、数時間かけて収縮できるようになりました。
もつれたネットワークから単一の収縮リングへ
この小さなペプチドが挙動をここまで劇的に変える仕組みを理解するため、チームは支持膜上の平坦面でFtsZフィラメントを高解像度顕微鏡で観察しました。通常、こうした表面上のFtsZは渦を巻く曲がった回転模様を作ります。cytoFtsNを徐々に増やすと、これらの渦は次第に消え、より直線的で整列したバンドルに置き換わりました。定量的な画像解析は、ペプチド濃度が上がるにつれてネットワークがより一貫性と秩序を帯びることを確認しました。蛍光回復実験では、これらのバンドル内のサブユニット交換が遅くなることが示され、ペプチドがフィラメントを安定化してその回転するような動態を抑えていることが示唆されました。

フィラメントを結びつける静電的“ベルクロ”
生化学的測定により、cytoFtsNとFtsZの相互作用は主に逆の電荷によることが示されました:FtsZは概して負電荷である一方、ペプチドは正電荷のクラスターを持っています。塩濃度が低いほどペプチドの結合が強く、溶液中でより太いFtsZバンドルの形成を促し、フィラメントの分解を遅らせることでGTP加水分解活性を抑えました。研究者がペプチド中の重要な正電荷残基を変えたり、静電引力を遮蔽するために塩濃度を上げると、束化や再編成の効果は消失しました。これは、正に帯電したペプチドが分子的な“ベルクロ”のように働き、FtsZフィラメント間の反発を減らして横並びに詰め込みやすくし、剛直な束を形成させるという単純な物理的機構を示しています。
単一のリングが巨大小胞をどのように形作るか
小胞内では、このペプチドによる束化の安定化が劇的な結果をもたらします。多数の小さな曲がったリングの代わりに、直線化されたFtsZバンドルは小胞の大きな曲率に沿うよう強制され、全周を覆う一つの連続したリングとして組み上がります。タイムラプス観察では、このような完全に閉じたリングが形成されるたびに、小胞は球形からダンベル形へ確実に変形し、リングが位置するところにきついくびれが生じることが示されました。プロセスは小胞径が縮小し収縮が深まる様子としてリアルタイムで追跡でき、区画はほぼ二つに分かれそうになりますが、最終的な切断までは達しませんでした。著者らは、減速しつつも活性を保つ安定した赤道にまたがるFtsZリングが、合成細胞で大規模な膜収縮を駆動するための最小限の構造であると提案しています。
将来の合成生命への含意
膜に固定されたFtsZ変異体と短い陽性ペプチドだけで巨大脂質小胞をほぼ分裂に近い形まで変形できることを示すことで、本研究は人工細胞の明確な設計規則を提示します:細胞サイズに見合った、時間的に機械的に安定した単一の一貫したタンパク質リングがあれば、細胞スケールの柔らかい境界をつまむのに十分だということです。膜を完全に切断するためにはより複雑な因子が必要かもしれませんが、本研究は大規模な制御された収縮が細菌の分裂タンパク質一式を必要としないことを示しています。代わりに、フィラメントの組織化と動態を慎重に調整することで、単純なタンパク質足場が効果的な収縮リングへと変わり、本当に自己分裂する合成細胞に一歩近づけることが示されました。
引用: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
キーワード: 合成細胞の分裂, FtsZリング, 膜の収縮, 最小分裂装置, 細胞骨格の自己組織化