Clear Sky Science · ja
単一分子ダイナミクスが示す、ATP結合だけで基質輸送を駆動するABCトランスポーター
微小な細胞ポンプが重要な理由
体内のあらゆる細胞は、分子を膜を越えて移動させる微小な機械に依存しており、栄養取り込みから免疫防御までさまざまな過程を形作っています。これらの機械の主要なクラスの一つであるABCトランスポーターは、細胞の化学燃料であるATPを使って貨物を自然な勾配に逆らって運びます。しかし長年にわたり基本的な疑問が議論されてきました:輸送の駆動に必要なのはATPが結合するという単純な動作だけなのか、それともATPが分解されるときに初めてエネルギーが放出されるのか。今回の研究は、単一のトランスポーターを分子ごとに詳しく追うことでその議論に決着をつけます。
一度に一つのトランスポーターを観る
何百万もの分子の挙動をまとめて測る代わりに、研究者たちは個々の輸送イベントをリアルタイムで追跡できる実験系を構築しました。彼らは、キラーT細胞に提示する免疫ペプチドを積むヒトのTAPの細菌に相当するTmrABに注目しました。TmrABは膜に埋まり、ATPを用いて短いタンパク質断片(ペプチド)を一方の側から他方へと運びます。各輸送段階を観察するために、チームは単一のTmrAB分子を人工膜の泡(リポソーム)に閉じ込め、その泡の内側に入れた特注の“センサー”タンパク質を用いました。このセンサーはペプチドを捕まえると蛍光が変化します。高感度顕微鏡を用いることで、光信号の短いジャンプとして、一つずつペプチドが泡の内部に到着する瞬間を正確に見ることができました。
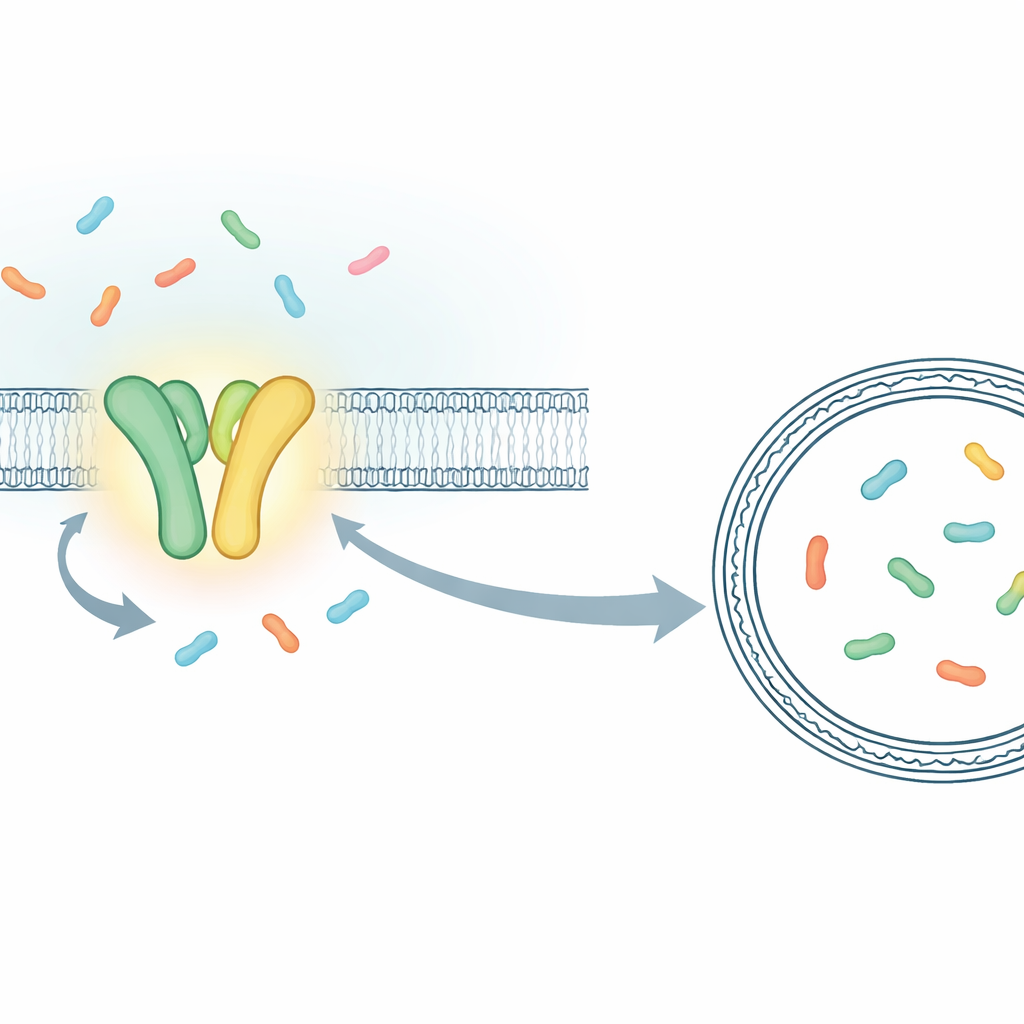
1つのATP結合が1つのペプチドを動かすことの証明
この単一分子アッセイを用いて、研究者たちは通常のTmrABとサイクルの進行が遅く伸びた変異型を比較しました。遅い変異体は個々のイベントを識別しやすくし、通常ならば重なって見える出来事を分離できました。ATPとペプチドが同時に存在するとき、リポソーム内のセンサーは「空」の状態から「満たされた」状態へ段階的に変化し、それぞれが1つのペプチドの輸送に対応することを示しました。センサーがペプチドを取り囲む速さを解析し、各リポソーム内の微小な体積を推定することで、これらの光の変化を概算のペプチド濃度に換算することさえできました。得られた数値は、直径約100ナノメートルの泡に1個、次に2個のペプチドが蓄積する場合に期待される値と一致し、彼らが輸送イベントを一つずつ数えていることを裏付けました。
ATP結合だけで分子スイッチが切り替わる
主要な論点はMg2+イオンに関するものです。Mg2+は細胞内で通常ATPに伴い、ATPの効率的な分解に必要とされています。あるモデルでは、Mg2+がATPの結合やトランスポーターの閉鎖にも必要であると示唆されていました。これらの役割を分けて調べるために、研究者たちはキレート剤でMg2+を除去しつつATPは供給しました。この条件下で、通常型と遅延型のトランスポーターはそれぞれ分子当たりちょうど一回のペプチド輸送を実行しましたが、その後停止しました。この挙動は、Mg2+がなくてもATPは結合でき、輸送体を内向きから外向きの形に切り替えてペプチドを動かすことができることを示しています。しかしMg2+がないとATPを効率的に分解できないため、トランスポーターは次のサイクルに備えてリセットできません。
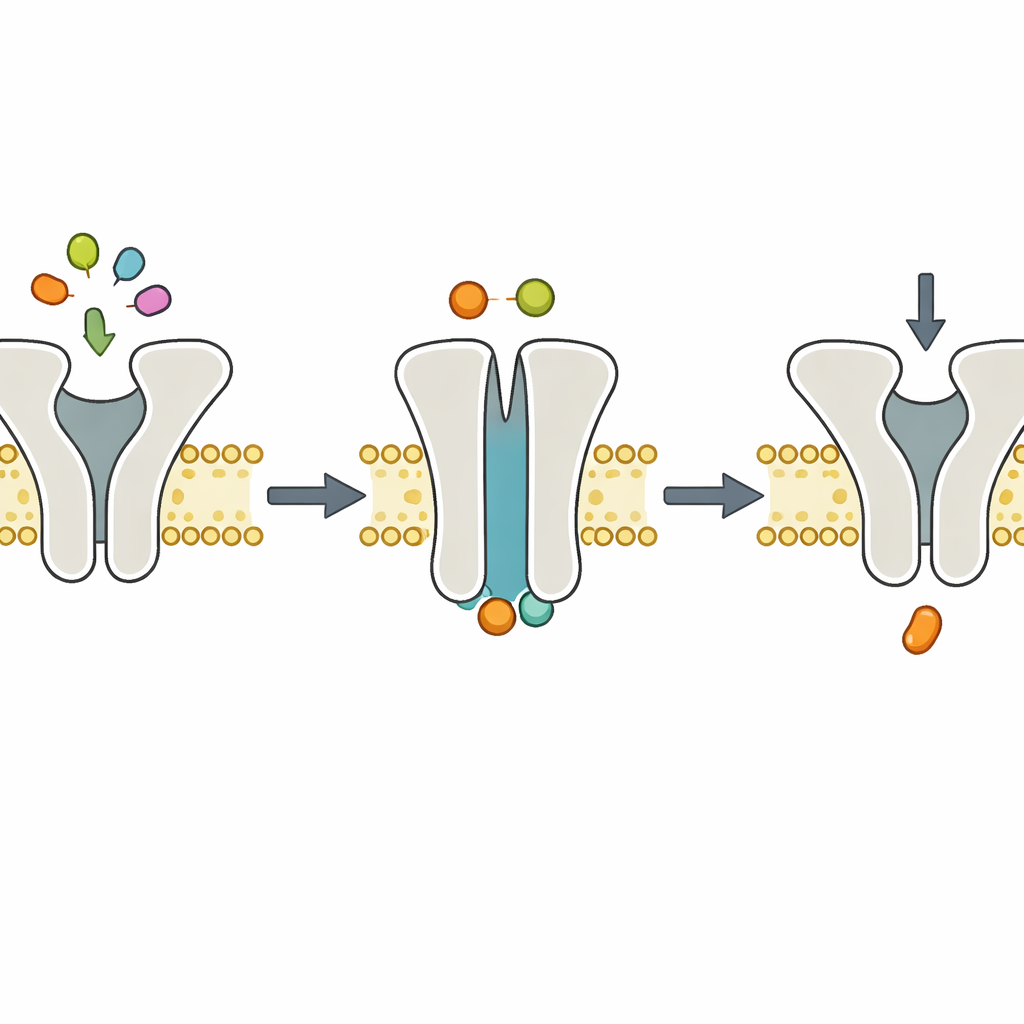
構造スナップショットが動的観察を裏付ける
Mg2+欠乏のステップで機械がどのように見えるかを確認するために、チームはクライオ電子顕微鏡を用いました。これは瞬間凍結された分子を原子近傍の詳細で描き出します。彼らはTmrABを脂質ナノディスクに再構成し、Mg2+なしでATPを加えて複合体を凍結しました。得られた構造は、TmrABが外向きの“閉塞”構造をとり、ATPが両方の内部結合部位に挟まっているがMg2+は見えない、というものでした。これらのスナップショットは、ATPとMg2+が両方ある場合に得られる以前の構造と本質的に区別がつきませんでした。加えて、Mg2+がないとATP分解が完全に停滞することを示す生化学的アッセイの結果もあり、これらは単純な役割分担を支持します:ATP結合がペプチドを移動させる構造変化を駆動し、Mg2+依存のATP加水分解が回復(リセット)段階を担う、ということです。
細胞ポンプの働きのより明確な絵
単一トランスポーターを観察しその構造を解くことで、本研究はABCトランスポーターに関する長年の疑問に決着をつけます:ペプチドを動かす機械的なパワーストロークはATPの後の化学分解ではなく、ATPの結合自体によって引き起こされる。Mg2+は主にATPを分解できるようにするために関与し、その結果としてトランスポーターが再び働けるようにリセットされます。基本的な細胞生物学の一断面を明らかにしたことに加え、この単一分子アプローチは、免疫、薬剤耐性、さまざまな疾患の基盤となるほかの膜機械を一分子ずつ、一輸送ステップずつ詳細に解析するための青写真を提供します。
引用: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
キーワード: ABCトランスポーター, ATP結合, 単一分子FRET, 膜輸送, TAPとTmrAB