Clear Sky Science · ja
キラルなペプチドグリカン模倣体が細菌の壁合成を標的にして病原体介入を行う
有害な病原体を見つける新しい方法
抗生物質耐性の感染症は世界中で増加していますが、医師は依然として自分の細胞を傷つけずに危険な細菌だけを精密に検出して攻撃できるツールを欠いています。本研究は、細菌の細胞壁の重要な構成要素を模した巧妙な分子「デコイ(おとり)」を紹介します。これらの設計分子は感染部位をイメージングで明るく示すと同時に、抗生物質を直接微生物に運ぶことができ、治療困難な病原体に対抗する新たな戦略を提供します。
細菌の鎧を模倣する
細菌は糖と、我々の細胞ではほとんど使われない特殊な鏡像アミノ酸からなる頑丈な網状の細胞壁に包まれています。研究者らはこの差異を利用して、特定の鏡像(D)型アラニンで装飾された長い糖鎖を作成しました。これらの鎖はキラルなペプチドグリカン模倣体と呼ばれ、細菌が壁を合成する際に用いる天然成分に非常に似るよう設計されていますが、哺乳類組織には存在しません。D型アラニンの付加量を精密に調整することで、ヒト細胞よりも細菌を強く選択するバージョンを作り出しました。
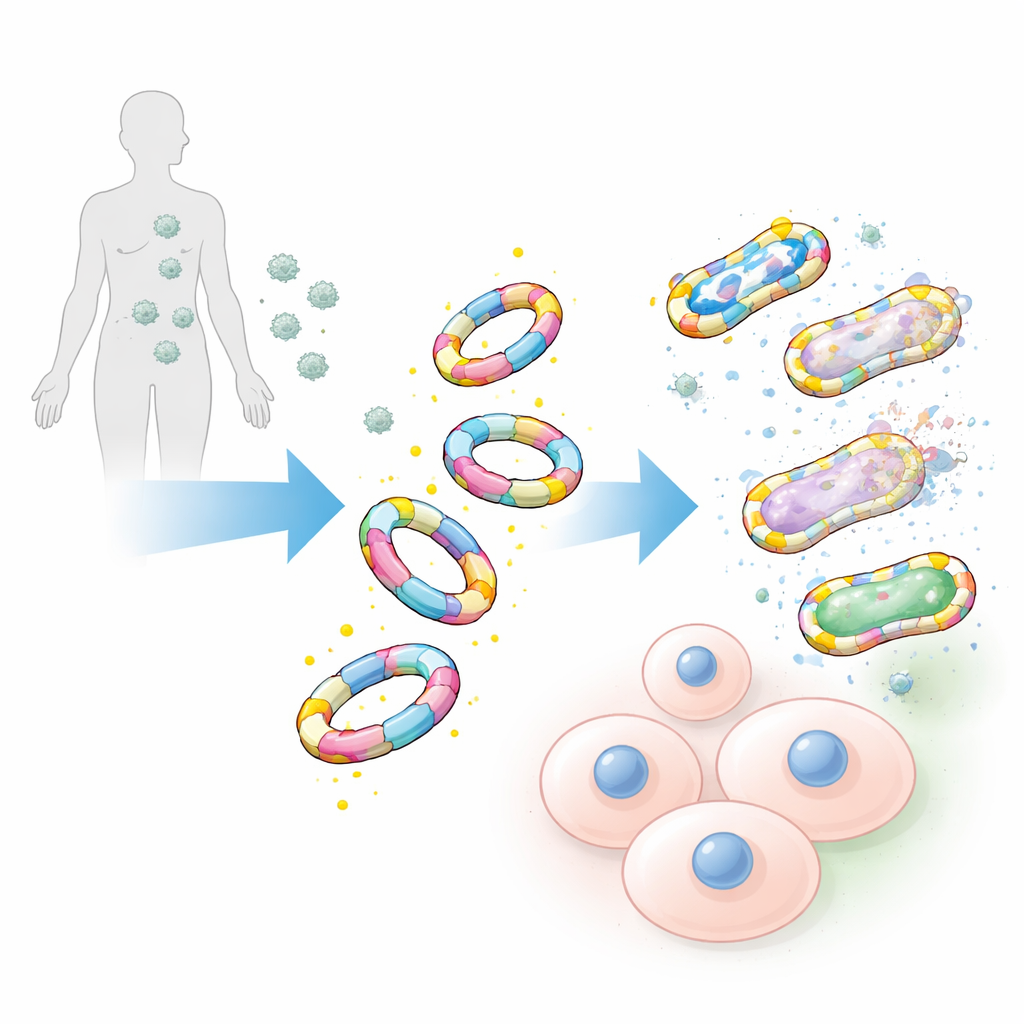
我々の細胞ではなく細菌に特異的に結合する
メチシリン耐性黄色ブドウ球菌などの悪名高い院内株やその他のESKAPE菌を含む幅広い病原体に対する試験で、D-アラニンで飾られた模倣体は細菌表面に著しく効率よく結合しました。一方、L型アラニンで作られた鏡像の対照体や元の糖鎖のみは、弱いあるいはほとんど結合を示しませんでした。研究チームは、これらの大型模倣体を単一のD-アラニン分子に基づく従来の小さな化学プローブと比較しました。小型プローブを非常に明るくしても、ラベルされる細菌は遥かに少なく、信号も弱いままであり、より大きく実物に近い設計の優位性が強調されました。
細胞壁合成ラインを乗っ取る
認識がこれほど強くなる仕組みを理解するため、研究者らは模倣体が細菌の壁構築機構とどのように相互作用するかを調べました。D-アラニン由来の鎖は単に外側に付着するだけでなく、本物の構成要素として取り込まれ、通常細胞壁の成分を結合する同じ酵素反応段階に送り込まれることがわかりました。化学解析では、これらの模倣体が存在するときにのみ生じる新しい中間体分子が検出され、計算シミュレーションは主要な壁構築酵素が模倣体を天然基質よりも強く把握することを示しました。数回の細菌増殖サイクルを経て、模倣体は壁に蓄積し、その構造を徐々に歪め、漏れやすくしました。
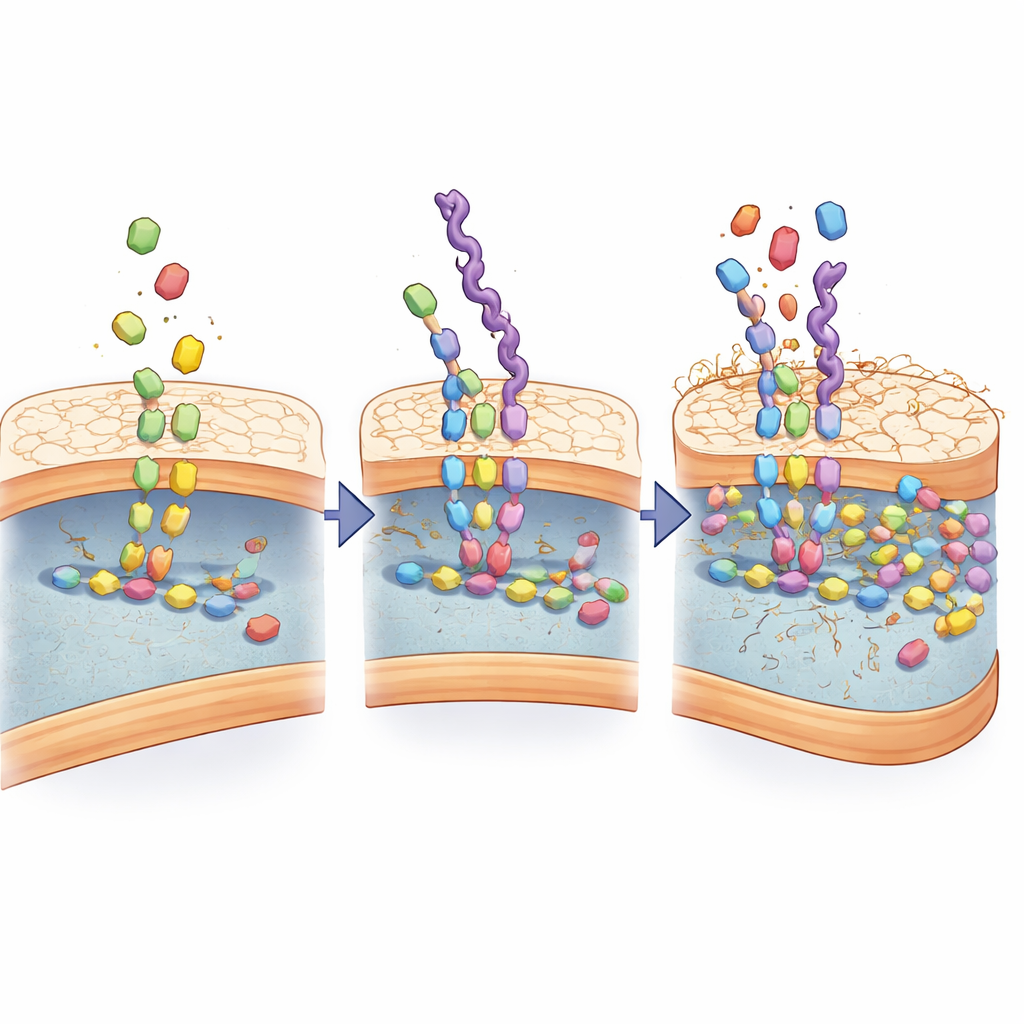
模倣体をスマートな薬物運搬体に変える
これらの鎖は水中で自然に微粒子を形成し、多くの化学的ハンドルを持つため、研究チームはそれらをイメージング色素や抗生物質の足場として利用しました。蛍光化したバージョンは細胞培養中の細菌を明瞭に描出し、同培養に共存する哺乳類細胞とはほとんど相互作用しませんでした。次に研究者らは模倣体ベースの粒子にテトラサイクリンを搭載しました。実験室での試験では、この被覆によりテトラサイクリンの有効性が数倍に高まり、遊離薬に比べてはるかに低用量で耐性株さえも殺菌しました。顕微鏡観察では、抗生物質を搭載した模倣体が細菌に密集し、その被膜に浸透して、非標的の製剤と比べて広範な細胞死を引き起こしていることが明らかになりました。
体内での感染と戦う
最も厳しい試験は、局所的な皮膚創傷と致命的な腹腔内感染のマウスモデルで行われました。感染した創傷では、蛍光化した模倣体が組織深部の細菌に集積し、テトラサイクリンを運搬した場合にはほぼ完全に微生物を除去しました。これにより治癒が速まり、新しい皮膚が厚くなり、コラーゲンの沈着が整い、小血管の再生も促進されました。全身感染モデルでは、模倣体は脾臓や肺など感染した臓器に特異的に蓄積し、抗生物質を搭載した際には細菌数を大幅に減少させました。重要なことに、模倣体単独の高用量でも主要臓器や血液化学に明らかな損傷は見られず、安全性は良好でした。
将来の治療にとって何を意味するか
細菌の細胞壁の成分に化学的に近い類似物を構築することで、本研究は外部からただ攻撃するのではなく病原体の代謝に「溶け込む」新しい方法を示しました。これらのキラル模倣体は、高精度のイメージング用ビーコンであると同時に、抗生物質を微生物の標的に直接誘導するスマートな輸送体として機能し、耐性株を含む標的を攻撃しつつ哺乳類細胞を保護します。臨床応用に翻訳されれば、このような生体模倣プラットフォームは医師が感染箇所を正確に把握し、より低用量で効率的に治療するのに役立ち、増大する抗菌薬耐性という課題に対する有望な武器となる可能性があります。
引用: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
キーワード: 抗生物質耐性, 細菌細胞壁, 標的薬物送達, 分子イメージング, ナノ医療